جيسون واسرمان MD PhD FRCPC
28 تشرين الثاني، 2025
سرطان الغدد القنوي هو النوع الأكثر شيوعًا من سرطان البنكرياس. يبدأ من الخلايا التي تبطن الأنابيب الصغيرة (القنوات) داخل البنكرياس. تساعد هذه الخلايا عادةً على نقل السوائل الهضمية التي ينتجها البنكرياس إلى الأمعاء الدقيقة. في سرطان الغدد القنوية، تبدأ هذه الخلايا بالنمو بشكل غير طبيعي. غزا الأنسجة المحيطة. مع مرور الوقت، قد ينتشر السرطان إلى الأعضاء المجاورة أو أجزاء بعيدة من الجسم.
أين يوجد هذا الورم عادة في البنكرياس؟
يُوجد حوالي ثلثي أورام الغدد القنوية في رأس البنكرياس (الجزء الأقرب إلى الأمعاء الدقيقة). أما البقية فتُوجد في جسم الغدة أو ذيلها. معظم الأورام منفردة، أي أن هناك ورمًا واحدًا فقط في البنكرياس.
ما هي أعراض سرطان غدي الأقنية؟
يعاني العديد من المصابين بسرطان الغدد القنوية من أعراض مثل التعب، وفقدان الشهية، وعسر الهضم، وفقدان الوزن، أو ألم في الجزء العلوي من البطن أو الظهر. إذا سد الورم القناة الصفراوية، فقد يُسبب اليرقان، الذي يُسبب اصفرار الجلد والعينين. يُشخص بعض المصابين بعد ظهور أعراض جديدة لمرض السكري أو الاكتئاب. في الحالات الأكثر تقدمًا، قد تُسبب الأعراض انتشار السرطان إلى الكبد أو أعضاء أخرى.
ما الذي يسبب سرطان غدي الأقنية؟
يُعد التدخين عامل الخطر الأكثر شيوعًا. تشمل عوامل الخطر الأخرى السمنة، وداء السكري، والتهاب البنكرياس المزمن، والتاريخ العائلي للإصابة بسرطان البنكرياس. كما قد يزيد الإفراط في تناول الكحول من خطر الإصابة. يرث بعض الأشخاص جينات... الطفرات (التغييرات) التي تزيد من خطر الإصابة بسرطان البنكرياس، بما في ذلك التغييرات في B، CDKN2A، أو جينات إصلاح الحمض النووي الأخرى.
كيف يتم هذا التشخيص؟
عادةً ما يُشخَّص سرطان الغدد القنوية في البنكرياس بعد إجراء خزعة، حيث تُؤخذ قطعة صغيرة من الأنسجة ويفحصها أخصائي علم الأمراض تحت المجهر. تُجرى معظم الخزعات باستخدام إبرة دقيقة أثناء فحص الموجات فوق الصوتية بالمنظار (EUS)، مع أن بعضها يُؤخذ أثناء الجراحة. بعد تأكيد التشخيص من خلال خزعة صغيرة، قد تُجرى جراحة لاحقًا لإزالة الورم بأكمله إذا لزم الأمر.
الميزات المجهرية
تحت المجهر، يتكون سرطان الغدد القنوية من غدد غير طبيعية تنمو بشكل غير منتظم وتغزو أنسجة البنكرياس المحيطة. غالبًا ما تكون هذه الغدد غير منتظمة الشكل والحجم، وقد تحتوي على المخاط، وهو مادة هلامية تُنتجها عادةً خلايا القناة البنكرياسية. عادةً ما يُظهر النسيج المحيط بالورم تفاعلًا كثيفًا وليفيًا، وهو استجابة للنمو الغازي. في الأورام الأكثر عدوانية، قد تفقد الخلايا السرطانية بنيتها المكونة للغدد، وتُشكل بدلاً من ذلك صفائح صلبة أو تُظهر اختلافًا ملحوظًا في الحجم والشكل.
المناعية
غالبًا ما يُجري أخصائيو علم الأمراض فحص الكيمياء المناعية (IHC) لدعم التشخيص. الكيمياء المناعية هي اختبار يستخدم أجسامًا مضادة مرتبطة بأصباغ لتسليط الضوء على بروتينات محددة داخل خلايا الورم. تساعد أنماط التلوين هذه على تأكيد أن الورم بدأ في البنكرياس واستبعاد أنواع أخرى من السرطان التي قد تبدو مشابهة تحت المجهر. على الرغم من عدم وجود بروتين واحد يُحدد سرطان القناة البنكرياسية الغدي بمفرده، إلا أن مجموعات معينة من العلامات تدعم التشخيص. تُنتج معظم الأورام بروتينات تُرى عادةً في خلايا القناة البنكرياسية، مثل CK7 وCK8 وCK18 وCK19، وقد تُظهر أيضًا تلوينًا لـ CEA وCA19-9 وCA125 وMUC1 (EMA) وMUC5AC وDUPAN-2. هذه البروتينات مفيدة ليس فقط للتشخيص، ولكن أيضًا لأن بعضها يُستخدم لمراقبة الاستجابة للعلاج.
تكون الصبغات الأخرى سلبية، مما يساعد على استبعاد الأورام المشابهة. على سبيل المثال، عادةً لا يُظهر سرطان الغدد القنوية (الغدي القنوي) بروتين الفيمنتين، أو علامات الغدد الصماء العصبية مثل السينابتوفيزين أو الكروموجرانين أ، أو علامات الخلايا الأسينية مثل التربسين أو BCL10. يساعد هذا النمط على التمييز بين سرطان الغدد القنوية وأورام الغدد الصماء العصبية أو سرطان الخلايا الأسينية.
تُظهر العديد من سرطانات الغدد القنوية فقدانًا لبروتينات مثبطة للورم، مثل SMAD4 (DPC4) وp16 (CDKN2A)، والتي تُساعد عادةً في التحكم بنمو الخلايا. ويدعم فقدان هذه البروتينات تشخيص السرطان. ومن البروتينات الأخرى المُتغيرة بشكل شائع بروتين p53. في حوالي 75 إلى 80% من الحالات، يكون p53 إما مُنتجًا بشكل مفرط أو مفقودًا تمامًا في خلايا الورم - وكلا النمطين غير طبيعيين ويدعمان التشخيص.
في الحالات الصعبة، مثل الأورام ذات السمات غير العادية أو عندما يكون من غير الواضح ما إذا كان السرطان قد بدأ في البنكرياس أم في عضو مجاور، تُعدّ الكيمياء المناعية مهمةً للغاية. يجمع أخصائي علم الأمراض نتائج هذه الاختبارات مع المعلومات السريرية ودراسات التصوير للوصول إلى التشخيص النهائي.
الصف النسيجي
التقييم النسيجي هو وسيلةٌ يُمكِّن أخصائيي علم الأمراض من وصف مدى اختلاف مظهر وسلوك خلايا الورم مقارنةً بالخلايا الطبيعية في البنكرياس. يُوفِّر التقييم معلوماتٍ مهمةً حول مدى عدوانية الورم، ويُساعد في توجيه قرارات العلاج.
لتحديد الدرجة، يقوم أخصائي علم الأمراض بفحص الورم تحت المجهر وينظر إلى العديد من الميزات الرئيسية:
-
التمايز الغدييشير هذا إلى مدى قدرة خلايا الورم على تكوين هياكل تشبه الغدد. تُعتبر الأورام التي تُشبه إلى حد كبير البنية الغدية الطبيعية للبنكرياس جيدة التمايز. أما الأورام التي تُشكل غددًا أقل أو غير منظمة، فتُصنف على أنها متوسطة أو ضعيفة التمايز.
-
إنتاج المخاطالمخاط مادة هلامية تُنتجها غدد البنكرياس عادةً. قد تختلف سلوكيات الخلايا السرطانية التي تُنتج مخاطًا أقل أو غير منتظم عن تلك التي تُنتج مخاطًا أكثر.
-
نشاط الانقسامية: الانقسام المتساوي هي العملية التي تنقسم بها الخلايا. يحصي علماء الأمراض عدد خلايا الورم النشطة في الانقسام. الأورام ذات النشاط الانقسامي العالي أكثر عرضة للنمو والانتشار بسرعة.
-
المميزات النووية: نواة هو مركز التحكم في الخلية. في السرطان، غالبًا ما تحتوي خلايا الورم على نوى متضخمة أو غير منتظمة أو داكنة اللون. درجة التغير النووي تُحدد درجة الورم.
إذا أظهر الورم مناطق ذات درجات مختلفة (تُسمى التباين داخل الورم)، تُعتمد أعلى درجة للتشخيص النهائي. يضمن هذا النهج مراعاة حتى المناطق الصغيرة من الورم الأكثر عدوانية.
بناءً على هذه الميزات، يتم تقسيم سرطان القناة الغدية في البنكرياس إلى ثلاث درجات:
-
متباينة بشكل جيدتبدو خلايا الورم مشابهة للخلايا الطبيعية، وتُشكل غددًا مُنظمة، وتنقسم ببطء. عادةً ما تنمو هذه الأورام وتنتشر بمعدل أبطأ.
-
متباينة بشكل معتدل:تختلف خلايا الورم بشكل أكبر عن الخلايا الطبيعية، وتنقسم بوتيرة أكبر. ويكون تكوين الغدد أقل تنظيمًا.
-
متباينة بشكل سيءتبدو خلايا الورم غير طبيعية للغاية، وغالبًا ما تُكوّن عددًا قليلًا من الغدد أو لا تُكوّن أي غدد، وتنقسم بسرعة. هذه الأورام أكثر عدوانية وأكثر عرضة للانتشار.
درجة الورم عامل مهم في التنبؤ بنتائج المريض. الأورام عالية الدرجة ترتبط بانخفاض فرص النجاة، وقد تتطلب علاجًا مكثفًا.
الأنواع الفرعية النسيجية لسرطان الغدة القنوية
الأنماط الفرعية النسيجية هي أنماط مختلفة يمكن أن تُشكلها خلايا السرطان عند فحصها تحت المجهر. تُحدد هذه الأنماط الفرعية من خلال شكل خلايا الورم وبنيتها وسلوكها. يُعدّ تمييز النمط الفرعي أمرًا بالغ الأهمية لأن بعض الأنواع الفرعية تتصرف بشكل أكثر عدوانية، أو تستجيب للعلاج بشكل مختلف، أو يكون تشخيصها أفضل أو أسوأ من غيرها.
تتناول الأقسام التالية الأنواع الفرعية النسيجية لسرطان القناة الغدية في البنكرياس.
سرطان الغدد الحرشفية وسرطان الخلايا الحرشفية
يحتوي سرطان الغدد الحرشفية على نوعين من الخلايا السرطانية: الخلايا الغدية المكونة للغدد (السرطان الغدي) والخلايا الحرشفية. لا توجد الخلايا الحرشفية عادةً في البنكرياس، وعادةً ما ترتبط بأسطح الجلد والأغشية المخاطية. في هذا النوع الفرعي، يتكون ما لا يقل عن 30% من الورم من الخلايا الحرشفية. تظهر هذه الخلايا تحت المجهر كصفائح من الخلايا متعددة الأضلاع ذات حواف حادة وسيتوبلازم وردي كثيف.
يميل هذا النوع الفرعي إلى أن يكون أكثر عدوانية من سرطان الغدد القنوية النموذجي. سرطان الخلايا الحرشفية يعتبر سرطان البنكرياس نادرًا للغاية، وفي مثل هذه الحالات، يجب على الأطباء التأكد من أن السرطان لم ينتشر من جزء آخر من الجسم مثل الرئتين.
سرطان الغرواني
سرطان الغرواني هو نوع فرعي نادر تطفو فيه خلايا الورم في تجمعات كبيرة من المخاط، وهو مادة سميكة هلامية تُنتجها عادةً بعض أنواع الخلايا. تحت المجهر، تبدو خلايا السرطان معلقة في المخاط بدلاً من أن تُشكل غددًا متماسكة.
غالبًا ما يرتبط هذا النوع الفرعي بورم غير جراحي يُسمى الورم الحليمي المخاطي داخل القناة المعوية (IPMN). يتميز سرطان الغروانية بتوقعات أفضل من معظم سرطانات البنكرياس الأخرى، مع معدل بقاء أعلى لمدة خمس سنوات.
سرطان الكبد
سرطان الكبد هو نوع نادر جدًا من سرطان البنكرياس، يشبه سرطان الكبد تحت المجهر. خلايا الورم كبيرة الحجم، ولها سيتوبلازم وردي اللون يشبه خلايا الكبد. وقد تُنتج أيضًا بروتينًا يُسمى ألفا-فيتوبروتين (AFP)، والذي يُنتجه الكبد عادةً.
لأن العديد من الأورام تُحاكي سرطان الكبد، فإن هذا التشخيص يتطلب فحوصات خاصة لتأكيد أصله. في بعض الحالات، قد تتطور سرطانات الكبد بشكل عدواني، ولكن المعلومات المتاحة حول التشخيص محدودة نظرًا لندرتها.
سرطان النخاع
سرطان النخاع هو نوع فرعي نادر يتكون من صفائح أو أعشاش من متباينة بشكل سيئ خلايا ورمية تنمو بنمط دفع بدلًا من التسلل. غالبًا ما تتميز هذه الأورام باستجابة مناعية قوية، حيث توجد العديد من الخلايا المناعية داخل الورم وحوله.
على الرغم من أن سرطانات النخاع تتميز بضعف التمايز، إلا أن بعض مرضى هذا النوع من الأورام قد يحصلون على نتائج أفضل من المتوقع. غالبًا ما يرتبط هذا النوع الفرعي بعدم استقرار الميكروساتلايت، وقد يستجيب للعلاج المناعي.
سرطان الحليمات الدقيقة الغازي
في هذا النوع الفرعي، يتكون نصف الورم على الأقل من مجموعات صغيرة من الخلايا السرطانية محاطة بمساحات فارغة. تبدو هذه المجموعات من الخلايا وكأنها تطفو داخل الأنسجة، مشكلةً ما يصفه علماء الأمراض بـ حليمي دقيق .
تميل سرطانات الحليمات الدقيقة إلى أن تكون أكثر عدوانية وقد تنتشر بسهولة أكبر الغدد الليمفاوية ومناطق أخرى من الجسم.
سرطان الخلايا الخاتمية
سرطان الخلايا الخاتمية هو شكل نادر للغاية من سرطان البنكرياس. يتكون الورم من خلايا فردية أو مجموعات صغيرة من الخلايا التي تحتوي على الميوسين، مما يدفع النواة إلى الجانب، مما يعطي الخلية "خاتم الخاتم"المظهر تحت المجهر."
غالبًا ما يرتبط هذا النوع من السرطان بأورام من أجزاء أخرى من الجسم، مثل المعدة أو الثدي، لذا يجب على الأطباء استبعاد احتمالية انتشاره إلى أجزاء أخرى من الجسم بعناية قبل تشخيصه كورم بنكرياسي أولي. تميل سرطانات الخلايا الختمية إلى السلوك العدواني.
سرطان غير متمايز
السرطان غير المتمايز هو سرطان شديد الخطورة، حيث لا تشبه خلايا الورم الخلايا الطبيعية، ولا تُظهر نمطًا واضحًا للتمايز. غالبًا ما تنمو هذه الأورام كصفائح خلوية صلبة، وقد تفتقر إلى تكوين الغدد.
هناك عدة أنماط من السرطان غير المتمايز:
-
يحتوي السرطان اللانمطي غير المتمايز على خلايا شاذة للغاية ذات نوى كبيرة وغير منتظمة، وأحيانًا خلايا عملاقة غريبة الشكل. غالبًا ما تكون هذه الأورام شديدة العدوانية.
-
يشمل سرطان الساركوما غير المتمايز خلايا ورمية مغزلية الشكل قد تشبه العظام أو الغضاريف. في بعض الحالات، يحتوي الورم على خلايا رابدوية، وهي كبيرة الحجم وضعيفة التماسك.
-
الساركوما السرطانية ورم نادر يحتوي على مكونات غدية (ظهارية) ومغزلية (ساركوماتويدية). يجب أن يشكل كل مكون 30% على الأقل من الورم.
عادةً ما يكون تشخيص السرطانات غير المتمايزة سيئًا وتميل إلى النمو والانتشار بسرعة.
سرطان غير متمايز مع خلايا عملاقة تشبه الخلايا الناقضة للعظم
يحتوي هذا الورم النادر على ثلاثة أنواع من الخلايا. النوع الأول هو خلايا عملاقة غير سرطانية شبيهة بالخلايا الناقضة للعظم، وهي خلايا كبيرة ذات نوى متعددة. النوع الثاني هو الخلايا النسيجية وحيدة النواة، وهي جزء من الجهاز المناعي للجسم. أما النوع الثالث فهو الخلايا السرطانية، والتي قد تختلف في الشكل والحجم.
على الرغم من وجود خلايا سرطانية شاذة للغاية، فإن بعض الأورام في هذه المجموعة تتصرف بشكل أقل عدوانية، ويعيش العديد من المرضى لسنوات بعد التشخيص. يرتبط هذا النوع الفرعي بسرطان الغدد القنوية النموذجي، ويشترك في بعض التغيرات الجينية نفسها.
امتداد الورم ومرحلة الورم المرضية (pT)
يبدأ سرطان الغدد القنوية في البنكرياس في قنوات صغيرة تُسمى القنوات، تحمل الإنزيمات الهضمية التي ينتجها البنكرياس. توجد هذه القنوات داخل البنكرياس، وتبطنها طبقة رقيقة من الخلايا الظهارية المتخصصة. مع نمو الورم، قد يتجاوز القنوات ويغزو طبقات أعمق من البنكرياس والأنسجة المجاورة، بما في ذلك الأعصاب والأوعية الدموية والدهون والأعضاء المحيطة به.
يُعد مدى نمو الورم، وخاصةً مدى انتشاره داخل البنكرياس وخارجه، أحد أهم العوامل في فهم مدى تقدم السرطان والتنبؤ بنتائج العلاج. تُستخدم هذه المعلومات لتحديد المرحلة المرضية للورم، والتي غالبًا ما تُختصر بـ pT.
يحدد أخصائيو علم الأمراض مرحلة pT بقياس حجم الورم الغازي وتحديد أي انتشار له إلى بنى حيوية مجاورة، مثل الشرايين الرئيسية. تُعد مرحلة pT جزءًا من نظام تصنيف TNM المُستخدم لوصف السرطان. عادةً ما تعني مرحلة pT الأعلى أن الورم أكبر حجمًا أو أنه قد غزا بنى مهمة مجاورة، وقد يصعب إزالته جراحيًا.
فيما يلي شرح مبسط لمراحل pT المستخدمة في سرطان القناة الغدية في البنكرياس:
- pT0:لم يتم العثور على أي ورم.
-
pTis (سرطان موضعي):تتواجد خلايا الورم فقط داخل القنوات، ولم تغزو أنسجة البنكرياس المحيطة. ويشمل ذلك تغيرات سرطانية عالية الدرجة، مثل PanIN-3، والأورام الحليمية المخاطية داخل القنوات المصحوبة بخلل تنسج عالي الدرجة، وآفات مماثلة.
-
pT1:الورم حجمه 2 سم أو أصغر.
-
pT1a:الورم حجمه 0.5 سم أو أصغر.
-
pT1b:يبلغ حجم الورم ما بين 0.5 سم إلى 1 سم.
-
pT1c:الورم حجمه من 1 إلى 2 سم.
-
-
pT2:الورم أكبر من 2 سم ولكن ليس أكثر من 4 سم.
-
pT3:الورم أكبر من 4 سم لكنه لم ينمو إلى الشرايين الرئيسية القريبة.
-
pT4:نما الورم إلى شريان رئيسي واحد أو أكثر، مثل المحور البطني، أو الشريان المساريقي العلوي، أو الشريان الكبدي المشترك. لا يهم حجم الورم في هذه المرحلة.
يُعد فهم مرحلة ما قبل الورم (pT) أمرًا بالغ الأهمية، إذ يُساعد في توجيه قرارات العلاج، ويُوفر معلومات حول التشخيص. غالبًا ما يكون من الأسهل استئصال الأورام في مراحلها الأولى تمامًا، وترتبط بنتائج أفضل. أما الأورام في مراحلها المتقدمة، فقد تتطلب علاجًا أكثر تعقيدًا، وتكون أكثر عرضة للتكرار أو الانتشار إلى أجزاء أخرى من الجسم.
هوامش
هوامش تشير إلى حواف أو حدود الأنسجة التي تُقطع أثناء الجراحة لإزالة الورم. بعد الجراحة، يفحص أخصائي علم الأمراض هذه الحواف بعناية تحت المجهر للتحقق من وجود أي خلايا سرطانية على حافة النسيج المُزال.
-
A هامش سلبي (وتُسمى أيضًا هامشًا واضحًا) يعني عدم وجود خلايا سرطانية ظاهرة على الحافة. هذا يشير إلى أنه من المرجح استئصال الورم تمامًا.
-
A هامش إيجابي يعني ذلك أن الخلايا السرطانية تُرى مباشرةً على حافة النسيج. وهذا يثير القلق من احتمال ترك بعض الخلايا السرطانية.
حالة الهامش مهمة لأنها تساعد الأطباء على تحديد ما إذا كانت هناك حاجة إلى علاج إضافي. على سبيل المثال، إذا كان الهامش إيجابيًا، فقد يُوصى بإجراء جراحة إضافية أو علاج إشعاعي لتقليل خطر عودة السرطان.
في جراحة البنكرياس، يتم عادة تقييم عدة هوامش محددة:
-
هامش قطع البنكرياسهذه هي حافة البنكرياس التي قُطعت لإزالة الورم. غالبًا ما تكون الحافة الأهم عندما يكون الورم في رأس أو عنق البنكرياس.
-
حافة القناة الصفراوية المشتركةهذه هي حافة القناة الصفراوية التي أُزيلت مع البنكرياس. تحمل القناة الصفراوية الصفراء من الكبد إلى الأمعاء، وتمر عبر رأس البنكرياس أو بالقرب منه.
-
الحافة المعقوفة (خلف الصفاق):هذه هي الحافة النسيجية العميقة الواقعة خلف البنكرياس. وهي قريبة من الأوعية الدموية والأعصاب المهمة، وتُفحص كثيرًا للكشف عن وجود ورم.
-
حواف الاثني عشر والمعدة:إذا تم استئصال جزء من الأمعاء الدقيقة (الاثني عشر) أو المعدة أثناء الجراحة، يتم فحص الحواف المقطوعة لهذه الأعضاء أيضًا.
قد يتضمن التقرير أيضًا المسافة بين الورم وأقرب هامش. حتى لو لم يكن الهامش إيجابيًا، فإن الهامش القريب جدًا (مثل أقل من 1 مم) قد يزيد من خطر تكرار المرض.
إن معرفة ما إذا كانت الهوامش سلبية أو إيجابية أمر ضروري للتخطيط للخطوات التالية في الرعاية وتقدير احتمالية عودة السرطان.
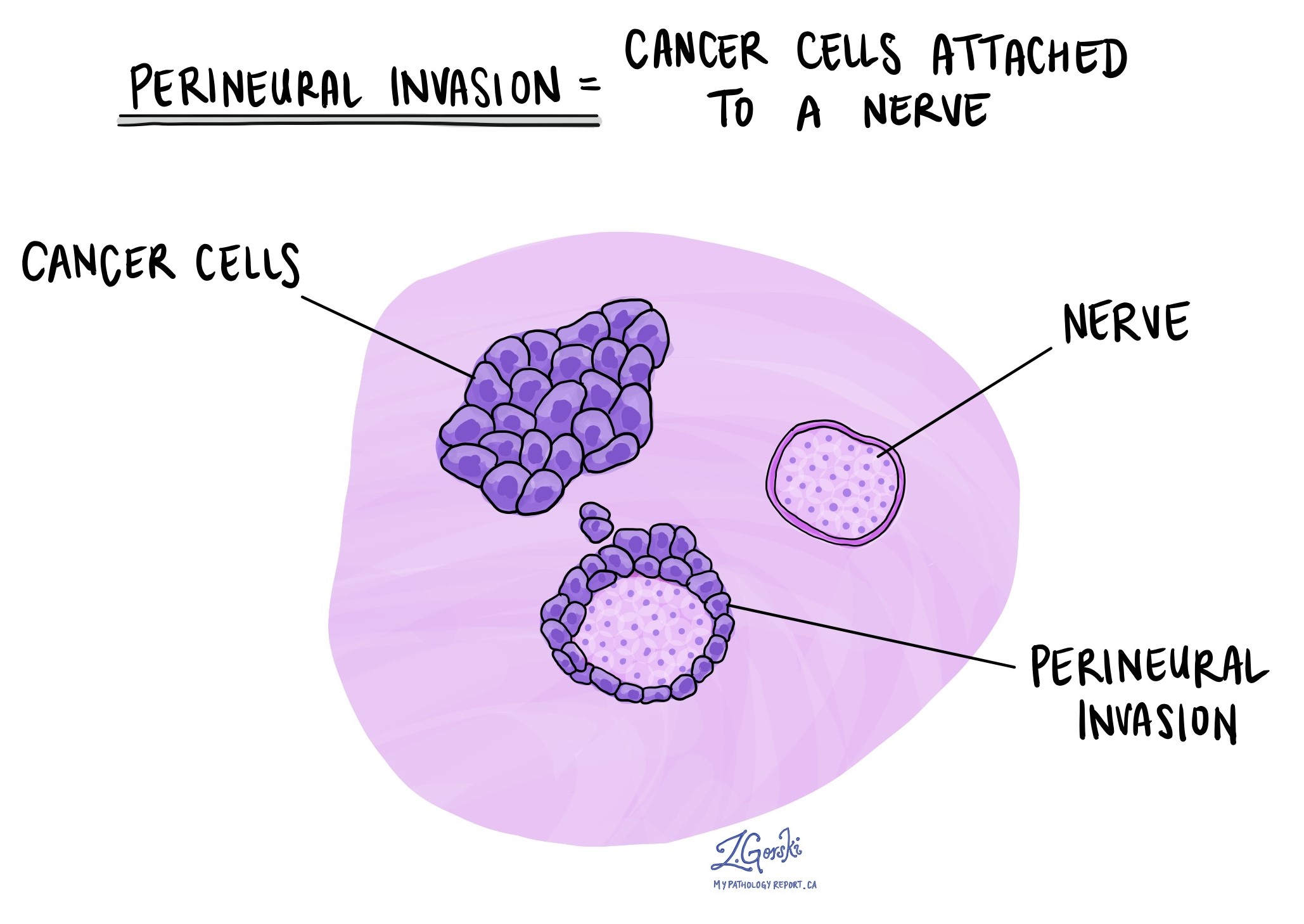
غزو العجان
غزو العجان (PNI) يعني نمو خلايا سرطانية على طول الأعصاب أو حولها. هذه سمة عدوانية قد تزيد من احتمالية انتشار السرطان. في حال وجودها، سيتم وصفها في تقريرك المرضي.
غزو الأوعية الدموية اللمفاوية
غزو الأوعية اللمفاوية (LVI) يعني ذلك أن الخلايا السرطانية تُرى داخل الأوعية الدموية أو الأوعية اللمفاوية القريبة من الورم. وهذا يزيد من خطر انتشار السرطان إلى العقد اللمفاوية أو أجزاء أخرى من الجسم.

العقد الليمفاوية
الغدد الليمفاوية أعضاء صغيرة تشبه حبة الفاصولياء، وهي جزء من الجهاز المناعي. تساعد على تصفية المواد الضارة من الجسم، وغالبًا ما تكون أول مكان ينتشر فيه السرطان من البنكرياس. أثناء جراحة سرطان الغدد القنوية في البنكرياس، عادةً ما تُزال الغدد الليمفاوية المجاورة ويفحصها أخصائي علم الأمراض تحت المجهر.
في تقرير علم الأمراض الخاص بك، قد يتم وصف الغدد الليمفاوية بعدة طرق:
-
العدد الإجمالي للغدد الليمفاوية التي تم فحصها.
-
عدد العقد التي تحتوي على السرطان (وتسمى أيضًا العقد الإيجابية).
-
موقع الغدد الليمفاوية المصابة.
-
حجم أكبر منطقة للسرطان في العقد.
-
ما إذا كان السرطان قد انتشر خارج العقدة الليمفاوية إلى الأنسجة المحيطة بها.
يتم استخدام هذه المعلومات لتحديد المرحلة المرضية للعقدة (pN)، مما يساعد الأطباء على فهم مدى انتشار السرطان ويرشدهم في اتخاذ القرارات بشأن العلاج.
المراحل العقدية المرضية
-
لم يتم تعيين pN:لم يتم تسجيل أو العثور على أي عقد ليمفاوية في الأنسجة التي تمت إزالتها أثناء الجراحة.
-
لم يتم تعيين pN (لا يمكن تحديده):تم إرسال العقد الليمفاوية ولكن لم يكن من الممكن تقييمها بشكل صحيح لأسباب فنية أو معلومات غير كاملة.
-
pN0:لم يتم العثور على أي سرطان في أي من الغدد الليمفاوية التي تم فحصها.
-
pN1:تم العثور على السرطان في واحدة إلى ثلاث عقد ليمفاوية إقليمية.
-
pN2:تم العثور على السرطان في أربع أو أكثر من الغدد الليمفاوية الإقليمية.
يُعدّ عدد العقد الليمفاوية الإيجابية مهمًا لارتباطه الوثيق بالتشخيص. فالأشخاص الذين لديهم عدد أكبر من العقد الليمفاوية المصابة بالسرطان يكونون أكثر عرضة لعودة المرض بعد الجراحة. تُستخدم هذه المعلومات أيضًا لتحديد المرحلة العامة للسرطان وما إذا كان يُنصح بعلاج إضافي، مثل العلاج الكيميائي.
المؤشرات الحيوية لسرطان غدة البنكرياس
المؤشرات الحيوية هي تغيرات قابلة للقياس داخل خلايا الورم - عادةً ما تشمل جينات أو بروتينات محددة - تساعد الأطباء على فهم سلوك السرطان وتحديد العلاجات الأكثر فعالية. يُعد اختبار المؤشرات الحيوية مهمًا بشكل خاص في سرطان القناة البنكرياسية الغدي، لأن بعض الأورام تحمل تغيرات جينية موروثة أو مكتسبة تؤثر على التشخيص، وتُوجه استخدام العلاج المُوجه، ويمكنها تحديد أفراد العائلة الذين قد يكونون أيضًا أكثر عرضة للإصابة بالسرطان. تساعد نتائج المؤشرات الحيوية فريق الرعاية الصحية الخاص بك على اختيار علاجات مثل مثبطات PARP، والعلاج المناعي، أو الأدوية الموجهة لطفرات جينية محددة.
ما هي أنواع المؤشرات الحيوية التي يتم اختبارها في سرطان البنكرياس؟
تُفحص معظم اختبارات المؤشرات الحيوية لسرطان البنكرياس الحمض النووي للورم، بحثًا عن طفرات وراثية أو خاصة بالورم تؤثر على مسارات النمو أو أنظمة إصلاح الحمض النووي. قد تكشف هذه الاختبارات عن طفرات في جينات مثل BRCA1 وBRCA2 وPALB2 وKRAS، أو تحدد اندماجات جينية مثل RET. قد تُقيّم اختبارات إضافية الجينات المعنية بإصلاح عدم التطابق (MMR)، بما في ذلك MLH1 وMSH2 وMSH6 وPMS2، لتحديد مدى فائدة العلاج المناعي. يُجرى الاختبار عادةً باستخدام تقنية تسلسل الجيل التالي (NGS) على خزعة أو عينة جراحية.
براف
BRAF هو جينٌ يُشارك في مسار نموٍّ يُساعد على تنظيم انقسام الخلايا. بعض الطفرات، وخاصةً طفرة V600E، يُمكن أن تُسرّع نمو الخلايا السرطانية. يُعدّ BRAF مهمًا لأن الأورام التي تحتوي على طفرات فيه قد تستجيب للعلاجات المُستهدفة له، والتي تُعيق البروتين غير الطبيعي وتُبطئ نمو الورم.
يقوم علماء الأمراض باختبار طفرات BRAF عن طريق فحص الحمض النووي للورم باستخدام تسلسل الجيل التالي أو الأساليب القائمة على تفاعل البوليميراز المتسلسل والتي تكشف عن التغيرات الجينية المحددة.
سيتم وصف الورم لديك بأنه إيجابي لـ BRAF إذا تم اكتشاف طفرة أو سلبي لـ BRAF إذا لم يتم العثور على أي طفرة.
BRCA1 و BRCA2
جينات BRCA1 وBRCA2 مسؤولة عن إصلاح الحمض النووي التالف. قد تكون الطفرات في هذه الجينات موروثة أو تنشأ فقط في الورم. تُعد هذه المؤشرات الحيوية مهمة لأن المرضى الذين يعانون من طفرات BRCA1 أو BRCA2 قد يستفيدون من مثبطات PARP، وهو نوع من العلاج الموجه يستغل ضعف قدرة الورم على إصلاح الحمض النووي. كما أن تحديد هذه الطفرات له آثار على أفراد العائلة الذين قد يحملون نفس الطفرة الموروثة.
يتم إجراء الاختبار باستخدام تسلسل الجيل التالي لتحليل كل من المادة الوراثية الموروثة (اختبار الخلايا الجرثومية) والتغيرات في الحمض النووي الخاصة بالورم (الاختبار الجسدي).
ستوضح النتائج ما إذا كان الورم إيجابيًا لجين BRCA1 أو إيجابيًا لجين BRCA2 في حال وجود طفرة، أو سلبيًا لجين BRCA1 أو سلبيًا لجين BRCA2 في حال عدم وجود أي طفرات. وقد تحدد التقارير أيضًا ما إذا كانت الطفرة موروثة.
EGFR
EGFR هو بروتين موجود على سطح الخلايا، يُعزز النمو والانقسام. على الرغم من أن EGFR يُعدّ مؤشرًا حيويًا مهمًا في بعض أنواع السرطان، إلا أن طفرات EGFR نادرة في سرطان البنكرياس. ومع ذلك، فإن تحديد أي تغيير في EGFR قد يُساعد في توجيه العلاج في حالات نادرة.
يتم إجراء اختبار EGFR باستخدام تسلسل الجيل التالي للبحث عن الطفرات في الحمض النووي للورم.
سيتم وصف الورم بأنه إيجابي لـ EGFR إذا كانت هناك طفرة موجودة أو سلبي لـ EGFR إذا لم يتم العثور على أي طفرة.
ERBB2 (HER2)
ERBB2، المعروف أيضًا باسم HER2، هو جين يُعزز نمو الخلايا. في عدد قليل من سرطانات البنكرياس، قد يكون HER2 مفرط النشاط. يُعد HER2 مهمًا لأن الأورام التي يُفرط فيها التعبير عن HER2 أو يُضخّم قد تستجيب للعلاجات المُستهدفة له.
يتم اختبار HER2 باستخدام المناعة الكيميائية لتقييم التعبير البروتيني، وعند الحاجة، اختبارات إضافية مثل FISH أو تسلسل الجيل التالي لتحديد تضخيم الجينات.
تُصنَّف مستويات بروتين HER2 على أنها 0، 1+، 2+، أو 3+. تُشير الدرجات 0 أو 1+ إلى سلبية HER2، و3+ إلى إيجابية HER2، و2+ إلى عدم اليقين وتتطلب اختبارات إضافية لتأكيد تضخيم الجينات.
KRAS
يُعد جين KRAS من أكثر الجينات طفرةً في سرطان البنكرياس. تُحفّز الطفرات في جين KRAS نمو الورم من خلال الحفاظ على إشارات النمو مُفعّلة باستمرار. يُعدّ هذا المؤشر الحيوي مهمًا لأن طفرات KRAS تؤثر بشدة على سلوك الورم، وقد تُحدد مدى أهلية المريض لعلاجات جديدة مُوجّهة لأنواع فرعية مُحددة من KRAS.
يتم إجراء اختبار KRAS باستخدام تسلسل الجيل التالي لتقييم مناطق معينة من الجين حيث تحدث الطفرات بشكل شائع.
سيتم وصف الورم لديك بأنه إيجابي لـ KRAS إذا تم العثور على طفرة وسلبي لـ KRAS إذا لم يتم اكتشاف أي طفرة.
بروتينات إصلاح عدم التطابق (MLH1، MSH2، MSH6، PMS2)
تساعد بروتينات إصلاح عدم التطابق (MMR) على تصحيح الأخطاء الطفيفة في الحمض النووي (DNA). عند فقدان أيٍّ من هذه البروتينات، يُصاب الورم بنقص إصلاح عدم التطابق (dMMR)، وقد يستجيب للعلاج المناعي. قد يُشير نقص MMR أيضًا إلى الإصابة بمتلازمة لينش، وهي حالة وراثية تزيد من خطر الإصابة بأنواع عديدة من السرطان.
يستخدم علماء الأمراض المناعة الكيميائية لتحديد ما إذا كان كل بروتين MMR موجودًا في نوى الخلايا السرطانية.
سيتم وصف الورم بأنه كفء في MMR (pMMR) إذا كانت جميع البروتينات موجودة أو ناقص MMR (dMMR) إذا كان أي منها غائبًا.
PALB2
PALB2 هو جين يتعاون بشكل وثيق مع جينات BRCA1 وBRCA2 في إصلاح الحمض النووي. قد تكون طفرات PALB2 وراثية أو تحدث فقط في الورم. يُعد هذا المؤشر الحيوي مهمًا لأن الأورام التي تحتوي على طفرة PALB2 قد تستجيب لمثبطات PARP، على غرار السرطانات المرتبطة بجين BRCA.
يتم إجراء الاختبار باستخدام تسلسل الجيل التالي لتحديد الطفرات في جين PALB2.
سيتم وصف الورم لديك بأنه إيجابي لـ PALB2 إذا تم اكتشاف طفرة وسلبي لـ PALB2 إذا لم يتم العثور على أي طفرة.
RAD51C وRAD51D
RAD51C وRAD51D هما جينان مسؤولان عن إصلاح الحمض النووي التالف. قد تشير الطفرات في هذين الجينين إلى حساسية الورم لمثبطات PARP، مما يجعلهما مؤشرين حيويين مهمين في تخطيط العلاج.
يتم تحليل هذه الجينات باستخدام تسلسل الجيل التالي، الذي يقيم الحمض النووي بحثًا عن طفرات محددة.
سيتم وصف الورم بأنه إيجابي لـ RAD51C أو إيجابي لـ RAD51D إذا كانت الطفرات موجودة وسلبي إذا لم يتم اكتشاف أي طفرات.
اندماجات RET
RET هو جين قادر على الاندماج مع جين آخر، مما يُنتج بروتين اندماج غير طبيعي يُعزز نمو الورم. على الرغم من ندرته، يُعد اندماج RET مهمًا لأن الأورام التي يُصاب بها هذا التغيير قد تستجيب للعلاجات المُستهدفة لـ RET.
يتم عادةً اكتشاف اندماجات RET باستخدام تسلسل الجيل التالي أو FISH لتحديد إعادة ترتيب الجينات.
سيتم وصف الورم بأنه إيجابي لـ RET إذا تم اكتشاف اندماج جيني، وسلبي لـ RET إذا لم يتم العثور على أي اندماج.
ما هو تشخيص سرطان القناة الغدية في البنكرياس؟
سرطان الغدد القنوية هو سرطان عدواني ذو احتمالية عالية للانتشار أو العودة بعد العلاج. يعتمد التشخيص على مرحلة الورم عند التشخيص، وما إذا كان قد أُزيل بالكامل جراحيًا، وما إذا كان قد انتشر إلى العقد اللمفاوية أو أعضاء أخرى. معدل البقاء على قيد الحياة لمدة خمس سنوات منخفض، لكن الجراحة مع العلاج الكيميائي قد تُحسّن النتائج لدى بعض المرضى.
أسئلة لطرح طبيبك
-
ما هو حجم ومرحلة الورم؟
-
هل هناك أي إصابة في الغدد الليمفاوية؟
-
هل كانت الهوامش واضحة؟
-
هل كان هناك دليل على وجود غزو عصبي أو لمفي وعائي؟
-
هل هناك أي علاجات إضافية موصى بها؟
-
هل تم إجراء اختبار جزيئي على الورم الخاص بي؟


