توسط Catherine Forse MD FRCPC و Jason Wasserman MD PhD FRCPC
آوریل 23، 2024
آدنوکارسینوم (همچنین به عنوان آدنوکارسینوم مهاجم شناخته می شود) نوعی سرطان مری است. این شایع ترین نوع سرطان مری در کشورهای توسعه یافته است و در مردان شایع تر از زنان است. این نوع سرطان معمولاً در بخشی از مری به نام محل اتصال معده به مری شروع می شود.
این مقاله به شما کمک می کند تا گزارش آسیب شناسی خود را برای آدنوکارسینوم مری بخوانید و درک کنید.
مری
مری یک لوله عضلانی توخالی است که گلو (حلق) را به معده متصل می کند. وظیفه اصلی آن انتقال غذا و مایعات از دهان به معده برای هضم است. وقتی قورت می دهید، دیواره های مری به طور هماهنگ منقبض می شوند – این حرکت که پریستالسیس نامیده می شود، غذا را به سمت پایین هل می دهد. مری همچنین دارای اسفنکترها در هر دو انتها است. این دریچههای عضلانی باز میشوند تا غذا و مایعات به معده بروند و بسته میشوند تا از برگشت محتویات معده به مری و دهان جلوگیری شود.
علائم آدنوکارسینوم در مری چیست؟
شایع ترین علائم آدنوکارسینوم مری دشواری در بلع (به ویژه غذاهای جامد)، درد قفسه سینه، بدتر شدن ریفلاکس اسید و کاهش وزن است.
علت ایجاد آدنوکارسینوم مری چیست؟
آدنوکارسینوم مری معمولاً از وضعیتی به نام ایجاد می شود مری بارت که در اثر برگشت طولانی مدت اسیدهای معده به مری (بیماری ریفلاکس اسید) ایجاد می شود. به همین دلیل، آدنوکارسینوم در مری اغلب پس از چندین سال رفلاکس اسید ایجاد می شود.
هنگامی که قسمت داخلی مری برای مدت طولانی در معرض اسید معده قرار می گیرد سلولهای سنگفرشی که معمولاً داخل مری را می پوشانند، جایگزین می شوند سلولهای غده ای که شبیه سلول های موجود در داخل روده کوچک هستند. این سلولهای رودهای در برابر آسیب اسیدهای قوی که در معده ایجاد میشوند، مقاومتر هستند. تغییر سلول های سنگفرشی به سلول های روده ای نامیده می شود متاپلازی روده.
پزشکان از اصطلاح مری بارت برای توصیف متاپلازی روده در مری استفاده می کنند. این نام به افتخار دکتر نورمن آر. افرادی که سالها مری بارت دارند میتوانند به نوعی رشد غیرطبیعی به نام دیسپلازی مبتلا شوند که با افزایش خطر ابتلا به آدنوکارسینوم همراه است.
در گزارش پاتولوژی خود برای آدنوکارسینوم تهاجمی مری باید به دنبال چه چیزی باشید:
درجه بافت شناسی
آسیب شناسان از اصطلاح متمایز شده برای تقسیم آدنوکارسینوم مری به سه درجه استفاده می کنند - با تمایز خوب، با تمایز متوسط و با تمایز ضعیف. درجه بر اساس درصد ساختارهای گرد تشکیل دهنده تومور به نام است غدد. توموری که هیچ غده ای تشکیل نمی دهد تمایز نیافته نامیده می شود. درجه مهم است زیرا تومورهای ضعیف و تمایز نیافته رفتار تهاجمی تری دارند و احتمال انتشار آنها به سایر نقاط بدن مانند گره های لنفاوی.
آدنوکارسینوم مری به شرح زیر طبقه بندی می شود:
- آدنوکارسینوم خوب تمایز یافته: بیش از 95 درصد تومور از غدد تشکیل شده است. آسیب شناسان نیز این تومورها را درجه 1 توصیف می کنند.
- آدنوکارسینوم با تمایز متوسط: 50 تا 95 درصد تومور از غدد تشکیل شده است. آسیب شناسان نیز این تومورها را درجه 2 توصیف می کنند.
- آدنوکارسینوم با تمایز ضعیف: کمتر از 50 درصد تومور از غدد تشکیل شده است. آسیب شناسان نیز این تومورها را درجه 3 توصیف می کنند.

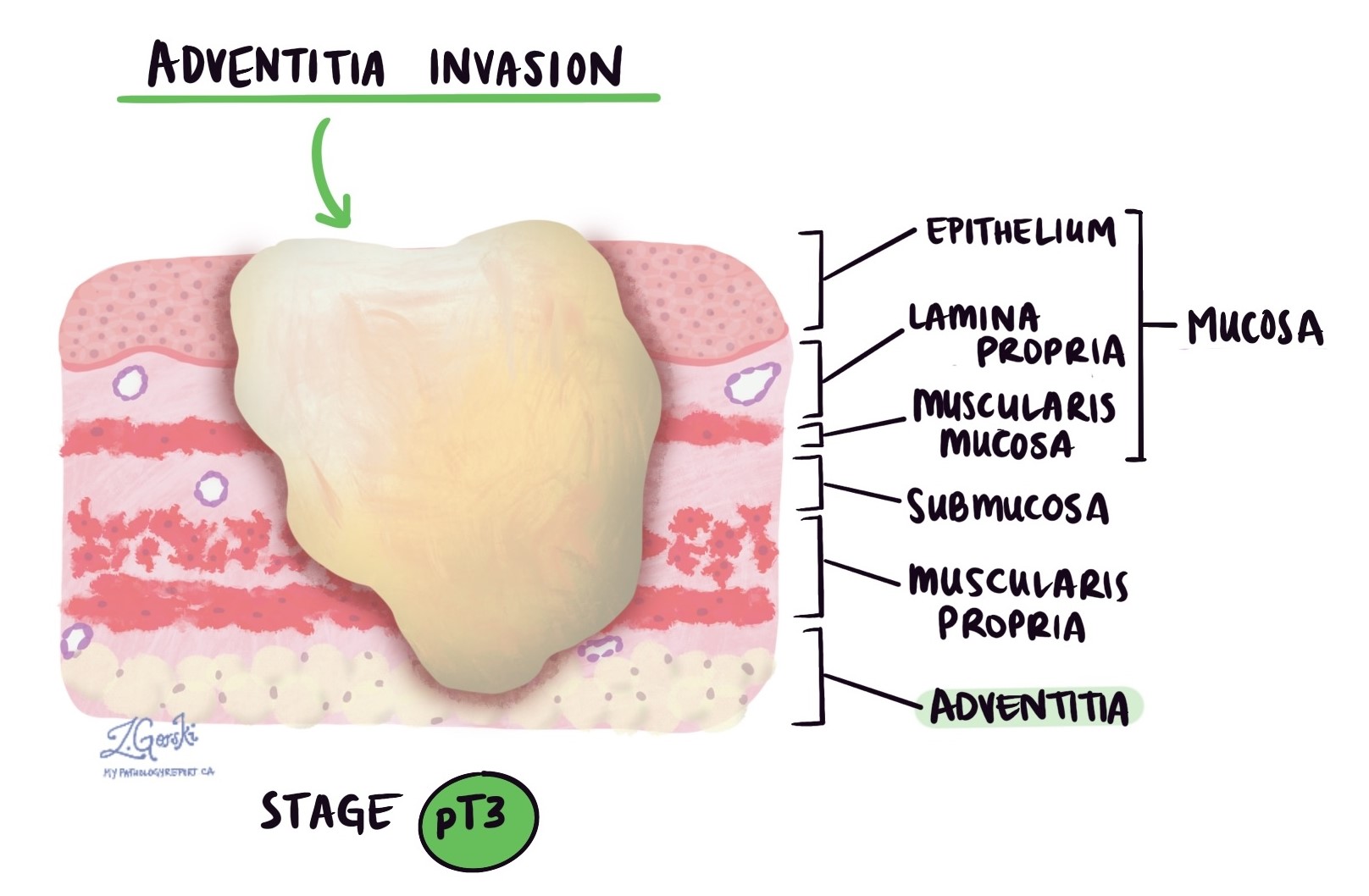
عمق تهاجم و مرحله تومور پاتولوژیک (pT)
آدنوکارسینوما در لایه نازکی از بافت داخل مری به نام مخاط شروع می شود. هنگامی که تومور به طور کامل در داخل مخاط قرار دارد، نامیده می شود داخل مخاطی. بیماران مبتلا به آدنوکارسینوم داخل مخاطی مری در مجموع وضعیت بهتری دارند پیش بینی زیرا سلول های تومور کمتر به سایر قسمت های بدن گسترش می یابند گره های لنفاوی.
در آسیب شناسی، تهاجم گسترش سلول های سرطانی به اندام ها یا بافت های اطراف محل شروع تومور را توصیف می کند. همانطور که تومور در مری رشد می کند، سلول های سرطانی می توانند در لایه های بافت زیر مخاط پخش شوند. در این مرحله، این بیماری به عنوان آدنوکارسینوم مهاجم شناخته می شود.
هنگام بررسی تومور در زیر میکروسکوپ، آسیب شناس شما خواهد دید که سلول های سرطانی تا چه اندازه از مخاط به لایه های زیرین بافت گسترش یافته اند. این عمق یا سطح تهاجم نامیده می شود و مهم است زیرا تومورهایی که به عمق بیشتری حمله می کنند احتمال بیشتری دارد که به سایر قسمت های بدن مانند گره های لنفاوی، کبد یا ریه ها. سطح تهاجم نیز برای تعیین مرحله پاتولوژیک تومور (pT) استفاده می شود. تصاویر زیر ارتباط بین عمق تهاجم و مرحله پاتولوژیک تومور را نشان می دهد.



HER2
HER2 نوعی پروتئین است که به عنوان یک گیرنده عمل می کند و مانند یک سوئیچ عمل می کند که رشد و تقسیم سلولی را کنترل می کند. در برخی از سلول های تومور، HER2 اضافی تولید می شود که منجر به رشد و تقسیم بسیار سریع تر از سلول های طبیعی می شود.
تقریباً یک مورد از هر پنج مورد آدنوکارسینوم مری شامل تولید بیش از حد HER2 است. درمانهای خاص تومورهایی را هدف قرار میدهند که HER2 اضافی تولید میکنند. بنابراین، پاتولوژیست شما ممکن است آزمایش تومور برای HER2 اضافی را برای تعیین بهترین رویکرد درمانی توصیه کند.
رایج ترین روش برای تشخیص HER2 در آدنوکارسینوم، آزمایشی به نام ایمونوهیستوشیمی است. نتایج این آزمایش معمولاً به روش زیر گزارش می شود:
- منفی (0 یا 1) - سلول های تومور HER2 اضافی تولید نمی کنند.
- صریح (2) - سلول های تومور ممکن است HER2 اضافی تولید کنند. در این مورد، پاتولوژیست ها معمولاً یک آزمایش آزمایشگاهی به نام انجام می دهند هیبریداسیون درجا فلورسنت (FISH) برای دیدن اینکه آیا سلول های تومور دارای نسخه های ژنی بیشتری از HER2 هستند یا خیر. این می تواند به تعیین اینکه آیا تومور پروتئین HER2 بیشتری را بیان می کند یا خیر کمک کند.
- مثبت (3) - سلول های تومور قطعاً مقادیر اضافی HER2 تولید می کنند.
عدم تطابق پروتئین های ترمیم کننده
ترمیم عدم تطابق (MMR) سیستمی در درون تمام سلول های سالم و طبیعی است که اشتباهات موجود در ماده ژنتیکی ما (DNA) را برطرف می کند. این سیستم شامل پروتئین های مختلفی است و چهار مورد از رایج ترین آنها MSH2، MSH6، MLH1 و PMS2 هستند.
چهار پروتئین ترمیم ناهماهنگی MSH2، MSH6، MLH1 و PMS2 به صورت جفت برای رفع DNA آسیب دیده کار می کنند. به طور خاص، MSH2 با MSH6 کار می کند و MLH1 با PMS2 کار می کند. اگر یک پروتئین از بین برود، این جفت نمی تواند به طور طبیعی عمل کند و خطر ابتلا به سرطان افزایش می یابد.
رایج ترین روش برای آزمایش عدم تطابق پروتئین های ترمیم کننده این است ایمونوهیستوشیمی. این آزمایش به پاتولوژیست ها اجازه می دهد تا ببینند آیا سلول های تومور هر چهار پروتئین ترمیم ناهماهنگ را تولید می کنند یا خیر. نتایج این آزمایش معمولاً به شرح زیر گزارش می شود:
- نتیجه عادی: بیان پروتئین حفظ شده
- نتیجه غیر طبیعی: از دست دادن بیان پروتئین.
تست ترمیم عدم تطابق بسیار مهم است زیرا می تواند به پیش بینی اینکه درمان های خاص چقدر خوب عمل می کنند کمک می کند. به عنوان مثال، سرطان هایی با از دست دادن بیان پروتئین ترمیم کننده عدم تطابق بیشتر به درمان های ایمونوتراپی مانند مهارکننده های PD-1 یا PD-L1 پاسخ می دهند. این به این دلیل است که تعداد بالای جهشهایی که اغلب در تومورهای کمبود یافت میشوند، میتوانند آنتیژنهای جدیدی تولید کنند که تومور را نسبت به سیستم ایمنی بیشتر قابل مشاهده و آسیبپذیر میکند.
آزمایش ترمیم عدم تطابق نیز برای شناسایی بیمارانی انجام می شود که ممکن است به سندرم لینچ، که به عنوان سرطان روده بزرگ غیر پولیپوز ارثی (HNPCC) نیز شناخته می شود، داشته باشند. سندرم لینچ یک اختلال ژنتیکی است که خطر ابتلا به انواع سرطان از جمله سرطان مری، سرطان روده بزرگ، سرطان آندومتر، سرطان تخمدان و سرطان معده را افزایش می دهد.
PD-L1
PD-L1 (مرگ برنامه ریزی شده- لیگاند 1) پروتئینی است که در سطح سلول های سالم و طبیعی و برخی سلول های سرطانی یافت می شود. این پروتئین یک نقطه بازرسی ایمنی نامیده می شود زیرا فعالیت سلول های ایمنی به نام سلول های T را کاهش می دهد. این سلولها معمولاً سلولهای غیرطبیعی مانند سلولهای سرطانی را شناسایی کرده و از بدن خارج میکنند. سلول های سرطانی که این پروتئین را بیان می کنند با فعال کردن پروتئینی به نام PD-1 روی سلول T از حمله سلول های T فرار می کنند.
پزشکان این پروتئین را آزمایش میکنند تا مشخص کنند کدام بیماران ممکن است از درمانهایی که مسیر PD-1/PD-L1 را هدف قرار میدهند، مانند مهارکنندههای ایست بازرسی، سود ببرند. برای آزمایش بیان PD-L1، آسیب شناسان معمولاً آزمایشی به نام انجام می دهند ایمونوهیستوشیمی روی نمونه بافت تومور در این آزمایش، یک آنتی بادی خاص علیه PD-L1 بر روی بخش بافت اعمال می شود و سپس با استفاده از یک آنتی بادی ثانویه متصل به رنگ شناسایی می شود.
سپس سطح بیان پروتئین بر اساس شدت و درصد سلول های مثبت شمارش و امتیازدهی می شود. برای سرطانهای مری، نتیجه بهعنوان یک امتیاز مثبت ترکیبی (CPS) گزارش میشود که نمره > 1 مثبت در نظر گرفته میشود.
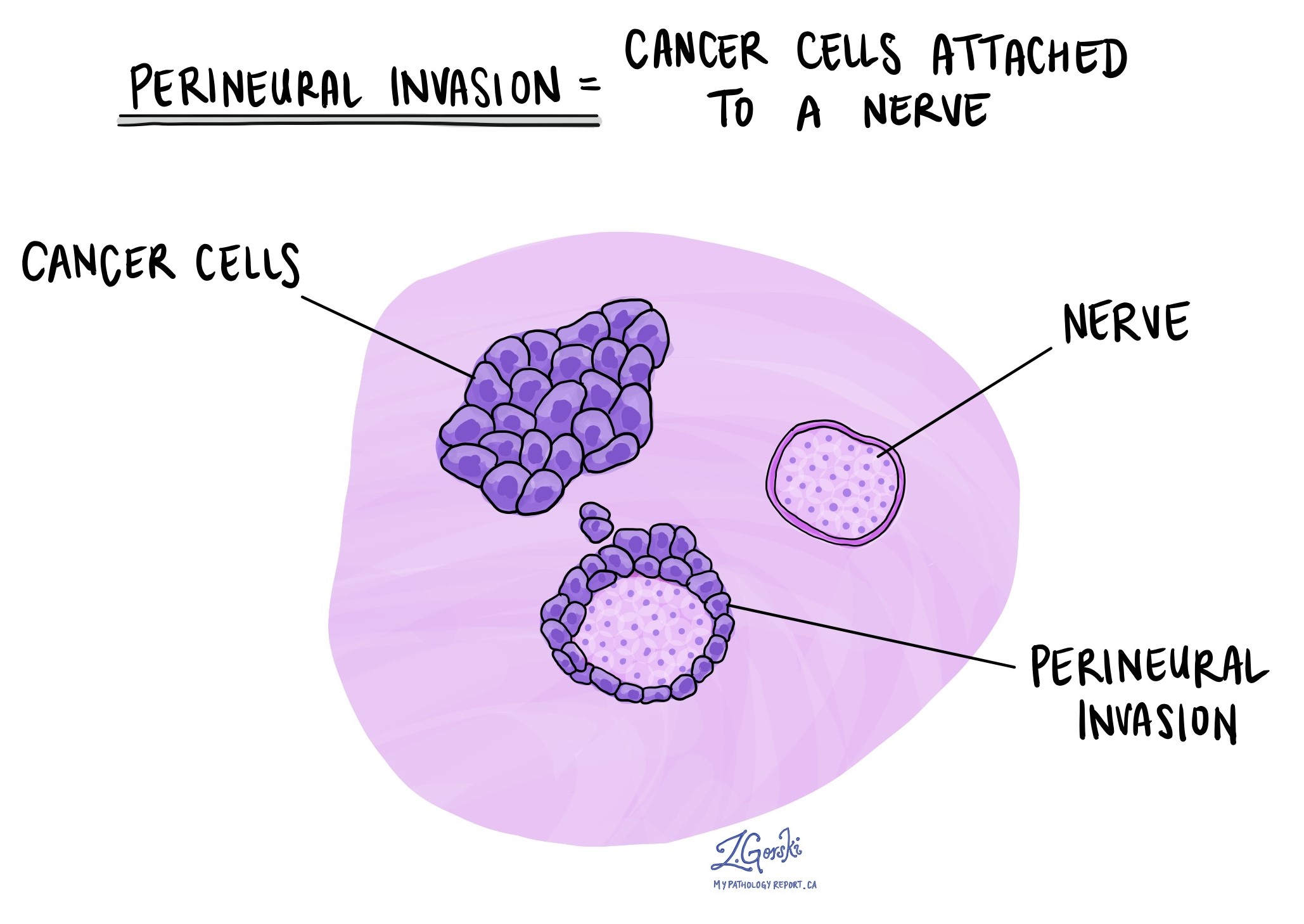
تهاجم پری عصبی
آسیب شناسان از اصطلاح «تهاجم اطراف عصبی» برای توصیف وضعیتی استفاده می کنند که در آن سلول های سرطانی به عصب متصل می شوند یا به آن حمله می کنند. "تهاجم درون عصبی" یک اصطلاح مرتبط است که به طور خاص به سلول های سرطانی موجود در یک عصب اشاره دارد. اعصاب، شبیه سیم های بلند، از گروه هایی از سلول ها به نام نورون ها تشکیل شده اند. این اعصاب که در سراسر بدن وجود دارند، اطلاعاتی مانند دما، فشار و درد را بین بدن و مغز منتقل می کنند. وجود تهاجم پری عصبی مهم است زیرا به سلول های سرطانی اجازه می دهد تا در طول عصب به اندام ها و بافت های مجاور حرکت کنند و خطر عود تومور پس از جراحی را افزایش می دهد.
تهاجم لنفاوی
تهاجم عروق لنفاوی زمانی رخ می دهد که سلول های سرطانی به یک رگ خونی یا رگ لنفاوی حمله کنند. رگ های خونی لوله های نازکی هستند که خون را در سراسر بدن حمل می کنند، در حالی که رگ های لنفاوی به جای خون مایعی به نام لنف را حمل می کنند. این رگ های لنفاوی به اندام های ایمنی کوچکی که در سراسر بدن پراکنده شده اند متصل می شوند که به نام شناخته می شوند گره های لنفاوی. تهاجم عروق لنفاوی مهم است زیرا سلول های سرطانی را قادر می سازد تا از طریق خون یا عروق لنفاوی به سایر قسمت های بدن از جمله غدد لنفاوی یا کبد گسترش یابند.

حاشیه
در پاتولوژی، حاشیه لبه بافتی است که در طی جراحی تومور برداشته می شود. وضعیت حاشیه در گزارش پاتولوژی مهم است زیرا نشان می دهد که آیا کل تومور برداشته شده است یا اینکه مقداری از آن باقی مانده است. این اطلاعات به تعیین نیاز به درمان بیشتر کمک می کند.
آسیب شناسان معمولاً حاشیه ها را پس از یک روش جراحی مانند یک ارزیابی می کنند برداشتن or برداشتن، که کل تومور را از بین می برد. حاشیه ها معمولاً بعد از یک ارزیابی نمی شوند بیوپسیکه تنها بخشی از تومور را از بین می برد.
برای برداشتن آندوسکوپی جایی که فقط یک قطعه کوچک از داخل مری برداشته شده است ، حاشیه شامل موارد زیر است:
- حاشیه مخاطی - این بافتی است که سطح داخلی مری را می پوشاند. نام دیگر این حاشیه، حاشیه جانبی است.
- حاشیه عمیق - این بافت داخل دیواره مری است. در زیر تومور قرار دارد.
برای نمونه های ازوفاژکتومی جایی که یک قسمت کامل از مری برداشته شده است ، حاشیه شامل موارد زیر است:
- حاشیه پروگزیمال - این حاشیه در نزدیکی قسمت فوقانی مری، نزدیکتر به دهان قرار دارد.
- حاشیه دیستال - این حاشیه در نزدیکی قسمت تحتانی مری قرار دارد. حاشیه دیستال می تواند در مری یا معده باشد.
- حاشیه شعاعی - این بافت اطراف خارج مری است.
آسیب شناسان حاشیه ها را برای بررسی وجود سلول های تومور در لبه بریده بافت بررسی می کنند. حاشیه مثبت، جایی که سلول های تومور یافت می شود، نشان می دهد که ممکن است مقداری سرطان در بدن باقی بماند. در مقابل، یک حاشیه منفی، بدون سلول های توموری در لبه، نشان می دهد که تومور به طور کامل برداشته شده است. برخی گزارشها فاصله بین نزدیکترین سلولهای تومور و حاشیه را اندازهگیری میکنند، حتی اگر همه حاشیهها منفی باشند.

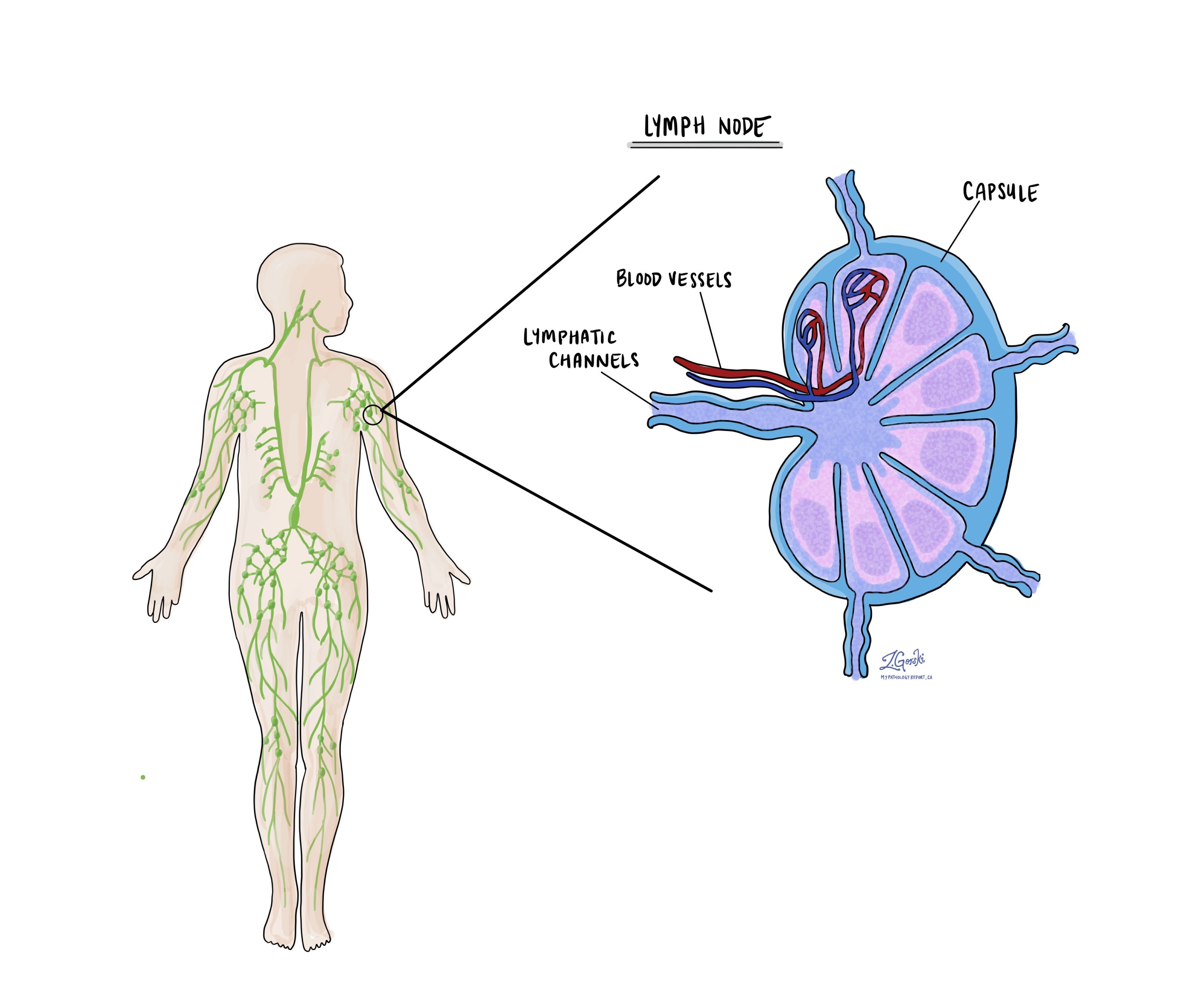
گره های لنفاوی
اندامهای کوچک ایمنی که به نام گره های لنفاوی، در سراسر بدن قرار دارند. سلول های سرطانی می توانند از طریق عروق لنفاوی کوچک از تومور به این غدد لنفاوی بروند. به همین دلیل، پزشکان اغلب غدد لنفاوی را برای جستجوی سلولهای سرطانی برداشته و با میکروسکوپی بررسی میکنند. این فرآیند که در آن سلول های سرطانی از تومور اصلی به قسمت دیگری از بدن مانند یک غدد لنفاوی حرکت می کنند، متاستاز نامیده می شود.
سلول های سرطانی معمولاً ابتدا به غدد لنفاوی نزدیک تومور مهاجرت می کنند، اگرچه گره های لنفاوی دورتر نیز ممکن است تحت تأثیر قرار گیرند. در نتیجه، جراحان معمولاً ابتدا غدد لنفاوی نزدیک به تومور را برمی دارند. اگر غدد لنفاوی دورتر از تومور بزرگ شوند و احتمال وجود سلولهای سرطانی وجود داشته باشد، ممکن است آنها را بردارند.
آسیب شناسان غدد لنفاوی برداشته شده را زیر میکروسکوپ بررسی می کنند و یافته ها در گزارش شما به تفصیل بیان می شود. نتیجه "مثبت" نشان دهنده وجود سلول های سرطانی در غدد لنفاوی است، در حالی که نتیجه "منفی" به این معنی است که هیچ سلول سرطانی یافت نشد. اگر این گزارش سلولهای سرطانی را در یک غدد لنفاوی پیدا کند، ممکن است اندازه بزرگترین خوشه این سلولها را نیز مشخص کند که اغلب به آن «فوکوس» یا «رسوب» میگویند. امتداد خارج جمجمه زمانی رخ می دهد که سلول های تومور به کپسول بیرونی غدد لنفاوی نفوذ کرده و به بافت مجاور گسترش می یابد.
بررسی غدد لنفاوی به دو دلیل مهم است. ابتدا، به تعیین مرحله گرهی پاتولوژیک (pN) کمک می کند. دوم، کشف سلولهای سرطانی در غدد لنفاوی نشاندهنده افزایش خطر یافتن سلولهای سرطانی در سایر قسمتهای بدن در آینده است. این اطلاعات پزشک شما را راهنمایی می کند تا تصمیم بگیرد که آیا به درمان های اضافی مانند شیمی درمانی، پرتودرمانی یا ایمونوتراپی نیاز دارید یا خیر.
مرحله گرهی پاتولوژیک (pN) برای آدنوکارسینوم مری:
- N0 - در هیچ یک از غدد لنفاوی بررسی شده سلول توموری دیده نمی شود.
- N1 – سلول های تومور در یک یا دو غدد لنفاوی دیده می شوند.
- N2 - سلول های تومور در سه تا شش غدد لنفاوی دیده می شوند.
- N3 - سلول های توموری در بیش از شش غدد لنفاوی دیده می شوند.
- NX - هیچ غدد لنفاوی برای معاینه به آسیب شناس ارسال نشد.
اثر درمانی
اگر قبل از برداشتن تومور تحت درمان سرطان (شیمیدرمانی یا پرتودرمانی یا هر دو) قرار گرفتهاید، پاتولوژیست ناحیهای از بافتی را که قبلاً تومور در آن شناسایی شده بود، به دقت بررسی میکند تا ببیند آیا سلولهای سرطانی هنوز زنده هستند (قابل زنده بودن). متداولترین سیستم مورد استفاده، اثر درمانی را در مقیاس 0 تا 3 توصیف میکند، با 0 بدون سلولهای سرطانی زنده (همه سلولهای سرطانی مرده) و 3 سرطان باقیمانده گسترده و بدون پسرفت ظاهری تومور (همه یا بیشتر موارد). سلول های سرطانی زنده هستند).
درباره این مقاله
پزشکان این مقاله را برای کمک به خواندن و درک گزارش آسیب شناسی خود نوشتند. تماس با ما با هر گونه سوال در مورد این مقاله یا گزارش آسیب شناسی شما. خواندن این مقاله برای معرفی کلی تر بخش های گزارش پاتولوژی معمولی.


