מאת ג'ייסון וסרמן MD PhD FRCPC
אפריל 18, 2022
מהי אדנוקרצינומה רירית של המעי הגס?
אדנוקרצינומה רירית היא סוג של סרטן המעי הגס. על מנת לבצע אבחנה זו, לפחות 50% מהגידול חייב להיות מורכב מחוץ תאי מוקין. אדנוקרצינומה רירית מהווה כ-10 עד 20% מכלל מקרי סרטן המעי הגס במבוגרים. בהשוואה לסוגים אחרים של סרטן המעי הגס, אדנוקרצינומה רירית נוטה יותר להחזיק שינויים בגנים הקשורים ל- תיקון אי התאמה (MMR) מערכת. שינויים אלו קשורים לסיכון מוגבר לפתח סרטן.
כיצד מאבחנים פתולוגים של אדנוקרצינומה רירית?
האבחנה של אדנוקרצינומה רירית של המעי הגס נעשית בדרך כלל לאחר הסרת דגימת רקמה קטנה במהלך בדיקה הנקראת קולונוסקופיה. ההליך המשמש להסרת הרקמה עשוי להיקרא א ביופסיה או פוליפקטומיה. לאחר מכן נשלחת דגימת הרקמה לפתולוג לבדיקה במיקרוסקופ.
לאחר הסרת הגידול כולו הוא יישלח לפתולוג שיחפש מאפיינים נוספים כגון הגידול ציון, עומק של פלישה, פלישה פרינוראלית, פלישה לימפה וכלי דם, ניצני גידול ותאי סרטן ב בלוטות לימפה או רקמות מסביב. בדיקות שצריך לחפש תיקון אי התאמה (MMR) ניתן לבצע גם חלבונים. תכונות אלה מוסברות בפירוט רב יותר בסעיפים להלן.
איך נראית אדנוקרצינומה רירית מתחת למיקרוסקופ?
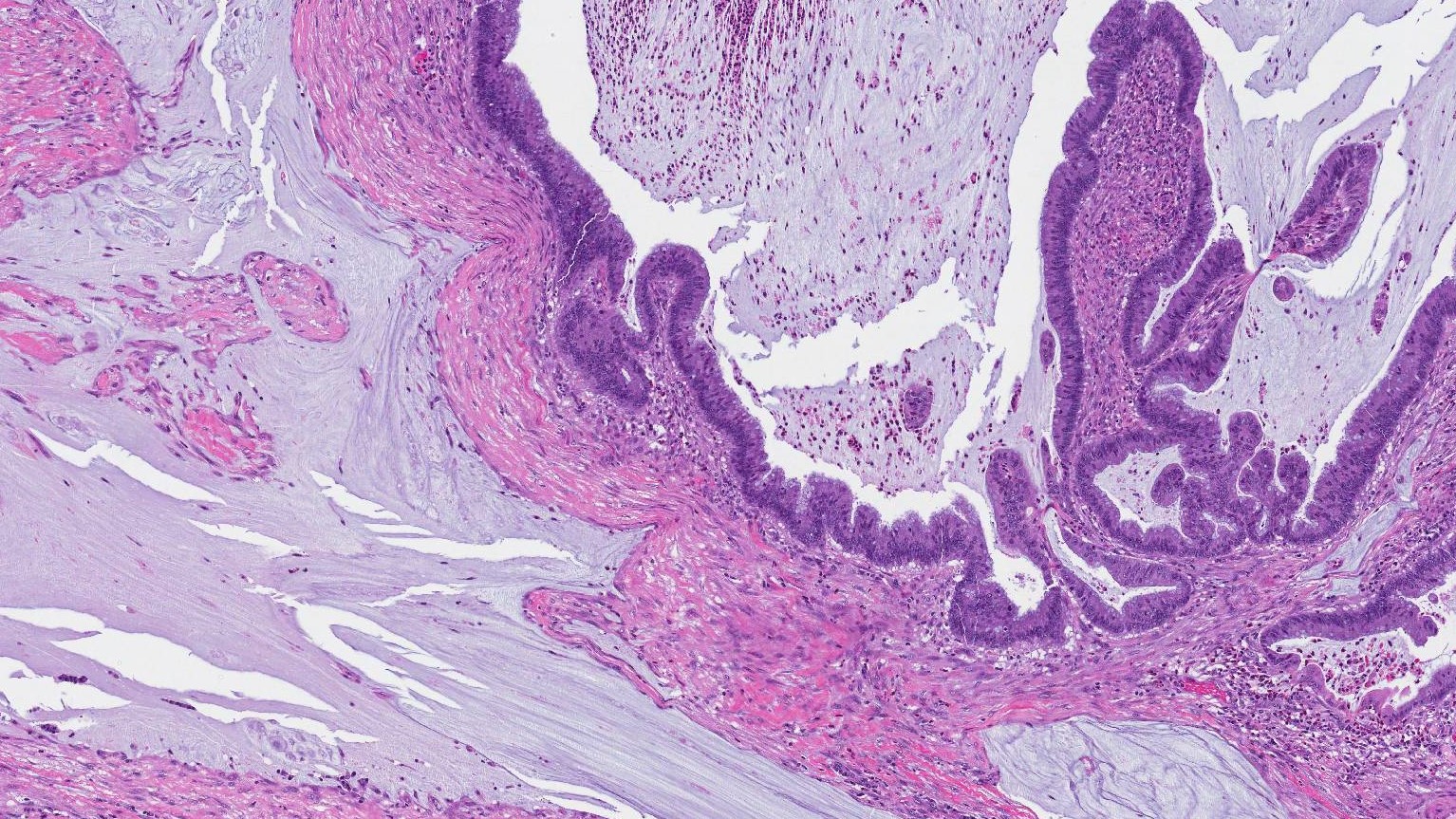
כאשר נבדקים במיקרוסקופ, אדנוקרצינומה רירית מורכבת מקבוצות של תאי גידול המוקפים בחוץ-תאי מוקין. המוצין נקרא חוץ תאי מכיוון שהוא נמצא מחוץ לתאי הגידול. פתולוגים משתמשים לעתים קרובות במונח 'בריכות' כדי לתאר אזורים גדולים של מוצין חוץ תאי. קבוצות תאי הגידול עשויות להיות מסודרות במבנים עגולים הנקראים בלוטות (שעשויות להיראות דומות לבלוטות הרגילות במעי הגס) או שהן עשויות להיות מסודרות בקנים או סדינים. חלק מתאי הגידול באדנוקרצינומה רירית עשויים להכיל כמות גדולה של מוצין תוך תאי (מוצין בתוך התא) שדוחף את הגרעין לקצה התא. תאים אלו נקראים תאי טבעת חותם והם נראים בדרך כלל באדנוקרצינומה רירית של המעי הגס.
כיצד מדרגים פתולוגים אדנוקרצינומה רירית?
פתולוגים משתמשים במונח מובחן כדי לחלק אדנוקרצינומה רירית לארבע דרגות - מובחן היטב, מובחן בינוני, מובחן גרוע ובלתי מובחן. הציון מבוסס על אחוז הגידול היוצר מבנים עגולים הנקראים בלוטות. גידול מובחן היטב (דרגה 1) הוא יותר מ-95% בלוטות. גידול מובחן בינוני (דרגה 2) הוא 50 עד 95% בלוטות. גידול מובחן גרוע (דרגה 3) הוא פחות מ-50% בלוטות. גידול לא מובחן (דרגה 4) אינו מייצר בלוטות. הציון חשוב מכיוון שגידולים פחות מובחנים (למשל גידולים מובחנים ובלתי מובחנים) מתנהגים בצורה אגרסיבית יותר ויש סיכוי גבוה יותר להתפשט לחלקים אחרים בגוף.
מה המשמעות של פלישה?
פתולוגים משתמשים במילה פלישה לתאר את התפשטות תאי הגידול מהחלק הפנימי של המעי הגס אל הרקמות שמסביב. אדנוקרצינומה רירית מתחילה מה- בלוטות על פני השטח הפנימיים של המעי הגס. הבלוטות הן חלק משכבה דקה של רקמה הנקראת רירית. שכבות הרקמה מתחת לרירית כוללות את התת-רירית, ה-muscularis propria, רקמת השומן התת-סרוסלית וסרוסה. ככל שהגידול גדל התאים יכולים להתפשט לשכבות אלו. בסופו של דבר, תאי הגידול יכולים לפרוץ דרך המשטח החיצוני של המעי הגס ולהתפשט ישירות לאיברים ורקמות סמוכים.
רמת הפלישה היא נקודת הפלישה העמוקה ביותר וניתן למדוד אותה רק לאחר בדיקת הגידול במיקרוסקופ על ידי פתולוג. רמת הפלישה חשובה מכיוון שגידולים שפולשים עמוק יותר לדופן המעי הגס נוטים יותר להתפשט לחלקים אחרים בגוף. רמת הפלישה משמשת גם לקביעת שלב הגידול הפתולוגי (pT).
מה המשמעות של פלישה פרינוראלית?
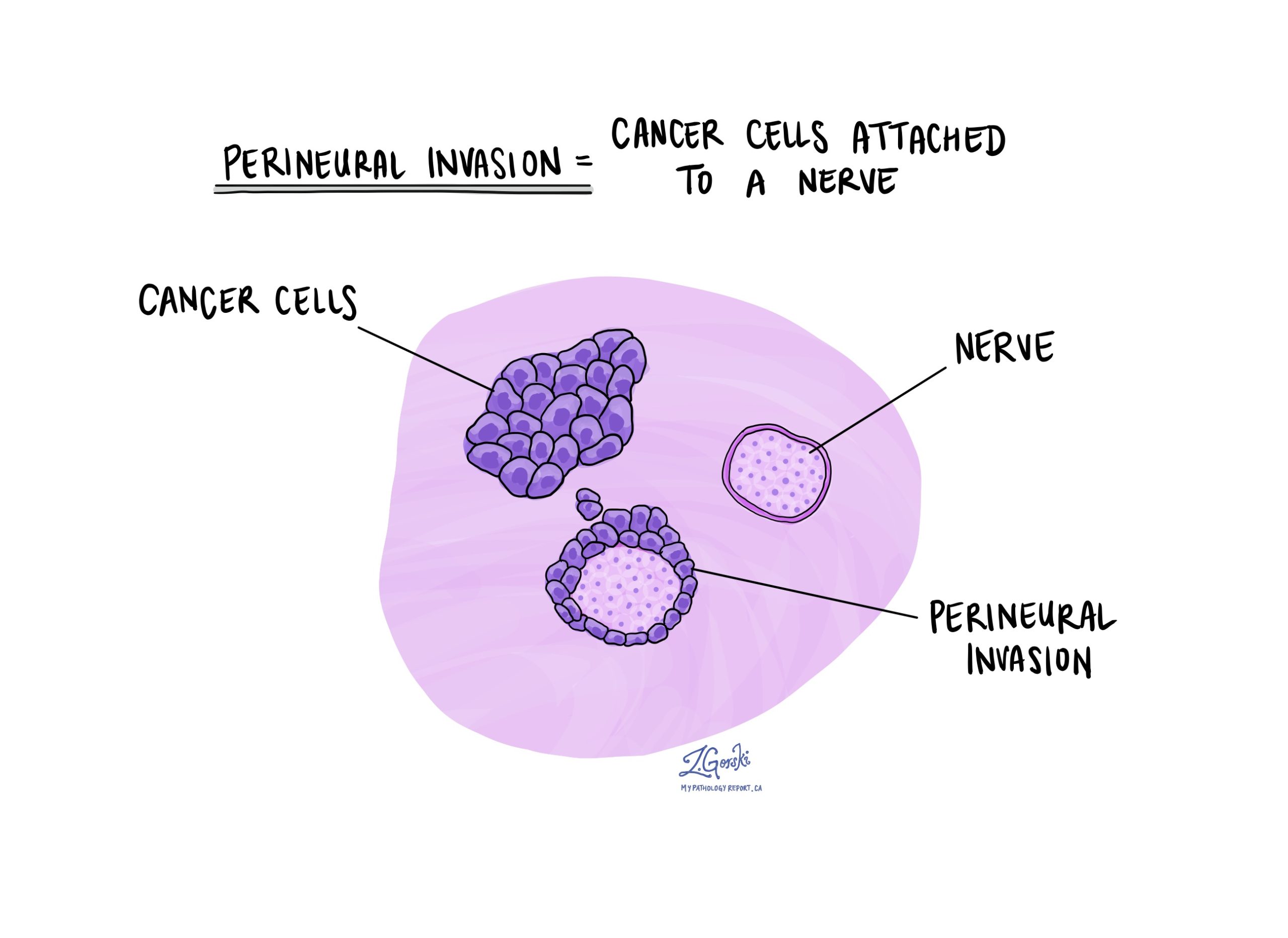
עצבים הם כמו חוטים ארוכים המורכבים מקבוצות תאים הנקראות נוירונים. עצבים נמצאים בכל הגוף והם אחראים על שליחת מידע (כגון טמפרטורה, לחץ וכאב) בין הגוף למוח. פלישה פרינוראלית היא מונח שפתולוגים משתמשים בהם כדי לתאר תאי גידול המחוברים לעצב. פלישה פרינוראלית חשובה מכיוון שתאי גידול שנקשרו לעצב יכולים לצמוח לאורך העצב ואל הרקמות הסובבות אותו. זה מגביר את הסיכון שהגידול יצמח מחדש לאחר הטיפול.
מה המשמעות של פלישה לימפווסקולרית?
דם נע ברחבי הגוף דרך צינורות ארוכים ודקים הנקראים כלי דם. סוג נוסף של נוזל הנקרא לימפה המכיל פסולת ותאי חיסון נע ברחבי הגוף דרך תעלות לימפה. המונח פלישה לימפה וכלי דם משמש לתיאור תאי גידול שנמצאים בתוך כלי דם או תעלת לימפה. פלישה לימפה וכלי דם חשובה מכיוון שברגע שתאי הגידול נמצאים בתוך כלי דם או תעלת לימפה הם מסוגלים גרורות (להתפשט) לחלקים אחרים בגוף כגון בלוטות לימפה או הריאות.
נוכחותם של תאי גידול בתוך וריד גדול מעבר לדופן המעי הגס (מחוץ לצרור השריר העבה) קשורה לסיכון גבוה שהתאים הסרטניים יימצאו בסופו של דבר בכבד.

מה זה שוליים?
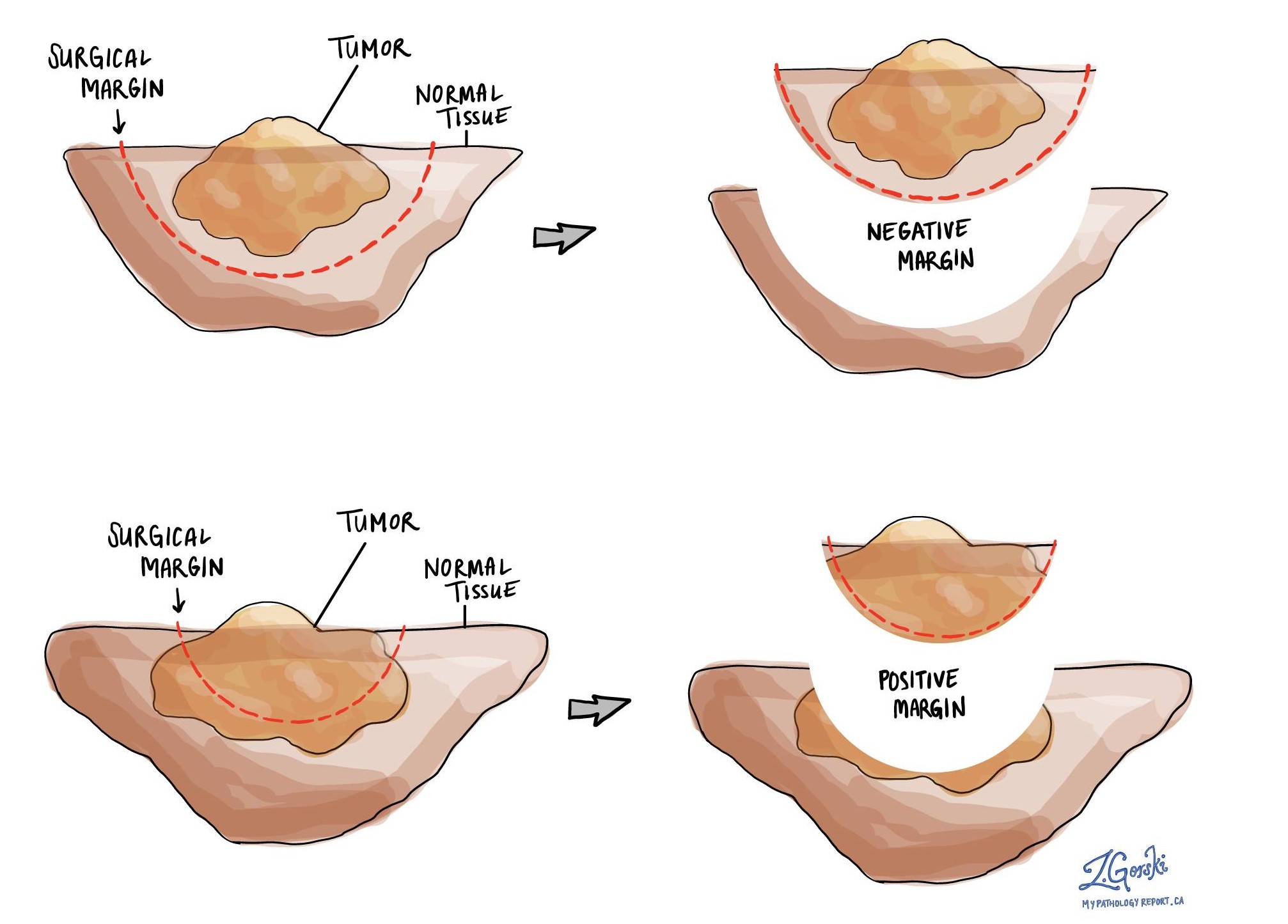
במעי הגס, א שולים היא כל רקמה שנחתכה על ידי המנתח על מנת להסיר את הגידול מגופך. המעי הגס הוא צינור ארוך והמנתח שלך יצטרך לחתוך חלק מהצינור כדי להסיר את הגידול מגופך. שני הקצוות החתוכים של הצינור נקראים השוליים הפרוקסימליים והדיסטליים. השוליים הרדיאליים הם כל רקמה סביב הצינור שיש לחתוך.
שוליים נקראים שליליים אם לא רואים תאים סרטניים בקצה החתוך של הרקמה. מרווח נחשב חיובי כאשר ישנם תאים סרטניים ממש בקצה הרקמה החתוכה. מרווח חיובי קשור לסיכון גבוה יותר שהגידול יחזור באותו מקום לאחר הטיפול.
הדוח שלך יתאר גם אם יש אדנומות או מצבים טרום סרטניים אחרים נראו בשוליים. השוליים יתואר בדוח שלך רק לאחר הסרת הגידול כולו.
מהו הפקדת גידול?
מאגר גידול הוא קבוצה של תאים סרטניים הנפרדים מהגידול הראשי אך לא ב-a בלוטת לימפה. נוכחות של משקעי גידול קשורה לסיכון גבוה יותר שסרטן יתפשט לאתר גוף אחר כגון הריאות לאחר הטיפול.
מה המשמעות של ניצני גידול?
ניצני גידול הוא מונח שפתולוגים משתמשים בהם כדי לתאר תאים סרטניים בודדים או קבוצות קטנות של תאים סרטניים הנראים בקצה הגידול. ניקוד מוקצה, נמוך, בינוני או גבוה, על סמך מספר הניצנים הנראים במיקרוסקופ. ציון גבוה קשור לסיכון מוגבר שתאים סרטניים יתפשטו לחלק אחר בגוף.
מה המשמעות של השפעת הטיפול?
אם קיבלת טיפול (כימותרפיה או הקרנות או שניהם) בסרטן שלך לפני הסרת הגידול, הפתולוג שלך יבדוק היטב את אזור הרקמה שבו זוהה הגידול כדי לראות אם תאים סרטניים עדיין חיים ( בַּר חַיִים).
המערכת הנפוצה ביותר מתארת את השפעת הטיפול בסולם של 0 עד 3 כאשר 0 הוא ללא תאים סרטניים ברי קיימא (כל התאים הסרטניים מתים) ו-3 הוא סרטן שיורי נרחב ללא נסיגה ניכרת של הגידול (כל או רוב הגידולים תאים סרטניים חיים).
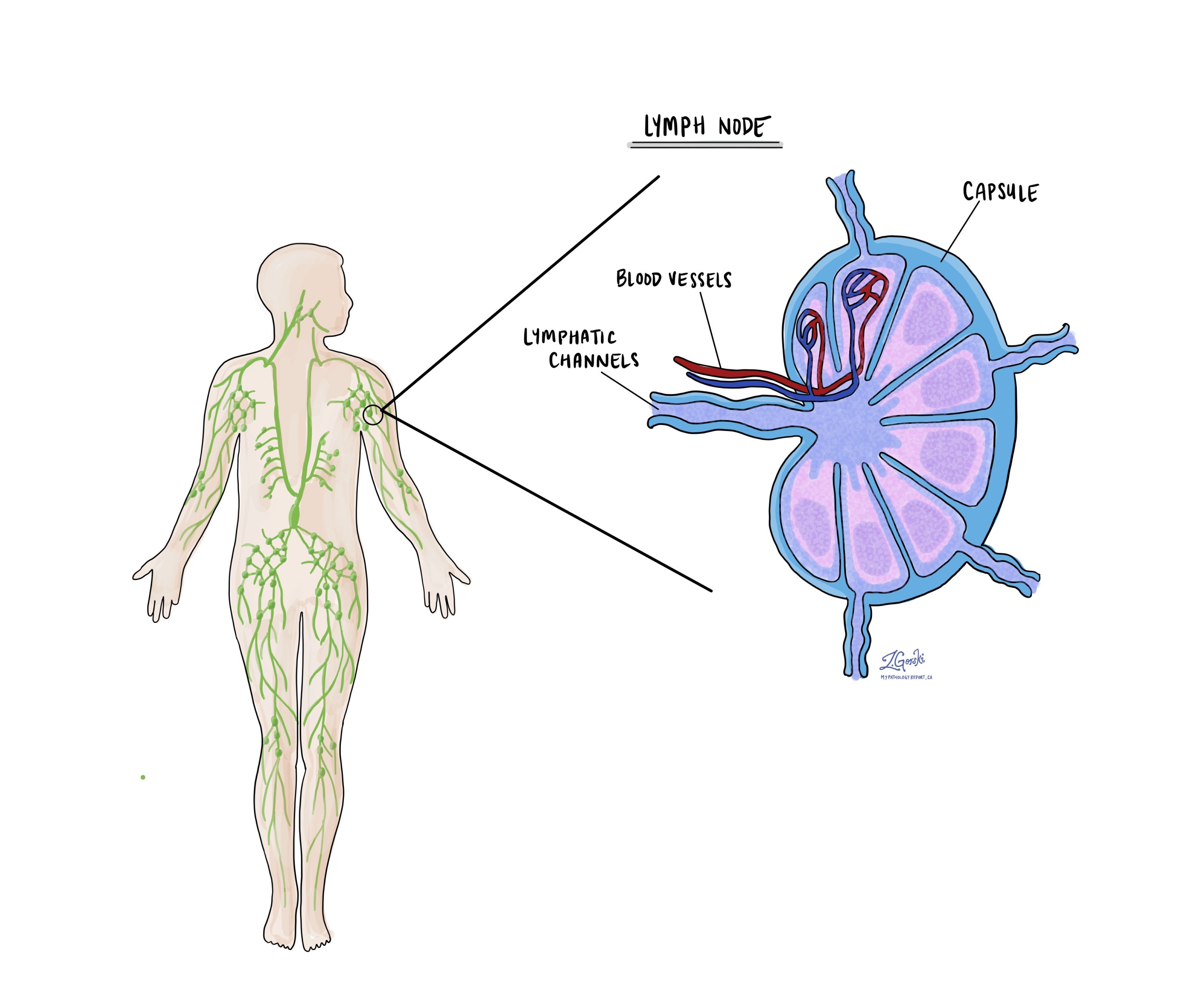
מהן בלוטות לימפה?
בלוטות לימפה הם איברים חיסוניים קטנים הממוקמים בכל הגוף. תאי סרטן יכולים לעבור מהגידול לבלוטת לימפה דרך תעלות לימפה הממוקמות בתוך ומסביב לגידול (ראה פלישה לימפה וכלי דם לעיל). התנועה של תאים סרטניים מהגידול לבלוטת לימפה נקראת גרורות.
רוב הדוחות כוללים את המספר הכולל של בלוטות הלימפה שנבדקו ואת המספר, אם בכלל, המכילים תאים סרטניים. הפתולוג שלך יבדוק בקפידה את כל בלוטות הלימפה עבור תאים סרטניים. בלוטות לימפה המכילות תאים סרטניים נקראות לעתים קרובות חיוביות ואילו אלה שאינן מכילות תאים סרטניים נקראות שליליות.
מציאת תאים סרטניים בא בלוטת לימפה חשוב כי זה קשור לסיכון גבוה יותר שהתאים הסרטניים יימצאו בבלוטות לימפה אחרות או באיבר מרוחק כמו הריאות. בדיקת בלוטות הלימפה משמשת גם לקביעת שלב הצמתים (ראה שלב פתולוגי להלן).
מהם חלבונים לתיקון אי התאמה?
תיקון אי התאמה (MMR) היא מערכת בתוך כל התאים התקינים והבריאים לתיקון טעויות בחומר הגנטי שלנו (DNA). המערכת מורכבת מחלבונים שונים וארבעת הנפוצים ביותר נקראים MSH2, MSH6, MLH1 ו-PMS2.
ארבעת חלבוני תיקון אי ההתאמה MSH2, MSH6, MLH1 ו-PMS2 פועלים בזוגות כדי לתקן DNA פגום. באופן ספציפי, MSH2 עובד עם MSH6 ו-MLH1 עובד עם PMS2. אם חלבון אחד אובד, הזוג לא יכול לתפקד כרגיל. אובדן של אחד מהחלבונים הללו מגביר את הסיכון לפתח סרטן.
פתולוגים מזמינים בדיקת תיקון אי התאמה כדי לראות אם אחד מהחלבונים הללו אובד בגידול. אם הוזמנה בדיקת תיקון אי התאמה בדגימת הרקמה שלך, התוצאות יתוארו בדוח הפתולוגיה שלך.
כיצד בודקים פתולוגים חלבונים לתיקון אי התאמה?
הדרך הנפוצה ביותר לבדוק חלבונים לתיקון אי התאמה היא לבצע בדיקה הנקראת אימונוהיסטוכימיה. בדיקה זו מאפשרת לפתולוגים לראות אם תאי הגידול מייצרים את כל ארבעת החלבונים לתיקון אי-התאמה.
אם תאי הגידול אינם מייצרים אחד מהחלבונים, הדוח שלך יתאר חלבון זה כ"אבוד" או "חסר". מכיוון שחלבוני תיקון אי ההתאמה פועלים בזוגות (MSH2 + MSH6 ו-MLH1 + PMS2), שני חלבונים הולכים לאיבוד בו-זמנית.
אם תאי הגידול בדגימת הרקמה שלך מראים אובדן של חלבון אחד או יותר לתיקון אי-התאמה, ייתכן שירשת את תסמונת לינץ' ויש להפנות למומחה גנטי לבדיקות נוספות וייעוץ.
כיצד פתולוגים קובעים את השלב הפתולוגי (pTNM) עבור אדנוקרצינומה רירית?
השלב הפתולוגי של אדנוקרצינומה רירית מבוסס על מערכת ה-TNM, מערכת מוכרת בינלאומית שנוצרה במקור על ידי הוועדה המשותפת האמריקאית לסרטן. מערכת זו משתמשת במידע על הראשי גידול סרטני (ת), בלוטות לימפה (נ), ומרוחקת גרורתי מחלה (M) כדי לקבוע את השלב הפתולוגי המלא (pTNM). הפתולוג שלך יבדוק את הרקמה שהוגשה ויתן מספר לכל חלק. באופן כללי, מספר גבוה יותר פירושו מחלה מתקדמת יותר וחמורה יותר פּרוֹגנוֹזָה.
שלב הגידול (pT) עבור אדנוקרצינומה רירית
אדנוקרצינומה רירית ניתנת לשלב גידולי בין 1 ל-4 בהתבסס על המרחק שעברו תאי הסרטן מהרירית אל דופן המעי הגס או הרקמות שמסביב (הרחבת הגידול).
- T1 - הגידול נמצא בתת הרירית ממש מתחת לרירית על פני השטח הפנימיים של המעי הגס.
- T2 - הגידול נכנס ל-muscularis propria של המעי הגס.
- T3 – הגידול שעבר את כל דופן השריר ונמצא בשומן ליד המשטח החיצוני של המעי הגס.
- T4 - הגידול נמצא בסרוסה על פני השטח החיצוניים של המעי הגס או שהוא נכנס לאיברים מסביב כמו שלפוחית השתן או דופן הבטן.
שלב נודאלי (pN) עבור אדנוקרצינומה רירית
אדנוקרצינומה רירית מקבלת שלב צמתים בין 0 ל-2 בהתבסס על האם נמצאו תאים סרטניים כלשהם באחד מהמחלות. בלוטות לימפה נבדק או מציאת משקעי גידול. אם לא נמצאו תאים סרטניים באף אחת מבלוטות הלימפה שנבדקו, שלב הצמתים הוא N0. אם לא נשלחו בלוטות לימפה לבדיקה פתולוגית, לא ניתן לקבוע את שלב הצמתים והוא רשום כ-NX.
שלב גרורתי (pM) עבור אדנוקרצינומה רירית
אדנוקרצינומה רירית ניתנת לשלב גרורתי של 0 או 1 בהתבסס על נוכחות של תאים סרטניים באתר מרוחק בגוף (למשל הכבד). ניתן להקצות את שלב M רק אם רקמה מאתר מרוחק מוגשת לבדיקה פתולוגית. מכיוון שרקמה זו קיימת לעתים רחוקות, לא ניתן לקבוע את שלב ה-M והוא רשום כ-X.


