کیتھرین فورس ایم ڈی ایف آر سی پی سی اور جیسن واسرمین ایم ڈی پی ایچ ڈی ایف آر سی پی سی
اپریل 24، 2024
انٹرا میوکوسل ایڈینو کارسینوما ابتدائی مرحلے کے غذائی نالی کے کینسر کی ایک قسم ہے۔ اسے 'انٹرموکوسل' کہا جاتا ہے کیونکہ ٹیومر کے خلیے ٹیومر کے خلیات سے زیادہ نہیں پھیلے ہیں۔ چپچپا، غذائی نالی کے اندر ٹشو کی ایک پتلی تہہ۔ اگر علاج نہ کیا گیا تو، ٹیومر کے خلیات غذائی نالی میں مزید پھیل جائیں گے جس کے نتیجے میں ایک زیادہ سنگین حالت پیدا ہو جائے گی جسے محض کہا جاتا ہے۔ اڈینوکارنیوما. انٹرا میوکوسل ایڈینو کارسینوما کے مریضوں کے علاج کے اختیارات میں اینڈوسکوپک میوکوسل ریسیکشن (EMR) اور بعض اوقات اینڈوسکوپک سب میوکوسل ڈسیکشن (ESD) شامل ہیں۔
یہ مضمون آپ کو غذائی نالی کے intramucosal adenocarcinoma کے لیے آپ کی پیتھالوجی رپورٹ کو پڑھنے اور سمجھنے میں مدد کرے گا۔
غذائی نالی
غذائی نالی ایک کھوکھلی پٹھوں کی نالی ہے جو گلے کو معدے سے جوڑتی ہے۔ اس کا بنیادی کام ہاضمے کے لیے خوراک اور مائعات کو منہ سے معدے تک پہنچانا ہے۔ جب آپ نگلتے ہیں تو غذائی نالی کی دیواریں مربوط طریقے سے سکڑ جاتی ہیں — یہ حرکت، جسے peristalsis کہتے ہیں، خوراک کو نیچے کی طرف دھکیل دیتی ہے۔ غذائی نالی کے دونوں سروں پر اسفنکٹرز بھی ہوتے ہیں۔ یہ عضلاتی والوز کھانے اور مائعات کو پیٹ میں جانے کی اجازت دینے کے لیے کھلتے ہیں اور پیٹ کے مواد کو غذائی نالی اور منہ میں واپس جانے سے روکنے کے لیے بند ہوتے ہیں۔
غذائی نالی کا انٹرا میوکوسل ایڈینو کارسینوما کہاں سے شروع ہوتا ہے؟
غذائی نالی کا انٹرا میوکوسل ایڈینو کارسینوما عام طور پر شروع ہوتا ہے۔ غدود کے خلیات غذائی نالی کے نچلے حصے کی پرت، جو معدے کے ساتھ سنگم کے قریب ہے۔ اس علاقے کو گیسٹرو فیجیل جنکشن کے نام سے جانا جاتا ہے۔ اس قسم کا کینسر اکثر ایسی حالت سے منسلک ہوتا ہے جسے کہا جاتا ہے۔ بیریٹ کی غذائی نالی، جہاں عام ہے squamous خلیات غذائی نالی کی جگہ غدود کے خلیات لے لیتے ہیں۔
غذائی نالی میں انٹرا میوکوسل ایڈینو کارسینوما کی علامات کیا ہیں؟
اننپرتالی کے انٹرا میوکوسل ایڈینو کارسینوما کی سب سے عام علامات نگلنے میں دشواری (خاص طور پر ٹھوس غذا)، سینے میں درد، تیزاب کا خراب ہونا، اور وزن میں کمی ہے۔
غذائی نالی کے intramucosal adenocarcinoma کی کیا وجہ ہے؟
غذائی نالی کا انٹرا میوکوسل ایڈینو کارسینوما ایک ایسی حالت سے پیدا ہوتا ہے جسے کہا جاتا ہے۔ بیریٹ کی غذائی نالی جو غذائی نالی میں معدے کے تیزاب کے طویل مدتی ریفلکس (ایسڈ ریفلوکس بیماری) کی وجہ سے ہوتا ہے۔ اس وجہ سے، غذائی نالی میں intramucosal adenocarcinoma اکثر ایسڈ ریفلوکس کے کئی سالوں کے بعد تیار ہوتا ہے۔
جب غذائی نالی کا اندرونی حصہ طویل عرصے تک معدے کے تیزاب کے سامنے آجاتا ہے۔ squamous خلیات جو کہ عام طور پر غذائی نالی کے اندر کا احاطہ کرتے ہیں ان کی جگہ غدود کے خلیات ہوتے ہیں جو چھوٹی آنت کے اندر پائے جانے والے خلیوں کی طرح ہوتے ہیں۔ یہ آنتوں کی قسم کے خلیات معدے میں پیدا ہونے والے مضبوط تیزاب سے ہونے والی چوٹ کے خلاف زیادہ مزاحم ہوتے ہیں۔ squamous خلیات سے آنتوں کے قسم کے خلیات میں تبدیلی کہا جاتا ہے آنتوں کا میٹاپلیسیا.
بیریٹ کی غذائی نالی وہ نام ہے جو ڈاکٹر غذائی نالی میں آنتوں کے میٹاپلاسیا کو بیان کرنے کے لیے استعمال کرتے ہیں۔ اس کا نام ڈاکٹر نارمن آر بیریٹ کے نام پر رکھا گیا ہے، ایک سرجن جنہوں نے 1950 کی دہائی میں لندن، انگلینڈ میں پریکٹس کی۔ جن لوگوں کو بیریٹ کی غذائی نالی کئی سالوں تک رہتی ہے ان میں ایک قسم کی غیر معمولی نشوونما ہو سکتی ہے جسے کہا جاتا ہے۔ dysplasia کے جو انٹرا میوکوسل اڈینو کارسینوما کی نشوونما کے بڑھتے ہوئے خطرے سے وابستہ ہے۔
esophagus کے intramucosal adenocarcinoma کے لیے آپ کی پیتھالوجی رپورٹ میں کیا دیکھنا ہے:
ہسٹولوجک گریڈ
پیتھالوجسٹ اننپرتالی کے انٹرا میوکوسل ایڈینو کارسینوما کو تین درجات میں تقسیم کرنے کے لیے تفریق کی اصطلاح استعمال کرتے ہیں – اچھی طرح سے تفریق، اعتدال پسند، اور ناقص تفریق۔ گریڈ ٹیومر کی تشکیل کے فیصد پر مبنی ہے جسے گول ڈھانچے کہتے ہیں۔ acorns کے. ایک ٹیومر جو کوئی غدود نہیں بنا رہا ہوتا ہے اسے غیر متفاوت کہا جاتا ہے۔ درجہ اہم ہے کیونکہ ناقص تفریق اور غیر متفاوت ٹیومر زیادہ جارحانہ انداز میں برتاؤ کرتے ہیں اور جسم کے دوسرے حصوں میں پھیلنے کا زیادہ امکان ہوتا ہے، جیسے لمف نوڈس.
غذائی نالی کے انٹراموکوسل اڈینو کارسینوما کی درجہ بندی اس طرح کی جاتی ہے:
- اچھی طرح سے مختلف اڈینو کارسینوما: 95% سے زیادہ ٹیومر غدود پر مشتمل ہوتا ہے۔ پیتھالوجسٹ ان ٹیومر کو گریڈ 1 کے طور پر بھی بیان کرتے ہیں۔
- اعتدال سے مختلف اڈینو کارسینوماٹیومر کا 50 سے 95 فیصد حصہ غدود پر مشتمل ہوتا ہے۔ پیتھالوجسٹ ان ٹیومر کو گریڈ 2 کے طور پر بھی بیان کرتے ہیں۔
- غیر تسلی بخش اڈینو کارسینوما: 50% سے بھی کم ٹیومر غدود پر مشتمل ہوتا ہے۔ پیتھالوجسٹ ان ٹیومر کو گریڈ 3 کے طور پر بھی بیان کرتے ہیں۔

حملے کی گہرائی اور پیتھولوجک ٹیومر مرحلے (پی ٹی)
غذائی نالی کا انٹرا میوکوسل ایڈینو کارسینوما غذائی نالی کی اندرونی سطح پر ٹشو کی ایک پتلی تہہ سے شروع ہوتا ہے جسے میوکوسا کہتے ہیں۔ غذائی نالی میں، میوکوسا تین حصوں پر مشتمل ہوتا ہے: اپیتھیلیم، لامینا پروپریا، اور مسکولرس میوکوسا۔ آپ کی پیتھالوجی رپورٹ یہ بتا سکتی ہے کہ میوکوسا کے کون سے حصے ٹیومر میں شامل ہیں۔ تعریف کے مطابق، غذائی نالی کے تمام انٹراموکوسل اڈینو کارسینوماس کو پیتھولوجک ٹیومر اسٹیج pT1a تفویض کیا گیا ہے۔
پیرینیورل یلغار
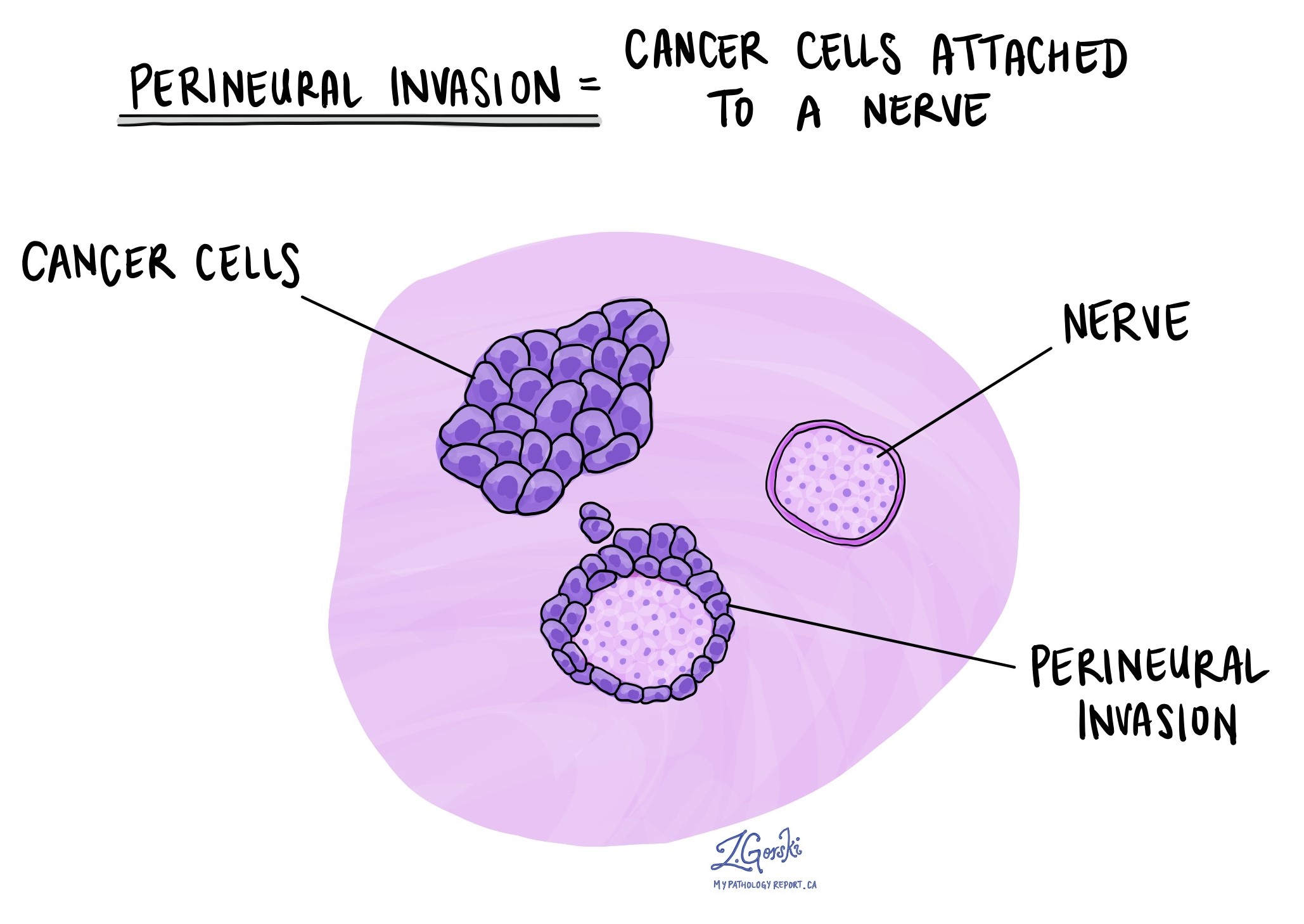
پیتھالوجسٹ اس صورت حال کو بیان کرنے کے لیے "پیرینیورل انویوژن" کی اصطلاح استعمال کرتے ہیں جہاں کینسر کے خلیے اعصاب سے منسلک ہوتے ہیں یا اس پر حملہ کرتے ہیں۔ "انٹرانیورل یلغار" ایک متعلقہ اصطلاح ہے جو خاص طور پر اعصاب کے اندر پائے جانے والے کینسر کے خلیوں سے مراد ہے۔ اعصاب، لمبی تاروں سے ملتے جلتے، خلیات کے گروپوں پر مشتمل ہوتے ہیں جنہیں نیوران کہتے ہیں۔ یہ اعصاب، پورے جسم میں موجود ہیں، جسم اور دماغ کے درمیان درجہ حرارت، دباؤ اور درد جیسی معلومات منتقل کرتے ہیں۔ perineural حملے کی موجودگی اہم ہے کیونکہ یہ کینسر کے خلیوں کو اعصاب کے ساتھ ساتھ قریبی اعضاء اور بافتوں میں سفر کرنے کی اجازت دیتا ہے، جس سے سرجری کے بعد ٹیومر کے دوبارہ ہونے کا خطرہ بڑھ جاتا ہے۔
لیموفواسکولر یلغار۔
لمفوواسکولر یلغار اس وقت ہوتی ہے جب کینسر کے خلیات خون کی نالی یا لیمفاٹک برتن پر حملہ کرتے ہیں۔ خون کی نالیاں پتلی ٹیوبیں ہوتی ہیں جو پورے جسم میں خون لے جاتی ہیں، جب کہ لیمفیٹک وریدیں خون کی بجائے لمف نامی سیال لے جاتی ہیں۔ یہ لیمفیٹک وریدیں پورے جسم میں بکھرے ہوئے چھوٹے مدافعتی اعضاء سے جڑتی ہیں، جنہیں کہا جاتا ہے۔ لمف نوڈس. لمفوواسکولر یلغار اہم ہے کیونکہ یہ کینسر کے خلیوں کو خون یا لمف کی نالیوں کے ذریعے جسم کے دیگر حصوں بشمول لمف نوڈس یا جگر میں پھیلنے کے قابل بناتا ہے۔

حاشیے
پیتھالوجی میں، مارجن ٹیومر کی سرجری کے دوران ہٹائے جانے والے ٹشو کا کنارہ ہے۔ پیتھالوجی رپورٹ میں مارجن کی حیثیت اہم ہے کیونکہ یہ بتاتی ہے کہ آیا پورا ٹیومر ہٹا دیا گیا تھا یا کچھ پیچھے رہ گیا تھا۔ یہ معلومات مزید علاج کی ضرورت کا تعین کرنے میں مدد کرتی ہے۔
پیتھالوجسٹ عام طور پر جراحی کے طریقہ کار کے بعد مارجن کا اندازہ لگاتے ہیں جیسے کہ حوصلہ افزا or ریسیکشن، جو پورے ٹیومر کو ہٹا دیتا ہے۔ عام طور پر a کے بعد مارجن کا جائزہ نہیں لیا جاتا ہے۔ بایپسی، جو ٹیومر کے صرف ایک حصے کو ہٹاتا ہے۔
کے لئے اینڈوسکوپک ریسیکشن جہاں اننپرتالی کے اندر کا صرف ایک چھوٹا سا ٹکڑا ہٹا دیا گیا ہے ، حاشیے میں شامل ہوں گے:
- میوکوسل مارجن۔ - یہ وہ ٹشو ہے جو غذائی نالی کی اندرونی سطح کو لائن کرتا ہے۔ اس مارجن کا دوسرا نام پس منظر کا حاشیہ ہے۔
- گہرا حاشیہ۔ - یہ ٹشو اننپرتالی کی دیوار کے اندر ہے۔ یہ ٹیومر کے نیچے واقع ہے۔
پیتھالوجسٹ مارجن کا معائنہ کرتے ہیں کہ آیا ٹیومر کے خلیے ٹشو کے کٹے ہوئے کنارے پر موجود ہیں یا نہیں۔ ایک مثبت مارجن، جہاں ٹیومر کے خلیات پائے جاتے ہیں، یہ بتاتا ہے کہ جسم میں کچھ کینسر رہ سکتا ہے۔ اس کے برعکس، ایک منفی مارجن، جس کے کنارے پر ٹیومر کے خلیات نہیں ہیں، تجویز کرتا ہے کہ ٹیومر کو مکمل طور پر ہٹا دیا گیا تھا۔ کچھ رپورٹیں قریب ترین ٹیومر سیلز اور مارجن کے درمیان فاصلے کی پیمائش بھی کرتی ہیں، چاہے تمام مارجن منفی ہوں۔

علاج اثر
اگر آپ نے ٹیومر کو ہٹانے سے پہلے کینسر کا علاج (یا تو کیموتھراپی یا ریڈی ایشن تھراپی یا دونوں) حاصل کیا ہے، تو آپ کا پیتھالوجسٹ ٹشو کے اس حصے کا بغور معائنہ کرے گا جہاں پہلے ٹیومر کی شناخت کی گئی تھی تاکہ یہ معلوم کیا جا سکے کہ آیا کینسر کے کوئی خلیے ابھی بھی زندہ ہیں (قابل عمل)۔ سب سے زیادہ استعمال ہونے والا نظام علاج کے اثر کو 0 سے 3 کے پیمانے پر بیان کرتا ہے، جس میں 0 کینسر کے قابل عمل خلیے نہیں ہیں (کینسر کے تمام خلیے مر چکے ہیں) اور 3 وسیع بقایا کینسر ہیں جس میں ٹیومر کا کوئی ظاہری رجعت نہیں ہوتا ہے (تمام یا زیادہ تر کینسر کے خلیے زندہ ہیں)۔
باہم کارکن
ہیرکسیم
ہیرکسیم پروٹین کی ایک قسم ہے جو ایک رسیپٹر کے طور پر کام کرتی ہے، ایک سوئچ کی طرح کام کرتی ہے جو سیل کی نشوونما اور تقسیم کو کنٹرول کرتی ہے۔ کچھ ٹیومر خلیوں میں، HER2 کی زیادتی پیدا ہوتی ہے، جس کی وجہ سے عام خلیات کی نسبت بہت تیزی سے نشوونما اور تقسیم ہوتی ہے۔
esophageal adenocarcinoma کے پانچ میں سے تقریباً ایک کیس میں HER2 کی زیادہ پیداوار شامل ہوتی ہے۔ مخصوص علاج ایسے ٹیومر کو نشانہ بناتے ہیں جو اضافی HER2 پیدا کرتے ہیں۔ اس لیے، آپ کا پیتھالوجسٹ علاج کے بہترین طریقہ کا تعین کرنے کے لیے اضافی HER2 کے لیے ٹیومر کی جانچ کی سفارش کر سکتا ہے۔
adenocarcinoma میں HER2 کا پتہ لگانے کا سب سے عام طریقہ ایک ٹیسٹ ہے جسے امیونو ہسٹو کیمسٹری کہا جاتا ہے۔ اس ٹیسٹ کے نتائج عام طور پر درج ذیل طریقے سے رپورٹ کیے جاتے ہیں:
- منفی (0 یا 1) - ٹیومر کے خلیے اضافی HER2 پیدا نہیں کر رہے ہیں۔
- مساوی (2) - ہو سکتا ہے کہ ٹیومر کے خلیے اضافی HER2 پیدا کر رہے ہوں۔ اس صورت میں، پیتھالوجسٹ عام طور پر لیبارٹری ٹیسٹ کریں گے جسے کہا جاتا ہے۔ فلوروسینٹ ان سیٹو ہائبرڈائزیشن (FISH) یہ دیکھنے کے لیے کہ آیا ٹیومر کے خلیوں میں HER2 کی زیادہ جین کاپیاں ہیں۔ اس سے یہ معلوم کرنے میں مدد مل سکتی ہے کہ آیا ٹیومر زیادہ HER2 پروٹین کا اظہار کر رہا ہے۔
- مثبت (3) - ٹیومر کے خلیے یقینی طور پر HER2 کی اضافی مقدار پیدا کر رہے ہیں۔
مماثل مرمت پروٹین
Mismatch repair (MMR) تمام نارمل، صحت مند خلیات کے اندر ایک ایسا نظام ہے جو ہمارے جینیاتی مواد (DNA) کی غلطیوں کو ٹھیک کرتا ہے۔ نظام مختلف پروٹینوں پر مشتمل ہے، اور چار سب سے زیادہ عام ہیں MSH2، MSH6، MLH1، اور PMS2۔
چار مماثل مرمت پروٹین MSH2، MSH6، MLH1، اور PMS2 جوڑوں میں کام کرتے ہیں تاکہ خراب ڈی این اے کو ٹھیک کریں۔ خاص طور پر، MSH2 MSH6 کے ساتھ کام کرتا ہے، اور MLH1 PMS2 کے ساتھ کام کرتا ہے۔ اگر ایک پروٹین ضائع ہو جائے تو جوڑا عام طور پر کام نہیں کر سکتا، اور کینسر ہونے کا خطرہ بڑھ جاتا ہے۔
مماثل مرمت پروٹین کے لیے ٹیسٹ کرنے کا سب سے عام طریقہ ہے۔ امیونو ہسٹو کیمسٹری. یہ ٹیسٹ پیتھالوجسٹوں کو یہ دیکھنے کی اجازت دیتا ہے کہ آیا ٹیومر کے خلیے چاروں غیر مماثل مرمت پروٹین تیار کرتے ہیں۔ اس ٹیسٹ کے نتائج عام طور پر درج ذیل رپورٹ کیے جاتے ہیں:
- عام نتیجہ: پروٹین کا اظہار برقرار رکھا۔
- غیر معمولی نتیجہ: پروٹین کے اظہار کا نقصان۔
مماثل مرمت کی جانچ اہم ہے کیونکہ اس سے یہ اندازہ لگانے میں مدد مل سکتی ہے کہ بعض علاج کتنے اچھے طریقے سے کام کر سکتے ہیں۔ مثال کے طور پر، غیر مماثل مرمت کے پروٹین ایکسپریشن کے نقصان کے ساتھ کینسر میں PD-1 یا PD-L1 inhibitors جیسے امیونو تھراپی کے علاج کا زیادہ امکان ہوتا ہے۔ اس کی وجہ یہ ہے کہ اکثر ٹیومر کی کمی میں پائے جانے والے تغیرات سے نئے اینٹی جین پیدا ہوتے ہیں جو ٹیومر کو زیادہ دکھائی دیتے ہیں اور مدافعتی نظام کے لیے کمزور ہوتے ہیں۔
مماثل مرمت کی جانچ بھی ایسے مریضوں کی شناخت کے لیے کی جاتی ہے جن کو Lynch سنڈروم ہو سکتا ہے، جسے موروثی نان پولیپوسس کولوریکٹل کینسر (HNPCC) بھی کہا جاتا ہے۔ لنچ سنڈروم ایک جینیاتی عارضہ ہے جو مختلف قسم کے کینسر ہونے کا خطرہ بڑھاتا ہے، بشمول غذائی نالی کا کینسر، بڑی آنت کا کینسر، اینڈومیٹریال کینسر، رحم کا کینسر، اور پیٹ کا کینسر۔
PD-L1۔
PD-L1 (پروگرامڈ ڈیتھ-لیگینڈ 1) ایک پروٹین ہے جو عام، صحت مند خلیوں اور کینسر کے کچھ خلیوں کی سطح پر پایا جاتا ہے۔ اسے مدافعتی چیک پوائنٹ پروٹین کہا جاتا ہے کیونکہ یہ ٹی سیلز نامی مدافعتی خلیوں کی سرگرمی کو کم کر دیتا ہے۔ یہ خلیے عام طور پر کینسر کے خلیات جیسے غیر معمولی خلیات کا پتہ لگاتے ہیں اور انہیں جسم سے نکال دیتے ہیں۔ کینسر کے خلیے جو اس پروٹین سے بچنے کے حملے کا اظہار کرتے ہیں T خلیوں کے ذریعے T سیل پر ایک پروٹین کو فعال کرکے PD-1 کہتے ہیں۔
ڈاکٹر اس پروٹین کی جانچ کرتے ہیں تاکہ یہ تعین کرنے میں مدد ملے کہ کون سے مریض ایسے علاج سے فائدہ اٹھا سکتے ہیں جو PD-1/PD-L1 راستے کو نشانہ بناتے ہیں، جیسے کہ مدافعتی چیک پوائنٹ روکنے والے۔ PD-L1 اظہار کی جانچ کرنے کے لیے، پیتھالوجسٹ عام طور پر ایک ٹیسٹ کرتے ہیں جسے کہتے ہیں۔ امیونو ہسٹو کیمسٹری ٹیومر ٹشو کے نمونے پر۔ اس ٹیسٹ میں، PD-L1 کے خلاف ایک مخصوص اینٹی باڈی ٹشو سیکشن پر لگائی جاتی ہے اور پھر ڈائی سے منسلک سیکنڈری اینٹی باڈی کا استعمال کرتے ہوئے پتہ چلا۔
اس کے بعد پروٹین کے اظہار کی سطح کو مثبت خلیوں کی شدت اور فیصد کی بنیاد پر شمار کیا جاتا ہے اور اسکور کیا جاتا ہے۔ غذائی نالی کے کینسر کے لیے، نتیجہ مشترکہ مثبت سکور (CPS) کے طور پر رپورٹ کیا جاتا ہے، اسکور > 1 کو مثبت سمجھا جاتا ہے۔
اس مضمون کے بارے میں
ڈاکٹروں نے یہ مضمون آپ کی پیتھالوجی رپورٹ کو پڑھنے اور سمجھنے میں آپ کی مدد کے لیے لکھا ہے۔ ہم سے رابطہ کریں اگر آپ کے پاس اس مضمون یا اپنی پیتھالوجی رپورٹ کے بارے میں کوئی سوال ہے۔ پڑھیں اس مضمون ایک عام پیتھالوجی رپورٹ کے حصوں کے بارے میں مزید عام تعارف کے لیے۔


