от Catherine Forse MD FRCPC и Jason Wasserman MD PhD FRCPC
Април 24, 2024
Интрамукозният аденокарцином е вид ранен стадий на рак на хранопровода. Нарича се „интрамукозен“, защото туморните клетки не са се разпространили по-далеч от лигавицата, тънък слой тъкан вътре в хранопровода. Ако не се лекуват, туморните клетки ще се разпространят по-нататък в хранопровода, което ще доведе до по-сериозно състояние, просто наречено аденокарцином. Възможностите за лечение на пациенти с интрамукозен аденокарцином включват ендоскопска мукозна резекция (EMR) и понякога ендоскопска субмукозна дисекция (ESD).
Тази статия ще ви помогне да прочетете и разберете вашия патологичен доклад за интрамукозен аденокарцином на хранопровода.
Хранопровода
Хранопроводът е куха мускулна тръба, която свързва гърлото (фаринкса) със стомаха. Основната му функция е да транспортира храна и течности от устата до стомаха за храносмилане. Когато преглъщате, стените на хранопровода се свиват по координиран начин - това движение, наречено перисталтика, избутва храната надолу. Хранопроводът също има сфинктери в двата края; тези мускулни клапи се отварят, за да позволят на храната и течностите да преминат в стомаха, и се затварят, за да предотвратят обратния хладник на стомашното съдържание в хранопровода и устата.
Къде започва интрамукозният аденокарцином на хранопровода?
Интрамукозният аденокарцином на хранопровода обикновено започва от жлезисти клетки лигавицата на долната част на хранопровода, която е близо до кръстовището със стомаха. Тази област е известна като гастроезофагеална връзка. Този вид рак често се свързва със състояние, наречено Хранопровод на Барет, където нормалното плоскоклетъчни клетки на хранопровода се заменят с жлезисти клетки.
Какви са симптомите на интрамукозен аденокарцином в хранопровода?
Най-честите симптоми на интрамукозен аденокарцином на хранопровода са затруднено преглъщане (особено твърди храни), болка в гърдите, влошаване на киселинния рефлукс и загуба на тегло.
Какво причинява интрамукозен аденокарцином на хранопровода?
Интрамукозният аденокарцином на хранопровода възниква от състояние, наречено Хранопровод на Барет което се причинява от дълготраен рефлукс на стомашни киселини в хранопровода (киселинна рефлуксна болест). Поради тази причина интрамукозният аденокарцином в хранопровода често се развива след много години киселинен рефлукс.
Когато вътрешността на хранопровода е изложена на стомашна киселина за дълъг период от време, плоскоклетъчни клетки които обикновено покриват вътрешността на хранопровода, са заменени от жлезисти клетки, които са подобни на клетките, намиращи се от вътрешната страна на тънките черва. Тези клетки от чревен тип са по-устойчиви на нараняване от силните киселини, възникващи в стомаха. Промяната от сквамозни клетки към клетки от чревен тип се нарича чревна метаплазия.
Хранопровод на Барет е името, което лекарите използват, за да опишат чревната метаплазия в хранопровода. Кръстен е на д-р Норман Р. Барет, хирург, практикувал в Лондон, Англия през 1950-те години на миналия век. Хората, които имат хранопровод на Барет в продължение на много години, могат да развият вид анормален растеж, наречен дисплазия което е свързано с повишен риск от развитие на интрамукозен аденокарцином.
Какво да търсите във вашия патологичен доклад за интрамукозен аденокарцином на хранопровода:
Хистологична степен
Патолозите използват термина диференциран, за да разделят интрамукозния аденокарцином на хранопровода на три степени – добре диференциран, умерено диференциран и слабо диференциран. Степента се основава на процента на тумора, образуващ кръгли структури, наречени жлези. Тумор, който не образува никакви жлези, се нарича недиференциран. Степента е важна, тъй като слабо диференцираните и недиференцираните тумори се държат по-агресивно и е по-вероятно да се разпространят в други части на тялото, като напр. лимфни възли.
Интрамукозният аденокарцином на хранопровода се класифицира, както следва:
- Добре диференциран аденокарцином: Повече от 95% от тумора се състои от жлези. Патолозите също описват тези тумори като степен 1.
- Умерено диференциран аденокарцином: 50 до 95% от тумора се състои от жлези. Патолозите също описват тези тумори като степен 2.
- Слабо диференциран аденокарцином: По-малко от 50% от тумора се състои от жлези. Патолозите също описват тези тумори като степен 3.

Дълбочина на инвазия и стадий на патологичен тумор (pT)
Интрамукозният аденокарцином на хранопровода започва в тънък слой тъкан от вътрешната повърхност на хранопровода, наречен мукоза. В хранопровода лигавицата се състои от три части: епител, lamina propria и muscularis mucosae. Вашият патологичен доклад може да опише кои части от лигавицата са засегнати от тумора. По дефиниция всички интрамукозни аденокарциноми на хранопровода се определят като патологичен туморен стадий pT1a.
Периневрална инвазия
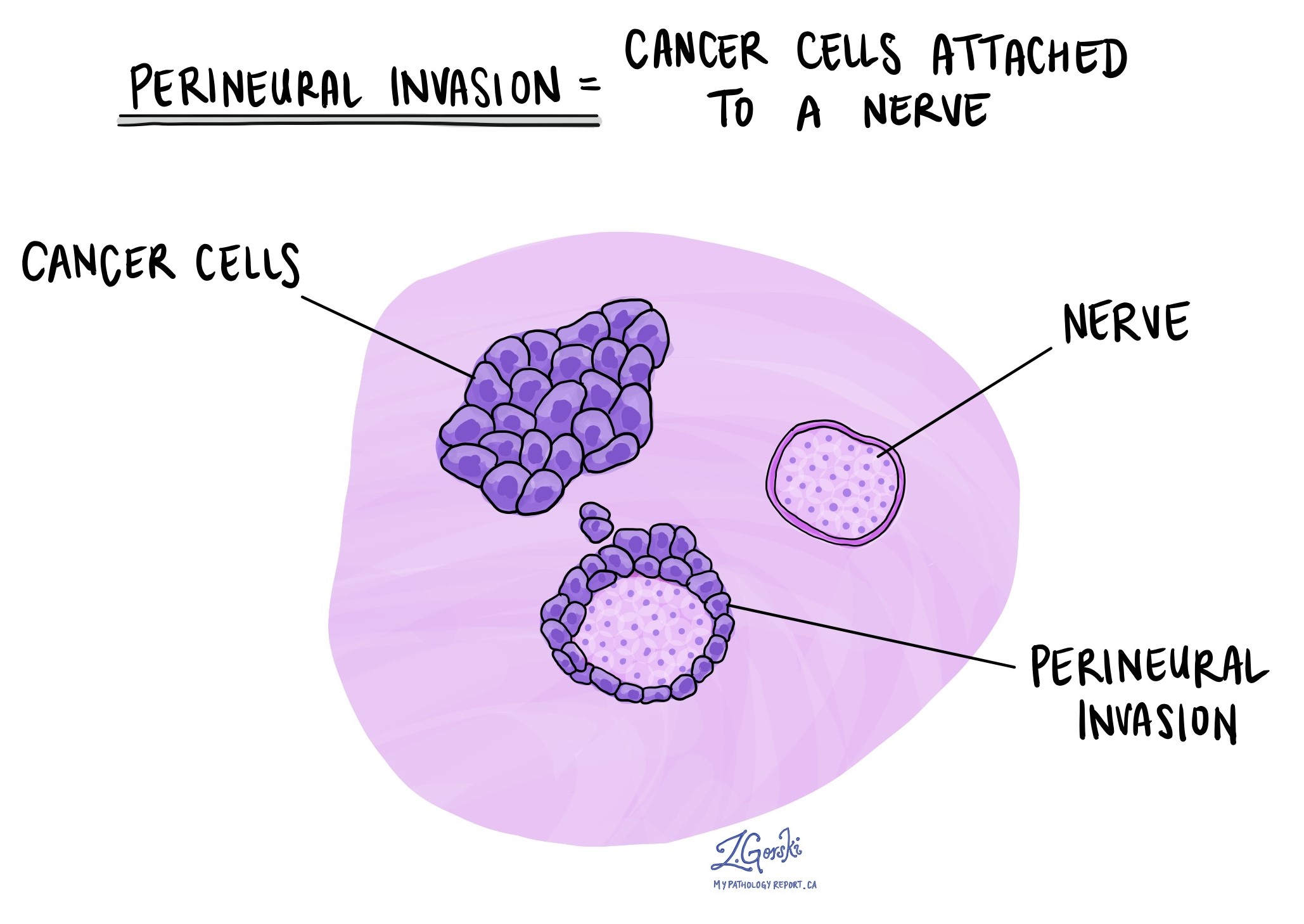
Патолозите използват термина „периневрална инвазия“, за да опишат ситуация, при която раковите клетки се прикрепят към или нахлуват в нерв. „Интраневрална инвазия“ е свързан термин, който конкретно се отнася до ракови клетки, намиращи се в нерв. Нервите, наподобяващи дълги жици, се състоят от групи клетки, известни като неврони. Тези нерви, присъстващи в цялото тяло, предават информация като температура, налягане и болка между тялото и мозъка. Наличието на периневрална инвазия е важно, защото позволява на раковите клетки да се придвижват по нерва до близките органи и тъкани, повишавайки риска от рецидив на тумора след операция.
Лимфоваскуларна инвазия
Лимфоваскуларна инвазия възниква, когато раковите клетки нахлуят в кръвоносен или лимфен съд. Кръвоносните съдове са тънки тръби, които пренасят кръв в цялото тяло, докато лимфните съдове пренасят течност, наречена лимфа, вместо кръв. Тези лимфни съдове се свързват с малки имунни органи, разпръснати из цялото тяло, известни като лимфни възли. Лимфоваскуларната инвазия е важна, защото позволява на раковите клетки да се разпространяват в други части на тялото, включително лимфни възли или черния дроб, чрез кръвоносните или лимфните съдове.

Полета
В патологията границата е ръбът на тъканта, отстранен по време на операция на тумора. Състоянието на границата в доклада за патология е важно, тъй като показва дали целият тумор е бил отстранен или някои са останали. Тази информация помага да се определи необходимостта от по-нататъшно лечение.
Патолозите обикновено оценяват границите след хирургична процедура като изрязване or ресекция, който премахва целия тумор. Маржовете обикновено не се оценяват след a биопсия, който премахва само част от тумора.
За ендоскопски резекции където е отстранена само малка част от вътрешността на хранопровода, полетата ще включват:
- Марж на лигавицата – Това е тъканта, която покрива вътрешната повърхност на хранопровода. Друго име за този марж е страничният марж.
- Дълбок марж – Тази тъкан е вътре в стената на хранопровода. Намира се под тумора.
Патолозите изследват границите, за да проверят дали туморните клетки присъстват в срязания ръб на тъканта. Положителна граница, където се откриват туморни клетки, предполага, че част от рак може да остане в тялото. За разлика от това, отрицателна граница, без туморни клетки по ръба, предполага, че туморът е бил напълно отстранен. Някои доклади също измерват разстоянието между най-близките туморни клетки и границата, дори ако всички граници са отрицателни.

Лечебен ефект
Ако сте получили лечение за рак (или химиотерапия, или лъчетерапия, или и двете) преди туморът да бъде отстранен, вашият патолог внимателно ще изследва областта от тъканта, където туморът е бил идентифициран преди това, за да види дали има ракови клетки, които са все още живи (жизнеспособни). Най-често използваната система описва ефекта от лечението по скала от 0 до 3, като 0 означава липса на жизнеспособни ракови клетки (всички ракови клетки са мъртви), а 3 е обширен остатъчен рак без видима регресия на тумора (всички или повечето от раковите клетки са живи).
биомаркери
HER2
HER2 е вид протеин, който функционира като рецептор, действайки като превключвател, който контролира растежа и деленето на клетките. В някои туморни клетки се произвежда излишък от HER2, което води до много по-бърз растеж и делене в сравнение с нормалните клетки.
Приблизително един на всеки пет случая на аденокарцином на хранопровода включва свръхпроизводство на HER2. Специфичните лечения са насочени към тумори, които произвеждат допълнителен HER2. Следователно вашият патолог може да препоръча тестване на тумора за излишък на HER2, за да определи най-добрия подход за лечение.
Най-честият метод за откриване на HER2 при аденокарцином е тест, наречен имунохистохимия. Резултатите от този тест обикновено се отчитат по следния начин:
- Отрицателен (0 или 1) – Туморните клетки не произвеждат допълнително HER2.
- Двусмислено (2) – Туморните клетки може да произвеждат допълнително HER2. В този случай патолозите обикновено извършват лабораторен тест, наречен флуоресцентна in situ хибридизация (FISH) за да видите дали туморните клетки имат повече генни копия на HER2. Това може да помогне да се определи дали туморът експресира повече HER2 протеин.
- Положителен (3) – Туморните клетки определено произвеждат допълнителни количества HER2.
Протеини за ремонт на несъответствие
Възстановяването на несъответствие (MMR) е система във всички нормални, здрави клетки, която поправя грешки в нашия генетичен материал (ДНК). Системата се състои от различни протеини, като четирите най-често срещани са MSH2, MSH6, MLH1 и PMS2.
Четирите протеина за ремонт на несъответствие MSH2, MSH6, MLH1 и PMS2 работят по двойки, за да коригират увредената ДНК. По-конкретно, MSH2 работи с MSH6, а MLH1 работи с PMS2. Ако един протеин се загуби, двойката не може да функционира нормално и рискът от развитие на рак се увеличава.
Най-често срещаният начин за тестване за протеини за възстановяване на несъответствие е имунохистохимия. Този тест позволява на патолозите да видят дали туморните клетки произвеждат и четирите протеина за възстановяване на несъответствието. Резултатите от този тест обикновено се отчитат, както следва:
- Нормален резултат: Запазена протеинова експресия.
- Ненормален резултат: Загуба на протеинова експресия.
Тестването за поправка на несъответствие е важно, защото може да помогне да се предвиди колко добре могат да работят определени лечения. Например, раковите заболявания със загуба на експресия на протеин за възстановяване на несъответствие е по-вероятно да реагират на имунотерапевтични лечения като PD-1 или PD-L1 инхибитори. Това е така, защото големият брой мутации, често открити в дефицитни тумори, могат да произведат нови антигени, които правят тумора по-видим и уязвим за имунната система.
Извършва се и тест за възстановяване на несъответствието, за да се идентифицират пациенти, които може да имат синдром на Lynch, известен също като наследствен неполипозен колоректален рак (HNPCC). Синдромът на Линч е генетично заболяване, което увеличава риска от развитие на различни видове рак, включително рак на хранопровода, рак на дебелото черво, рак на ендометриума, рак на яйчниците и рак на стомаха.
PD-L1
PD-L1 (Programmed Death-Ligand 1) е протеин, открит на повърхността на нормални, здрави клетки и някои ракови клетки. Нарича се имунен контролен протеин, защото намалява активността на имунните клетки, наречени Т клетки. Тези клетки обикновено откриват анормални клетки, като ракови клетки, и ги отстраняват от тялото. Раковите клетки, които експресират този протеин, избягват атаката на Т клетките чрез активиране на протеин върху Т клетката, наречен PD-1.
Лекарите тестват този протеин, за да помогнат да се определи кои пациенти могат да се възползват от лечения, насочени към PD-1/PD-L1 пътя, като например инхибитори на имунната контролна точка. За да тестват експресията на PD-L1, патолозите обикновено извършват тест, наречен имунохистохимия върху проба от туморна тъкан. При този тест специфично антитяло срещу PD-L1 се прилага върху тъканния участък и след това се открива с помощта на вторично антитяло, прикрепено към багрило.
Нивото на експресия на протеин след това се преброява и оценява въз основа на интензитета и процента на положителните клетки. За рак на хранопровода резултатът се отчита като комбиниран положителен резултат (CPS), като резултат > 1 се счита за положителен.
За тази статия
Лекарите написаха тази статия, за да ви помогнат да прочетете и разберете вашия патологичен доклад. Контакти ако имате някакви въпроси относно тази статия или вашия доклад за патология. Прочети тази статия за по-общо въведение в частите на типичен патологичен доклад.


