Jason Wasserman MD PhD FRCPC un Zuzanna Gorski MD
Janvāris 15, 2024
Invazīvā adenokarcinoma (pazīstama arī kā resnās zarnas adenokarcinoma) ir visizplatītākais resnās zarnas vēža veids. To veido šūnas, kas parasti pārklāj resnās zarnas iekšējo virsmu. Šis vēža veids bieži sākas ar polipu, piemēram, a cauruļveida adenoma, tubulovilozā adenoma, vai bārkstiņu adenoma.
Šis raksts palīdzēs jums izprast invazīvas resnās zarnas adenokarcinomas diagnozi un patoloģijas ziņojumu.
Resnās zarnas
Resnā zarna ir daļa no gremošanas sistēmas un resnās zarnas pirmā daļa. Tā ir gara doba caurule, kas sākas tievās zarnas galā un beidzas taisnajā zarnā. Resnā zarna ir sadalīta četrās daļās: augošā (pa labi), šķērseniskā, dilstošā (pa kreisi) un sigmoidā. Tam ir izšķiroša nozīme atkritumu pārstrādē un ūdens, elektrolītu un dažu vitamīnu uzsūkšanā. Invazīva adenokarcinoma var rasties jebkurā resnās zarnas daļā.
Kas izraisa invazīvu adenokarcinomu resnajā zarnā?
Tiek uzskatīts, ka invazīvu adenokarcinomu resnajā zarnā izraisa vides un ģenētisko faktoru kombinācija. Konstatētie riska faktori ietver pārmērīgu apstrādātas gaļas, sarkanās gaļas un alkohola patēriņu. Cilvēkiem ar lieko ķermeņa tauku daudzumu arī ir paaugstināts risks saslimt ar šāda veida vēzi. Ilgstoši iekaisums resnajā zarnā, ko var novērot iekaisīgas zarnu slimības (čūlainais kolīts un Krona slimība) gadījumā, ir saistīta arī ar paaugstinātu invazīvas adenokarcinomas attīstības risku.
Kādi ir invazīvas resnās zarnas adenokarcinomas simptomi?
Invazīvās adenokarcinomas simptomi ir atkarīgi no audzēja atrašanās vietas resnajā zarnā. Audzēji kreisajā resnajā zarnā (dilstošā resnajā zarnā) vai taisnajā zarnā var izraisīt izmaiņas zarnu ieradumos, asiņainus izkārnījumus, sāpes vēderā vai vēdera uzpūšanos. Audzēji labajā resnajā zarnā (augošā resnajā zarnā) var neizraisīt nekādus simptomus, kamēr audzējs nav ļoti liels vai nav izplatījies uz citām ķermeņa daļām.
Kur resnajā zarnā sākas invazīvā adenokarcinoma?
Invazīva resnās zarnas adenokarcinoma rodas no epitēlija šūnas parasti atrodas uz resnās zarnas iekšējās virsmas. Šīs epitēlija šūnas savienojas, veidojot struktūras, ko sauc dziedzeri. Dziedzeri kopā ar pamatā esošo lamina propria un muscularis mucosae veido plānu audu slāni, ko sauc par gļotādu. Ja audzēja šūnas pilnībā atrodas gļotādā, stāvokli sauc augstas pakāpes displāzija.
Augstas pakāpes displāzija tiek uzskatīta par neinvazīvu, pirmsvēža stāvokli, un audzēja šūnas to nevar metastizēt (izplatīties) uz citām ķermeņa daļām. Tomēr, audzējam augot un šūnām iekļūstot pamatā esošajos audu slāņos, diagnoze mainās uz invazīvu adenokarcinomu. Atšķirībā no augstas pakāpes displāzijas, audzēja šūnas invazīvā karcinomas gadījumā var metastēties (izplatīties) līdz limfmezgli un citas ķermeņa daļas.

Šī audzēja mikroskopiskās pazīmes
Mikroskopiskā izmeklēšanā invazīvā resnās zarnas adenokarcinoma sastāv no patoloģisku grupu grupām epitēlija šūnas parasti sakārtoti nemainīga izmēra dziedzeri (kas var izskatīties līdzīgi parastajiem dziedzeriem resnajā zarnā), ligzdām vai loksnēm.
Ko meklēt patoloģijas ziņojumā par invazīvu resnās zarnas adenokarcinomu:
Mucinozes diferenciācija
Patologi lieto terminu gļotādas diferenciācija, lai aprakstītu audzējus, kas satur lielu daudzumu ārpusšūnu mucins. Mucīns ir specializēts proteīna veids, ko ražo gan normālas šūnas, gan audzēja šūnas. Ekstracelulārs nozīmē, ka mucīns tika novērots ārpus audzēja šūnām. Ja vairāk nekā 50% audzēja veido mucīns, audzēju sauc gļotādas adenokarcinoma.
Histoloģiskā pakāpe
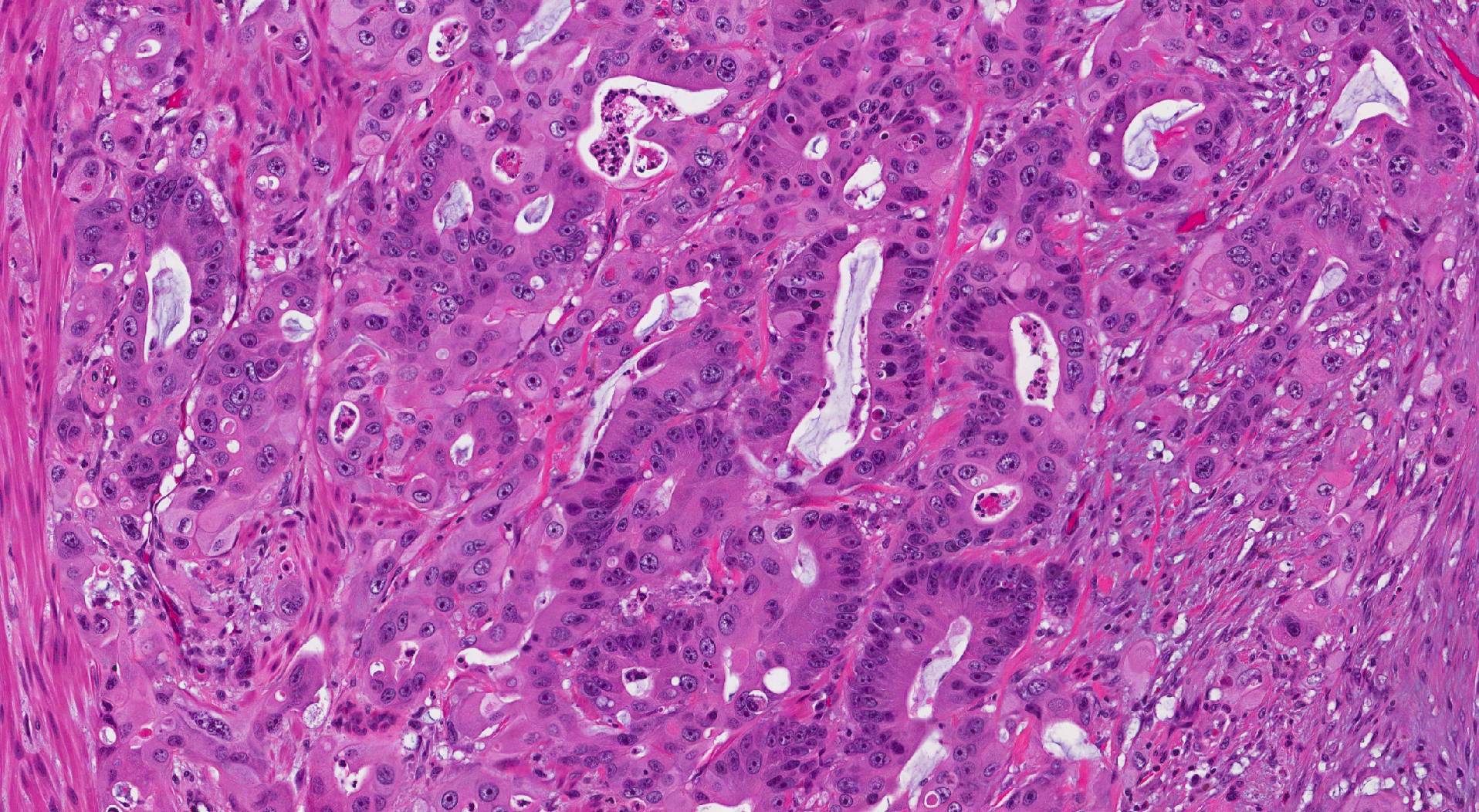
Invazīvā resnās zarnas adenokarcinoma ir sadalīta trīs pakāpēs - labi diferencēta, vidēji diferencēta un vāji diferencēta. Novērtējums ir balstīts uz audzēja šūnu procentuālo daudzumu, kas veido apaļas struktūras, ko sauc dziedzeri. Audzēju, kas neveido dziedzerus, sauc par nediferencētu. Atzīme ir svarīga, jo slikti diferencēti un nediferencēti audzēji mēdz uzvesties agresīvāk; piemēram, šie audzēji, visticamāk, izplatīsies uz limfmezgli un citas ķermeņa daļas.
- Labi diferencēts: vairāk nekā 95% audzēju veido dziedzeri. Patologi šos audzējus raksturo arī kā 1. pakāpi.
- Vidēji diferencēts: 50 līdz 95% audzēju veido dziedzeri. Patologi šos audzējus raksturo arī kā 2. pakāpi.
- Slikti diferencēts: mazāk nekā 50% audzēja veido dziedzeri. Patologi šos audzējus raksturo arī kā 3. pakāpi.
- Nediferencēts: audzēja vietā ir redzams ļoti maz dziedzeru.
Invāzijas dziļums un patoloģiskā audzēja stadija (pT)
Patoloģijā termins iebrukums apraksta vēža šūnu izplatīšanos orgānos vai audos, kas atrodas ap audzēja sākuma vietu. Tā kā invazīvā resnās zarnas adenokarcinoma sākas plānā audu slānī uz resnās zarnas iekšējās virsmas, ko sauc par gļotādas, invāzija ir definēta kā vēža šūnu izplatīšanās citos audu slāņos resnajā zarnā vai citos orgānos ārpus resnās zarnas. Invāziju var redzēt tikai pēc tam, kad patologs ir izmeklējis audzēju mikroskopā.
Pārbaudot audzēju zem mikroskopa, jūsu patologs redzēs, cik tālu vēža šūnas ir izplatījušās no gļotādas apkārtējos audos. To sauc par iebrukuma dziļumu vai līmeni. Invāzijas dziļums ir svarīgs, jo audzēji, kas iekļūst dziļāk resnās zarnas sieniņās, visticamāk izplatīsies uz citām ķermeņa daļām, piemēram, limfmezgli, aknas vai plaušas. Invāzijas līmeni izmanto arī, lai noteiktu patoloģiskā audzēja stadiju (pT). Zemāk esošie attēli parāda saistību starp invāzijas dziļumu un patoloģiskā audzēja stadiju.
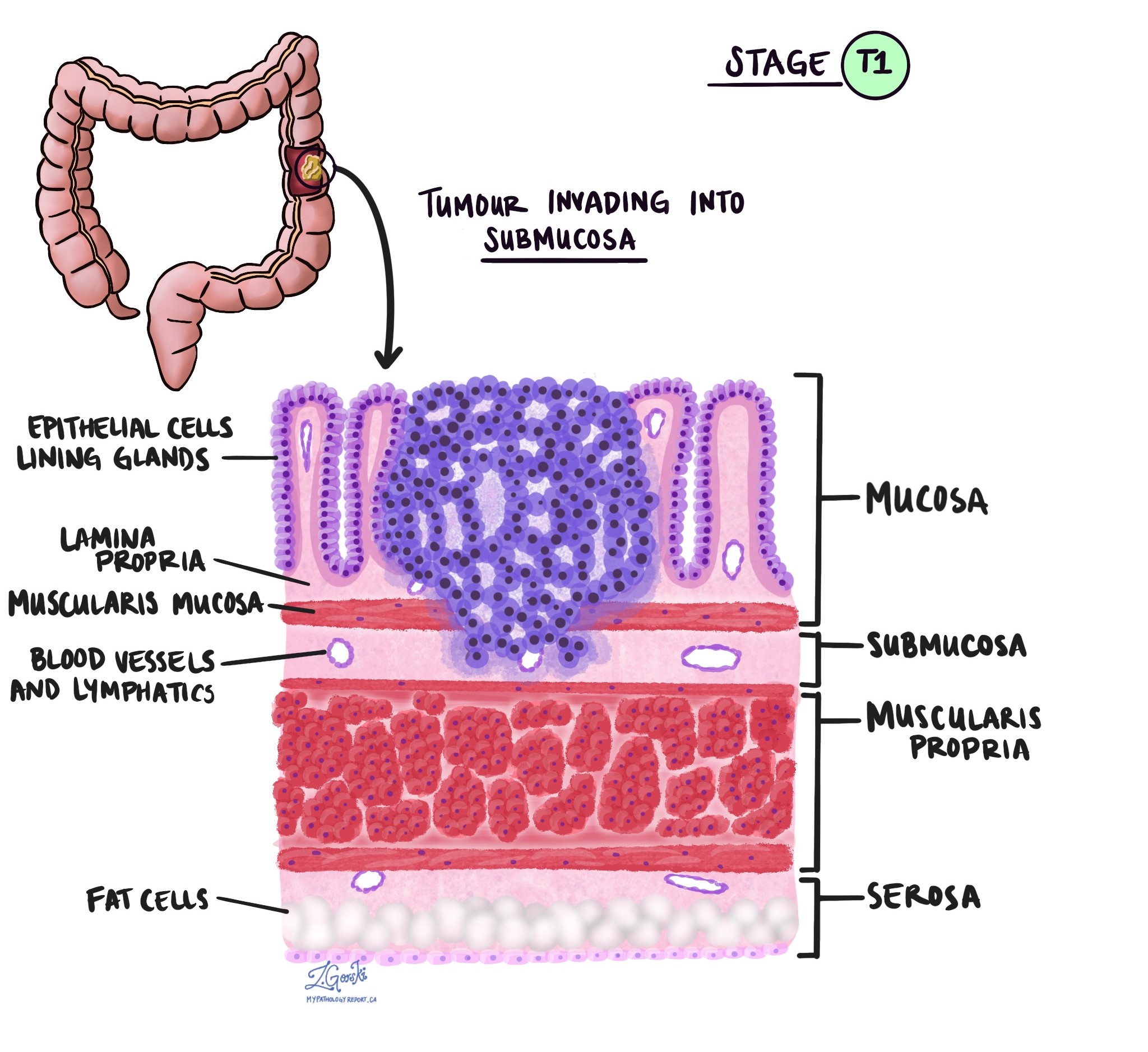
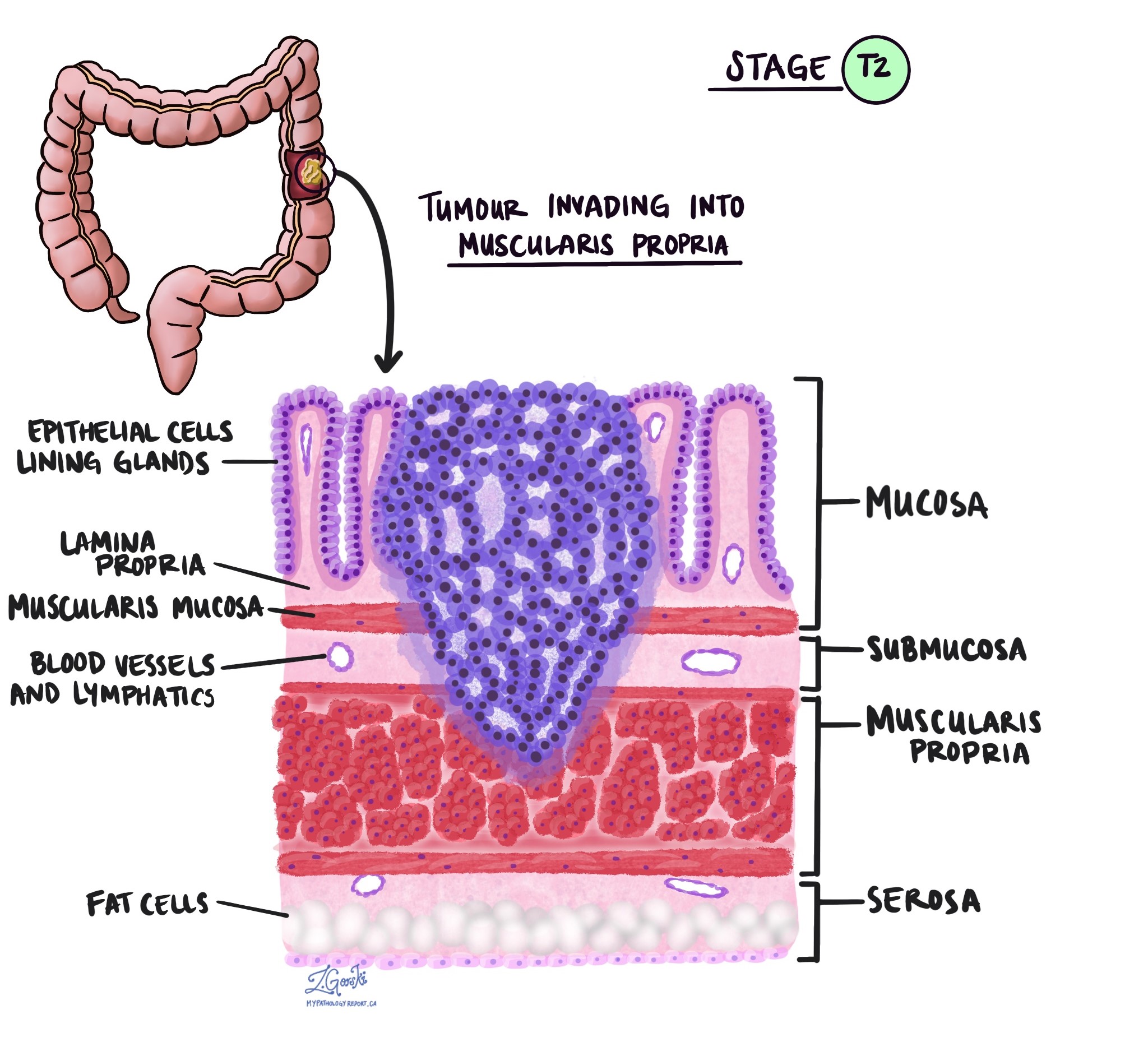
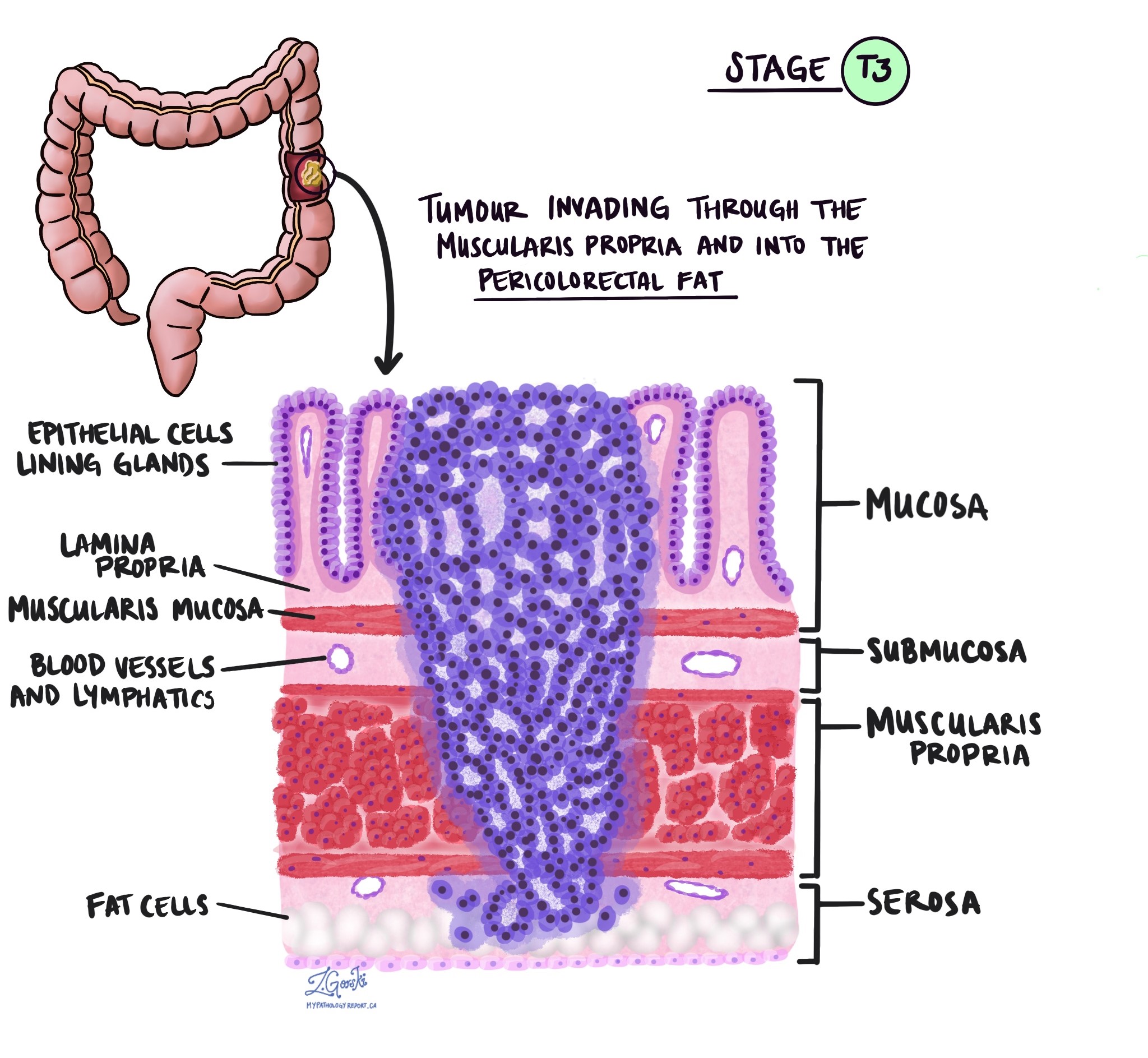
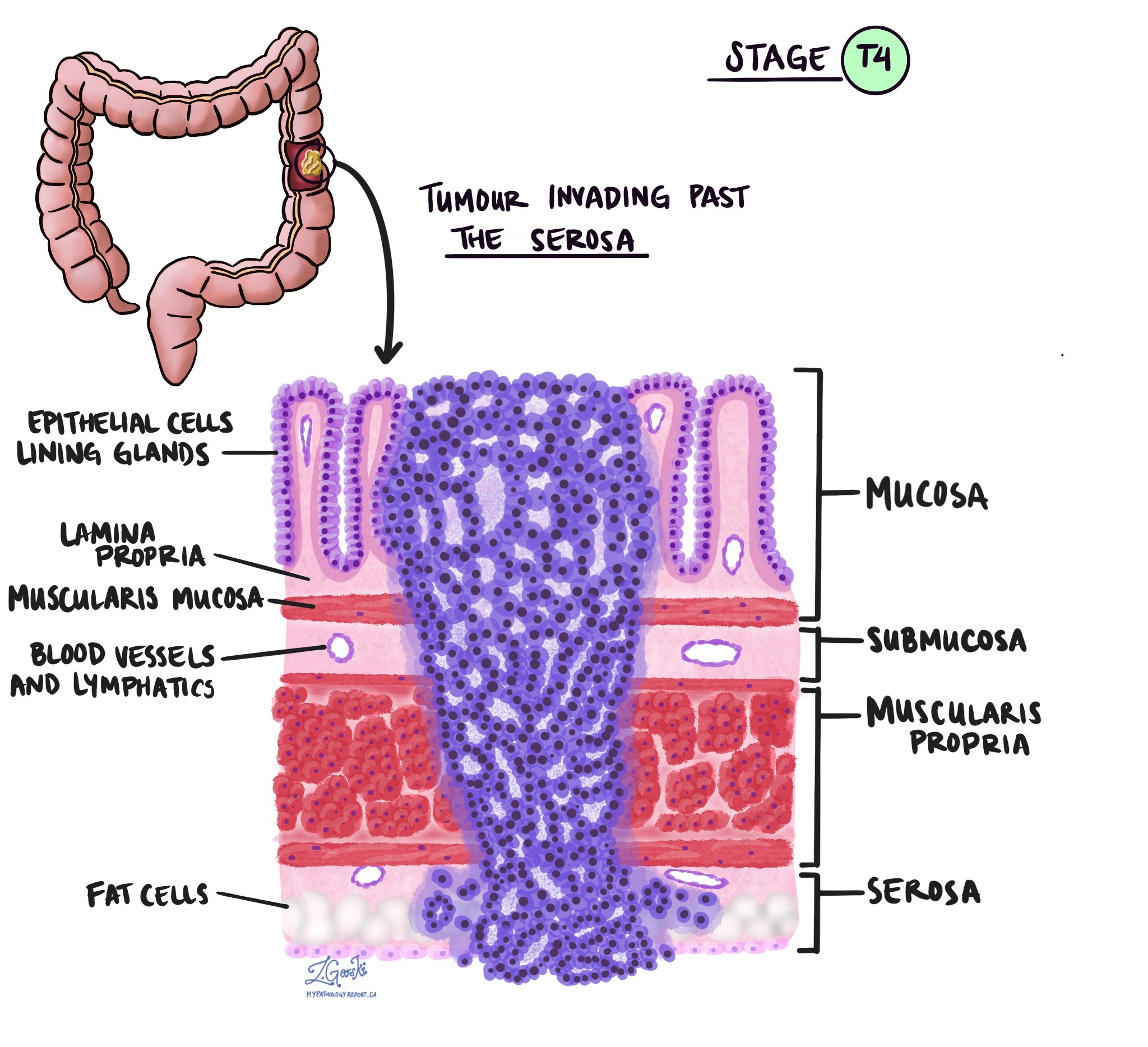
Perineirālā invāzija
Patologi lieto terminu "perineirāla invāzija", lai aprakstītu situāciju, kad vēža šūnas pievienojas nervam vai iekļūst tajā. "Intraneirālā invāzija" ir saistīts termins, kas īpaši attiecas uz vēža šūnām, kas atrodas nerva iekšpusē. Nervi, kas atgādina garus vadus, sastāv no šūnu grupām, kas pazīstamas kā neironi. Šie nervi, kas atrodas visā ķermenī, pārraida tādu informāciju kā temperatūra, spiediens un sāpes starp ķermeni un smadzenēm. Perineirālās invāzijas klātbūtne ir svarīga, jo tā ļauj vēža šūnām pārvietoties pa nervu tuvējos orgānos un audos, palielinot audzēja atkārtošanās risku pēc operācijas.
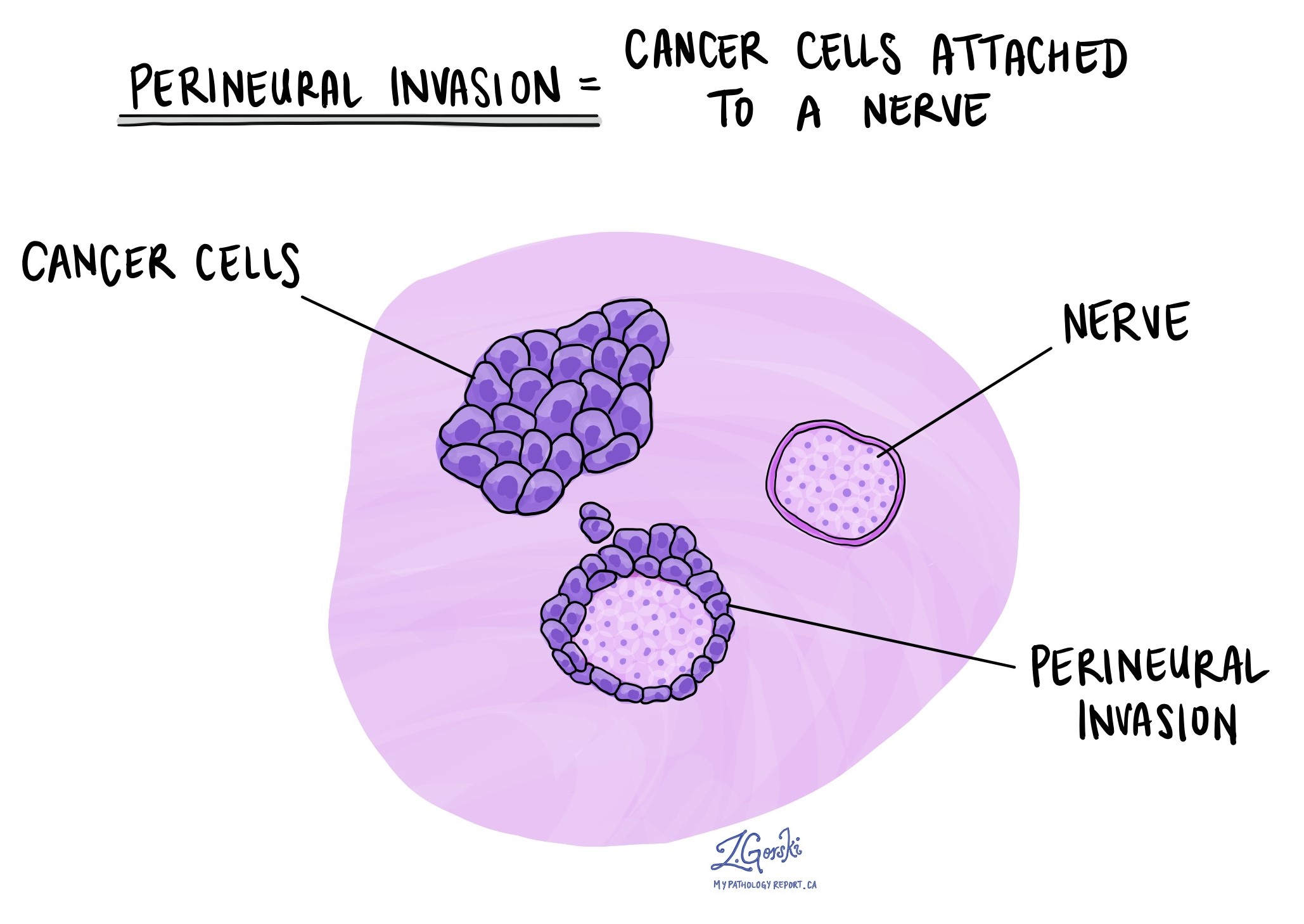
Limfovaskulāra invāzija
Limfovaskulāra invāzija rodas, kad vēža šūnas iekļūst asinsvadā vai limfātiskā traukā. Asinsvadi ir plānas caurules, kas pārvadā asinis visā ķermenī, turpretim limfātiskie asinsvadi asiņu vietā pārvadā šķidrumu, ko sauc par limfu. Šie limfātiskie asinsvadi savienojas ar maziem imūnsistēmas orgāniem, kas izkaisīti visā ķermenī, kas pazīstami kā limfmezgli.
Limfovaskulāra invāzija ir svarīga, jo tā ļauj vēža šūnām caur asinīm vai limfātiskajiem asinsvadiem izplatīties citās ķermeņa daļās, tostarp limfmezglos vai aknās. Turklāt vēža šūnu klātbūtne lielā vēnā aiz resnās zarnas sienas (ārpus biezā muskuļu saišķa) ir saistīta ar lielu risku, ka vēža šūnas galu galā tiks atrastas aknās.

Maržas
Patoloģijā robeža ir audu mala, kas noņemta audzēja operācijas laikā. Piemales statuss patoloģijas ziņojumā ir svarīgs, jo tas norāda, vai viss audzējs tika noņemts vai daži tika atstāti. Šī informācija palīdz noteikt turpmākas ārstēšanas nepieciešamību.
Patologi parasti novērtē robežas pēc tādas ķirurģiskas procedūras kā izgriešana or rezekcija, kuras mērķis ir noņemt visu audzēju. Rezerves parasti netiek novērtētas pēc a biopsija, kas noņem tikai daļu audzēja. Paziņoto malu skaits un to lielums — cik daudz normālu audu atrodas starp audzēju un griezuma malu — atšķiras atkarībā no audu veida un audzēja atrašanās vietas.
Patologi pārbauda malas, lai pārbaudītu, vai audu griezuma malās nav audzēja šūnas. Pozitīva robeža, kur tiek atrastas audzēja šūnas, liecina, ka kāds vēzis var palikt organismā. Turpretim negatīva robeža bez audzēja šūnām malā liecina, ka audzējs ir pilnībā noņemts. Dažos ziņojumos tiek mērīts arī attālums starp tuvākajām audzēja šūnām un robežu, pat ja visas robežas ir negatīvas.

Audzēja veidošanās
Audzēja veidošanās ir termins, ko patologi lieto, lai aprakstītu atsevišķas vēža šūnas vai nelielas vēža šūnu grupas, kas redzamas audzēja malās. Tiek uzskatīts, ka tā ir pazīme, ka audzējs kļūst mazāk diferencēts. Pamatojoties uz mikroskopā redzamo pumpuru skaitu, tiek piešķirts vērtējums – zems, vidējs vai augsts. Augsts rādītājs ir saistīts ar paaugstinātu risku, ka vēža šūnas izplatīsies citā ķermeņa daļā.
Ārstēšanas efekts
Ja pirms audzēja noņemšanas saņēmāt vēža ārstēšanu (ķīmijterapiju vai staru terapiju, vai abus), patologs rūpīgi pārbaudīs audu zonu, kurā audzējs iepriekš tika identificēts, lai noskaidrotu, vai vēža šūnas joprojām ir dzīvas (dzīvotspējīgas). Visbiežāk izmantotā sistēma apraksta ārstēšanas efektu skalā no 0 līdz 3, kur 0 nozīmē, ka nav dzīvotspējīgu vēža šūnu (visas vēža šūnas ir mirušas) un 3 ir plašs atlikušais vēzis bez redzamas audzēja regresijas (visi vai lielākā daļa no tiem vēža šūnas ir dzīvas).
Audzēja nogulsnes
Audzēja nogulsnes ir vēža šūnu grupa, kas ir atsevišķas no galvenā audzēja, bet nav a limfmezgls. Audzēja nogulsnes ir saistītas ar lielāku risku, ka audzēja šūnas pēc ārstēšanas izplatīsies citā ķermeņa daļā, piemēram, aknās vai plaušās. Audzēja nogulsnes nosaka arī patoloģiskā audzēja stadiju (pT).
Limfmezgli
Mazie imūnsistēmas orgāni, kas pazīstami kā limfmezgli, atrodas visā ķermenī. Vēža šūnas var pārvietoties no audzēja uz šiem limfmezgliem caur sīkiem limfātiskajiem asinsvadiem. Šī iemesla dēļ ārsti bieži noņem un mikroskopiski pārbauda limfmezglus, lai meklētu vēža šūnas. Šo procesu, kurā vēža šūnas pārvietojas no sākotnējā audzēja uz citu ķermeņa daļu, piemēram, limfmezglu, sauc metastāzes.
Vēža šūnas parasti vispirms migrē uz limfmezgliem pie audzēja, lai gan var tikt ietekmēti arī attālie limfmezgli. Līdz ar to ķirurgi parasti vispirms noņem limfmezglus, kas ir vistuvāk audzējam. Tie var noņemt limfmezglus tālāk no audzēja, ja tie ir palielināti un pastāv nopietnas aizdomas, ka tie satur vēža šūnas.
Patologi mikroskopā pārbaudīs visus noņemtos limfmezglus, un konstatējumi tiks detalizēti aprakstīti jūsu ziņojumā. "Pozitīvs" rezultāts norāda uz vēža šūnu klātbūtni limfmezglā, savukārt "negatīvs" rezultāts nozīmē, ka vēža šūnas nav atrastas. Ja ziņojumā tiek atrastas vēža šūnas limfmezglos, tajā var norādīt arī šo šūnu lielākās kopas lielumu, ko bieži dēvē par “fokusu” vai “noguldījumu”. Ekstranodāls pagarinājums rodas, kad audzēja šūnas iekļūst limfmezgla ārējā kapsulā un izplatās blakus audos.
Limfmezglu pārbaude ir svarīga divu iemeslu dēļ. Pirmkārt, tas palīdz noteikt patoloģiskā mezgla stadiju (pN). Otrkārt, vēža šūnu atklāšana limfmezglos liecina par paaugstinātu risku vēlāk atrast vēža šūnas citās ķermeņa daļās. Šī informācija palīdz ārstam izlemt, vai jums ir nepieciešama papildu ārstēšana, piemēram, ķīmijterapija, staru terapija vai imūnterapija.
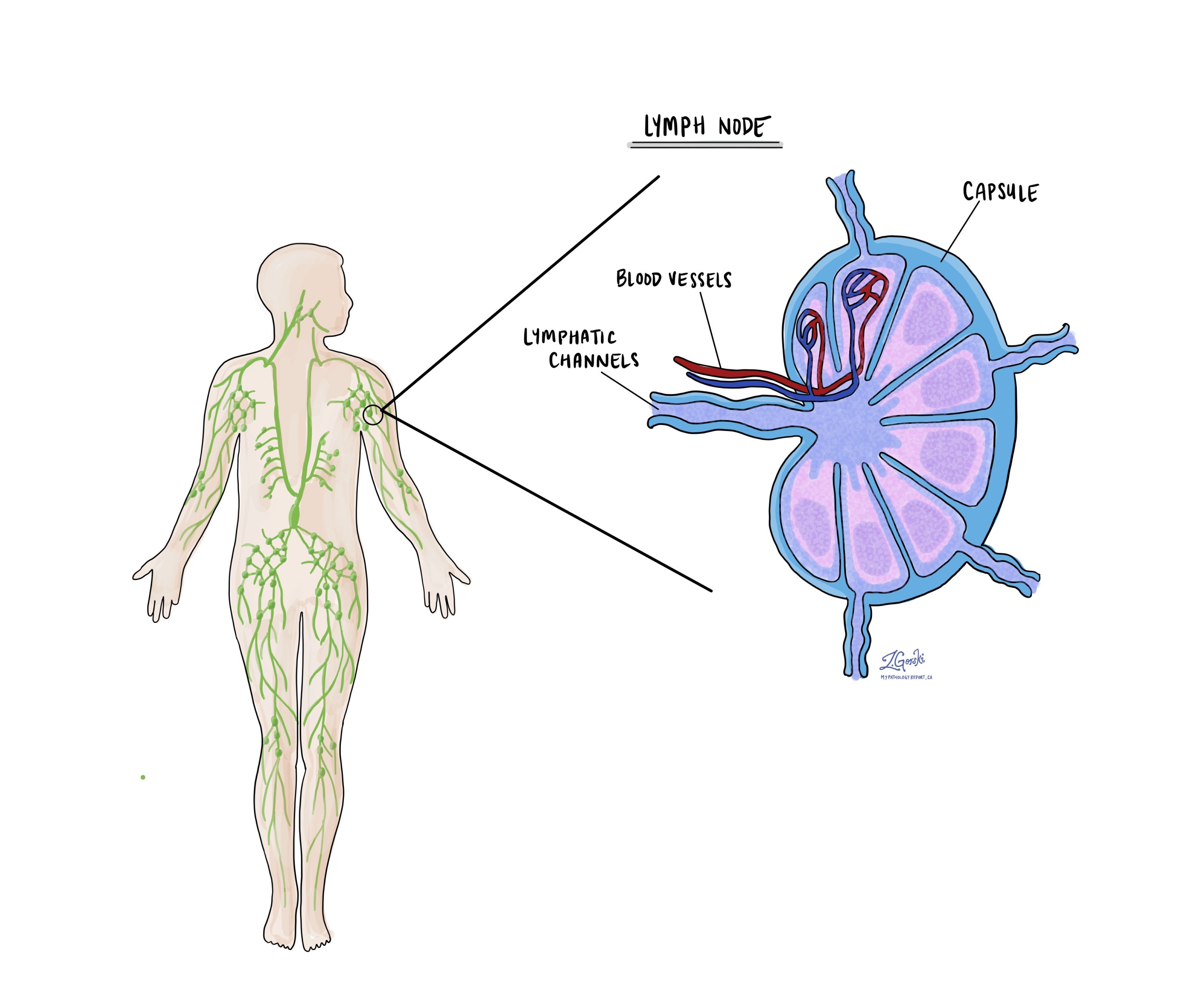
Nesakritības labošanas proteīni
Nesakritības labošana (MMR) ir sistēma visās normālās, veselajās šūnās, kas novērš kļūdas mūsu ģenētiskajā materiālā (DNS). Sistēma sastāv no dažādiem proteīniem, un četri visizplatītākie ir MSH2, MSH6, MLH1 un PMS2.
Četri nesakritības labošanas proteīni MSH2, MSH6, MLH1 un PMS2 darbojas pa pāriem, lai fiksētu bojāto DNS. Konkrēti, MSH2 darbojas ar MSH6, un MLH1 darbojas ar PMS2. Ja tiek zaudēts viens proteīns, pāris nevar normāli funkcionēt, un palielinās vēža attīstības risks.
Kā patologi pārbauda neatbilstības labošanas proteīnus?
Visizplatītākais veids, kā pārbaudīt neatbilstības labošanas proteīnus, ir imūnhistoķīmija. Šis tests ļauj patologiem noskaidrot, vai audzēja šūnas ražo visus četrus nesakritības labošanas proteīnus. Šī testa rezultāti parasti tiek ziņoti šādi:
- Normāls rezultāts: saglabāta proteīna ekspresija.
- Nenormāls rezultāts: olbaltumvielu ekspresijas zudums.
Kāpēc ir svarīgi pārbaudīt neatbilstības labošanas proteīnus?
Neatbilstības novēršanas pārbaude ir svarīga, jo tā var palīdzēt paredzēt, cik labi var darboties noteiktas ārstēšanas metodes. Piemēram, vēzis ar neatbilstības labošanas proteīna ekspresijas zudumu, visticamāk, reaģēs uz imūnterapijas ārstēšanu, piemēram, PD-1 vai PD-L1 inhibitoriem. Tas ir tāpēc, ka lielais mutāciju skaits, kas bieži sastopams deficītos audzējos, var radīt jaunus antigēnus, kas padara audzēju redzamāku un neaizsargātāku pret imūnsistēmu.
Tiek veikta arī neatbilstības novēršanas pārbaude, lai identificētu pacientus, kuriem var būt Linča sindroms, kas pazīstams arī kā iedzimts nepolipozes kolorektālais vēzis (HNPCC). Linča sindroms ir ģenētiska slimība, kas palielina risku saslimt ar dažāda veida vēzi, tostarp barības vada vēzi, resnās zarnas vēzi, endometrija vēzi, olnīcu vēzi un kuņģa vēzi.
Citas ģenētiskas izmaiņas, kas konstatētas invazīvā resnās un taisnās zarnas adenokarcinomā
- APC (Adenomatous Polyposis Coli) gēnu mutācijas: gandrīz visuresošas sporādiskos resnās zarnas vēža gadījumos, mutācijas APC gēnā bieži ir agrīns notikums kolorektālā vēža attīstībā. APC gēns ir audzēja supresora gēns, un tā inaktivācija izraisa patoloģisku šūnu augšanu.
- KRAS un NRAS mutācijas: mutācijas KRAS un NRAS gēnos, kas ir daļa no RAS gēnu saimes, rodas aptuveni 40–45% kolorektālā vēža gadījumu. Šīs mutācijas izraisa nekontrolētu šūnu dalīšanos un augšanu. Īpaši KRAS mutāciju klātbūtne ir saistīta ar rezistenci pret noteiktām anti-EGFR (epidermas augšanas faktora receptoru) terapijām.
- BRAF mutācijas: BRAF gēna mutācija, īpaši V600E, tiek konstatēta aptuveni 10% kolorektālā vēža gadījumu. Tas bieži ir saistīts ar sliktu prognozi un rezistenci pret dažām terapijām. BRAF mutācijas ir biežāk sastopamas vēža veidos, kas attīstījušies zobainā ceļā.
- PIK3CA mutācijas: mutācijas PIK3CA gēnā, kas kodē fosfatidilinozīta 3-kināzes (PI3K) apakšvienību, rodas aptuveni 10–20% kolorektālā vēža gadījumu. Šīs mutācijas var aktivizēt AKT signalizācijas ceļu, veicinot šūnu proliferāciju un izdzīvošanu.
Testi, ko izmanto, lai noteiktu ģenētiskās izmaiņas
- Nākamās paaudzes sekvencēšana (NGS): NGS ļauj vienlaikus pārbaudīt vairākus gēnus, lai noteiktu mutācijas, dzēšanas un amplifikācijas. Šī visaptverošā pieeja var novērtēt visas parastās ģenētiskās izmaiņas kolorektālā vēža gadījumā, tostarp APC, KRAS, NRAS, BRAF un PIK3CA mutācijas.
- Polimerāzes ķēdes reakcija (PCR): šī metode pastiprina DNS segmentus, ļaujot analizēt specifiskas ģenētiskas izmaiņas, piemēram, KRAS, NRAS un BRAF mutācijas.
- Fluorescences in situ hibridizācija (FISH): FISH var identificēt ģenētiskas novirzes, piemēram, amplifikācijas vai dzēšanas konkrētos gēnos. To retāk izmanto, lai regulāri noteiktu minētās ģenētiskās izmaiņas, bet var būt noderīga konkrētos kontekstos.
Par šo rakstu
Ārsti uzrakstīja šo rakstu, lai palīdzētu jums izlasīt un izprast jūsu patoloģijas ziņojumu. Sazināties ar mums ja jums ir jautājumi par šo rakstu vai jūsu patoloģijas ziņojumu. Lai iegūtu pilnīgu ievadu patoloģijas ziņojumā, izlasiet šis raksts.