Par Jason Wasserman, MD, PhD, FRCPC et Matt Cecchini, MD, PhD, FRCPC
27 novembre 2025
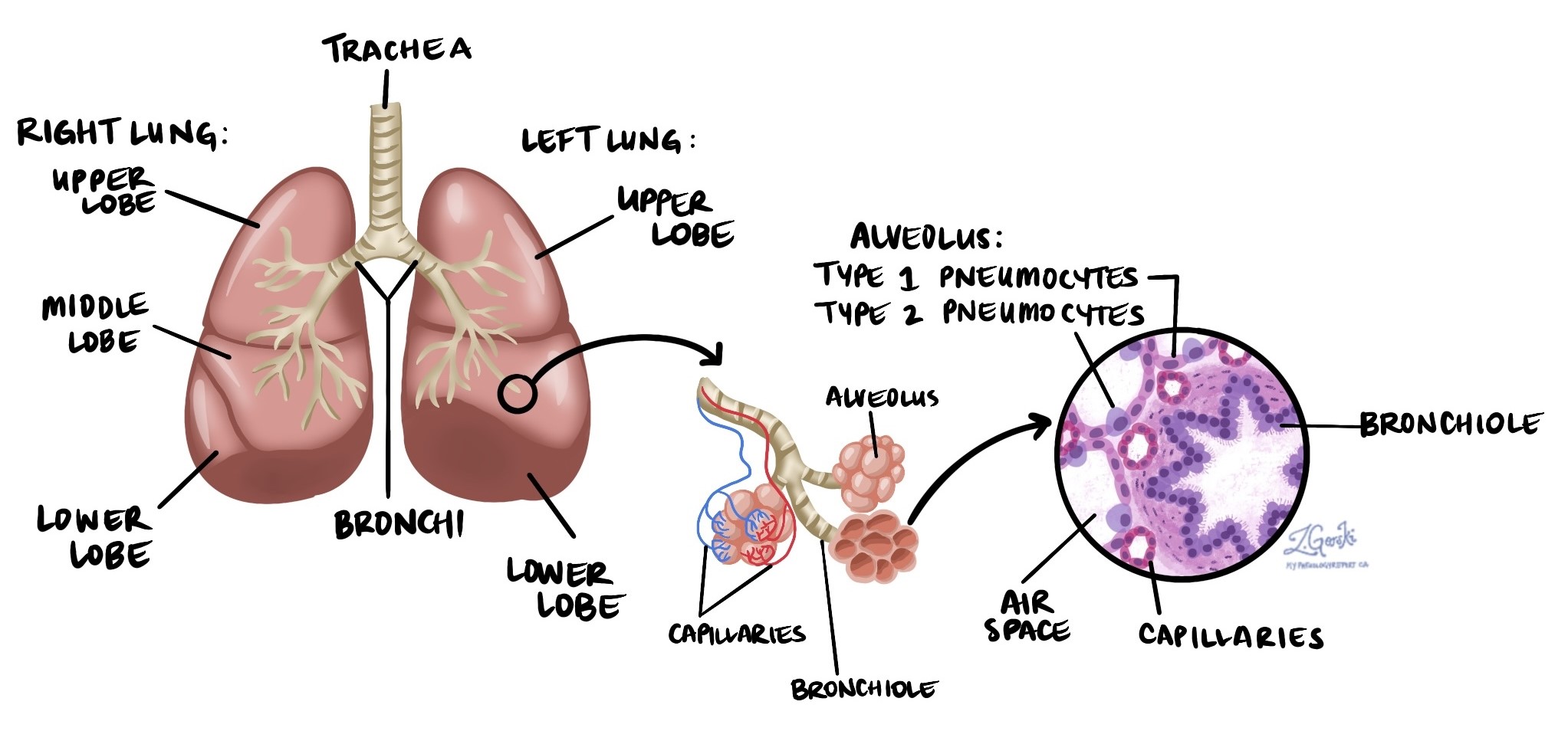
Adénocarcinome est le type de cancer du poumon le plus fréquent, représentant environ 40 % de tous les cas de cancer du poumon en Amérique du Nord. Il appartient au groupe des cancers connus sous le nom de cancer du poumon non à petites cellules (NSCLC)L'adénocarcinome se développe à partir des pneumocytes, cellules spécialisées qui tapissent les minuscules sacs d'air des poumons appelés alvéoles. C'est au niveau des alvéoles que l'oxygène pénètre dans le sang et que le dioxyde de carbone est éliminé.
L’adénocarcinome débutant souvent près des bords extérieurs du poumon, il peut être détecté précocement grâce à des examens d’imagerie – tels que les radiographies ou les tomodensitométries – qui révèlent un petit nodule ou une masse.
Qu'est-ce qui cause l'adénocarcinome dans le poumon?
La principale cause d'adénocarcinome pulmonaire est le tabagisme. Cela inclut les cigarettes, les cigares et la pipe. Cependant, l'adénocarcinome peut également survenir chez des personnes n'ayant jamais fumé.
Parmi les autres causes et facteurs de risque, on peut citer :
-
Exposition au radon.
-
Expositions professionnelles, telles que l'amiante, la silice ou les gaz d'échappement diesel.
-
Pollution de l'air extérieur.
Ces facteurs peuvent endommager les cellules pulmonaires et augmenter le risque de cancer au fil du temps.
Quels sont les symptômes de l'adénocarcinome pulmonaire ?
Les symptômes de l'adénocarcinome pulmonaire sont variables. Certaines personnes ne présentent aucun symptôme, surtout aux premiers stades. Lorsque des symptômes apparaissent, ils peuvent inclure :
-
Une toux persistante ou qui s’aggrave.
-
Tousser du sang.
-
Douleur thoracique.
-
Essoufflement.
-
Fatigue ou perte de poids involontaire.
Si le cancer se propage à d'autres parties du corps, les symptômes dépendent de sa localisation. Par exemple, la propagation aux os peut provoquer des douleurs, voire une fracture pathologique, c'est-à-dire une fracture osseuse causée par l'affaiblissement du tissu osseux dû au cancer.
Quelles conditions sont associées à l'adénocarcinome du poumon ?
L'adénocarcinome du poumon peut survenir à partir d'affections précancéreuses telles que :
-
L'hyperplasie adénomateuse atypique (HAA) est une affection dans laquelle les cellules tapissant les alvéoles ont une apparence anormale mais ne sont pas cancéreuses.
-
Adénocarcinome in situ (AIS) il s'agit d'un cancer non invasif limité à la surface interne des alvéoles et de taille inférieure à 3 cm.
L'AIS peut évoluer en adénocarcinome invasif lorsque la tumeur dépasse 3 cm ou lorsque les cellules cancéreuses envahissent le tissu de soutien situé sous la paroi alvéolaire.
Comment ce diagnostic est-il établi ?
Le diagnostic d'adénocarcinome débute lorsque les examens d'imagerie révèlent une zone suspecte dans le poumon. Pour confirmer le diagnostic, un biopsie Un prélèvement de tissu est effectué pour obtenir un petit échantillon. Les biopsies peuvent être réalisées par ponction à l'aiguille fine, bronchoscopie, échographie endobronchique (EBUS) ou cytoponction à l'aiguille fine (FNA). L'échantillon est ensuite examiné au microscope par un anatomopathologiste, médecin spécialiste du diagnostic des maladies par l'étude des tissus.
Si le cancer est confirmé, une intervention chirurgicale peut être recommandée pour retirer la tumeur. Le type d'intervention dépend de la taille et de la localisation de la tumeur. Les petites tumeurs proches de la surface peuvent être retirées par résection cunéiforme, tandis que les tumeurs plus volumineuses ou plus centrales peuvent nécessiter une lobectomie, voire une pneumonectomie.
Après l'exérèse, le pathologiste examine la tumeur dans son intégralité. Les caractéristiques importantes comprennent :
-
Le mode de croissance (type histologique).
-
Si le cancer s'est propagé aux tissus pulmonaires environnants.
-
Qu'il soit propagé par voie aérienne (STAS) est présent.
-
Que les cellules tumorales aient pénétré dans les vaisseaux sanguins ou les canaux lymphatiques.
-
Si la tumeur s'est étendue à la plèvre.
-
Si les marges chirurgicales sont saines.
-
Si les ganglions lymphatiques contiennent des cellules cancéreuses.
Immunohistochimie (IHC)
Immunohistochimie Il s'agit d'un test spécial qui utilise des anticorps liés à des colorants pour détecter des protéines spécifiques au sein des cellules. Ces protéines agissent comme des « marqueurs » qui aident le pathologiste à confirmer le type de cancer et à déterminer son point d'origine.
L'adénocarcinome du poumon présente généralement les résultats suivants :
-
TTF-1 : Positif.
-
p40 : Négatif.
-
CK5 : Négatif.
-
Chromogranine : Négatif.
-
Synaptophysine : Négatif.
Ce type de coloration confirme le diagnostic et permet d'exclure d'autres types de cancer du poumon tels que le carcinome épidermoïde ou les tumeurs neuroendocrines.
Types histologiques d'adénocarcinome
L'adénocarcinome pulmonaire est classé en types histologiques selon le mode de croissance des cellules cancéreuses. Une tumeur peut présenter un ou plusieurs types histologiques.
type lépidique
Les cellules cancéreuses se développent le long de la surface interne des alvéoles. Si la tumeur est complètement lépidique et mesure moins de 3 cm, elle est classée comme AIS.
Type acinaire
Les cellules tumorales forment des structures rondes, semblables à des glandes.
Type solide
Les cellules tumorales se développent en nappes denses, avec peu d'espace libre. Ce type de tumeur est plus agressif.
Type papillaire
Les cellules tumorales forment des projections en forme de doigts appelées papilles.
Type micropapillaire
Les cellules tumorales forment de minuscules amas qui ressemblent à des touffes. Il s'agit d'un schéma très agressif.
Taux de tumeur
Dans le cas d'un adénocarcinome pulmonaire, le grade tumoral décrit l'agressivité apparente du cancer au microscope. Ce grade repose sur deux caractéristiques microscopiques :
-
Le profil histologique prédominant.
-
Le schéma le plus grave (le plus agressif) observé dans toute la tumeur.
Les tumeurs à prédominance lépidique et présentant peu de composantes solides ou micropapillaires sont bien différenciées, ce qui signifie qu'elles croissent plus lentement et ont un meilleur pronostic. Les tumeurs à croissance acineuse ou papillaire et présentant de faibles composantes agressives sont modérément différenciées. Les tumeurs présentant une composante solide ou micropapillaire importante sont peu différenciées, ce qui signifie qu'elles sont plus agressives, croissent plus rapidement et ont un risque accru de métastases.
Le grade tumoral est l'un des facteurs prédictifs les plus importants du pronostic, notamment dans les cas de maladie à un stade précoce.
Diffusion dans les espaces aériens (STAS)
Le terme STAS désigne la présence de cellules cancéreuses flottant dans les espaces aériens du poumon, au-delà de la limite de la tumeur principale. Ces cellules sont distinctes de la masse primaire et peuvent se déplacer à travers les petits canaux aériens du poumon.
La présence de STAS est associée à un risque accru de récidive, notamment après une chirurgie limitée comme la résection cunéiforme. C'est pourquoi la recherche de STAS est systématiquement mentionnée dans le compte rendu d'anatomopathologie et contribue à orienter les décisions thérapeutiques.
Tumeurs multiples
Il est possible de trouver plusieurs tumeurs dans les poumons. Dans ce cas, chaque tumeur est examinée séparément. Parfois, la présence de plusieurs tumeurs résulte de la propagation d'une seule tumeur primitive, notamment lorsqu'elles sont identiques au microscope. Lorsque de petites excroissances secondaires apparaissent dans le même poumon que la tumeur primitive, on les appelle souvent nodules ; il s'agit de petites lésions arrondies pouvant correspondre à une dissémination métastatique intrapulmonaire.
Dans d'autres cas, les tumeurs peuvent s'être formées indépendamment, notamment si elles présentent des caractéristiques histologiques différentes. Par exemple, une tumeur peut être un adénocarcinome tandis qu'une autre est un carcinome épidermoïde. Lorsque les tumeurs se développent séparément, elles sont considérées comme des cancers primitifs distincts et non comme des métastases. Il est important de faire la distinction entre ces deux possibilités car cela influence la stadification, le traitement et le pronostic.
Invasion pleurale
La plèvre est une membrane fine composée de deux couches :
-
La plèvre viscérale recouvre la surface des poumons.
-
La plèvre pariétale, qui tapisse l'intérieur de la cavité thoracique.
L'invasion pleurale signifie que les cellules cancéreuses se sont propagées dans l'une ou les deux couches de la plèvre. Les tumeurs qui envahissent uniquement la plèvre viscérale sont considérées comme localement plus avancées que celles limitées au tissu pulmonaire. Les tumeurs qui envahissent la plèvre pariétale (la couche externe attachée à la paroi thoracique) sont considérées comme encore plus avancées, car le cancer s'est étendu au-delà du poumon et a atteint la plèvre, qui tapisse la cavité thoracique. L'invasion pleurale augmente le stade T et est associée à un risque accru de propagation et de récidive.
Invasion lymphovasculaire
L’invasion lymphovasculaire (ILV) se produit lorsque des cellules cancéreuses pénètrent dans les vaisseaux sanguins ou lymphatiques situés dans ou à proximité de la tumeur. Ces vaisseaux servent de voies de dissémination au cancer vers d’autres parties du corps, notamment les ganglions lymphatiques, les os, le foie ou le cerveau. En cas d’invasion lymphovasculaire, le risque de métastases est plus élevé et un traitement complémentaire peut être recommandé.
Les marges
Les marges sont les bords des tissus retirés lors d'une intervention chirurgicale. Le pathologiste examine toutes les marges afin de déterminer si la tumeur a été entièrement retirée. Une marge négative signifie qu'aucune cellule cancéreuse n'est visible au niveau de la marge de résection. Une marge positive indique la présence de cellules cancéreuses, ce qui soulève des inquiétudes quant à la présence de cellules cancéreuses résiduelles. L'analyse des marges aide les médecins à décider si une intervention chirurgicale ou une radiothérapie supplémentaire est nécessaire.

Ganglions
Ganglions Ce sont de petits organes immunitaires qui filtrent la lymphe. L'adénocarcinome pulmonaire se propage fréquemment aux ganglions lymphatiques du poumon et de la région centrale du thorax. Lors d'une intervention chirurgicale, des ganglions lymphatiques provenant de régions anatomiques spécifiques (appelées stations ganglionnaires) peuvent être prélevés et examinés.
Le rapport d'anatomopathologie précisera le nombre de ganglions lymphatiques examinés, leur localisation et la présence ou non de cellules cancéreuses. Ces informations permettent de déterminer le stade ganglionnaire et sont essentielles au choix du traitement.

Stade pathologique (pTNM)
L’adénocarcinome pulmonaire est classé selon le système TNM :
-
Le stade T décrit la taille de la tumeur et indique si elle a envahi les structures voisines.
-
Le stade N indique si les ganglions lymphatiques contiennent des cellules cancéreuses.
-
Le stade M indique si le cancer s'est propagé à des organes distants tels que le cerveau, les os ou le foie.
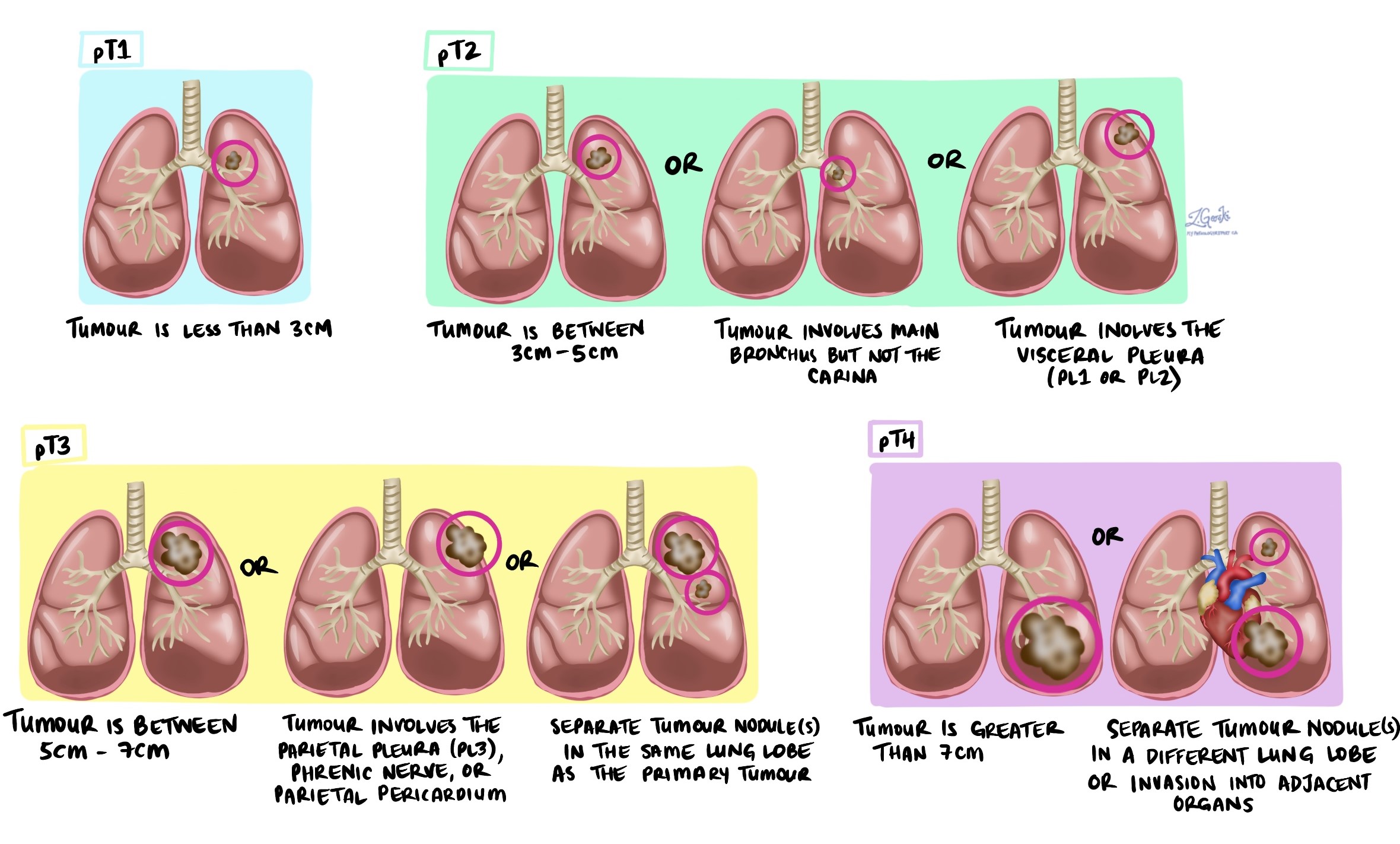
Stade tumoral (pT)
-
T1 : La tumeur mesure 3 cm ou moins.
-
T2 : La tumeur mesure plus de 3 cm mais pas plus de 5 cm, ou elle a envahi la plèvre viscérale ou les voies respiratoires centrales.
-
T3 : La tumeur mesure plus de 5 cm mais pas plus de 7 cm ou s'est étendue aux tissus voisins.
-
T4 : La tumeur mesure plus de 7 cm ou a envahi des organes voisins tels que le cœur ou l’œsophage.
Stade nodal (pN)
-
NX : Les ganglions lymphatiques n’ont pas été examinés.
-
N0 : Aucune cellule cancéreuse dans les ganglions lymphatiques.
-
N1 : Cellules cancéreuses dans les ganglions lymphatiques à l'intérieur du poumon ou près des voies respiratoires (stations 10 à 14).
-
N2 : Cellules cancéreuses dans les ganglions lymphatiques de la partie centrale du thorax près des voies respiratoires (stations 7 à 9).
-
N3 : Cellules cancéreuses dans les ganglions lymphatiques du côté opposé de la poitrine ou dans la partie inférieure du cou (stations 1 à 6).
Les stades plus avancés présentent un risque plus élevé de propagation et de récidive et nécessitent souvent un traitement plus intensif.
Biomarqueurs de l'adénocarcinome du poumon
Les biomarqueurs sont des modifications mesurables dans les cellules cancéreuses, impliquant souvent des gènes ou des protéines spécifiques. Ces modifications aident les médecins à comprendre le comportement de la tumeur et à déterminer les traitements les plus efficaces. Dans l'adénocarcinome pulmonaire, les biomarqueurs sont particulièrement importants car de nombreuses tumeurs présentent des altérations génétiques qui peuvent être ciblées par des thérapies bloquant les signaux anormaux favorisant la croissance du cancer. L'analyse des biomarqueurs est désormais une étape standard du diagnostic et oriente de nombreuses décisions thérapeutiques.
Quels types de biomarqueurs sont testés dans l'adénocarcinome pulmonaire ?
La plupart des tests de biomarqueurs pour l'adénocarcinome pulmonaire se concentrent sur les mutations génétiques et les réarrangements géniques présents dans l'ADN tumoral. Ces altérations sont détectées grâce à des techniques de laboratoire spécialisées telles que la PCR (un test qui amplifie de petits fragments d'ADN), le séquençage de nouvelle génération (SNG, un test qui analyse simultanément de nombreux gènes) et la FISH (un test qui utilise des sondes fluorescentes pour détecter les réarrangements géniques). Ces tests sont réalisés sur des prélèvements biopsiques ou sur la tumeur retirée chirurgicalement et jouent un rôle essentiel dans le choix des traitements les plus susceptibles d'être efficaces.
EGFR
L'EGFR est un gène codant pour un récepteur qui contrôle la croissance cellulaire. Lorsque l'EGFR présente certaines mutations, le récepteur devient hyperactif, favorisant ainsi la croissance tumorale. Les mutations de l'EGFR sont fréquentes chez les non-fumeurs, les femmes et les personnes d'origine est-asiatique. Ces mutations sont importantes car les tumeurs présentant des altérations de l'EGFR répondent souvent très bien aux thérapies ciblées contre l'EGFR, qui bloquent le signal de croissance anormal et peuvent réduire la taille de la tumeur ou ralentir sa progression.
Les pathologistes recherchent les mutations de l'EGFR en examinant l'ADN de la tumeur par PCR ou séquençage de nouvelle génération afin de détecter des modifications génétiques spécifiques.
Votre rapport d'anatomopathologie décrira la tumeur comme EGFR-positive si une mutation est détectée et EGFR-négative si aucune mutation n'est trouvée.
ALK
Le gène ALK peut fusionner avec un autre gène, créant une protéine de fusion anormale qui favorise la croissance tumorale. Ces fusions ALK sont plus fréquentes chez les patients jeunes et les non-fumeurs. Les réarrangements du gène ALK sont importants car les tumeurs présentant cette altération répondent souvent exceptionnellement bien aux thérapies ciblées anti-ALK, qui bloquent la protéine de fusion anormale.
Le test ALK est réalisé par immunohistochimie, qui met en évidence la protéine ALK dans les cellules tumorales, par FISH, qui détecte les réarrangements du gène ALK, ou par séquençage de nouvelle génération, qui analyse directement le gène ALK.
Les tumeurs sont qualifiées d'ALK-positives lorsqu'un réarrangement est présent et d'ALK-négatives lorsqu'aucun réarrangement n'est constaté.
ROSX NUMX
ROS1 est un gène susceptible de subir des réarrangements, formant une protéine de fusion qui stimule la croissance tumorale. Bien que moins fréquentes que les altérations d'EGFR ou d'ALK, les fusions de ROS1 sont importantes car elles répondent très bien aux thérapies ciblées anti-ROS1, qui bloquent la protéine anormale et contribuent à contrôler le cancer.
Le test ROS1 peut être réalisé par immunohistochimie, FISH ou séquençage de nouvelle génération pour détecter une fusion du gène ROS1.
Votre tumeur sera décrite comme ROS1-positive si une fusion est détectée et comme ROS1-négative dans le cas contraire.
FRÈRE
BRAF est un gène impliqué dans la régulation de la croissance cellulaire. Certaines mutations, comme la mutation BRAF V600E, peuvent accélérer la croissance des cellules tumorales. Ces mutations sont importantes car les tumeurs présentant des altérations de BRAF peuvent répondre aux thérapies ciblées anti-BRAF, qui bloquent la voie de signalisation anormale.
Le test consiste à analyser l'ADN tumoral par PCR ou séquençage de nouvelle génération afin d'identifier les mutations spécifiques du gène BRAF.
Votre tumeur sera qualifiée de BRAF-positive si une mutation est présente et de BRAF-négative si aucune mutation n'est détectée.
MET
MET est un gène qui contribue à la régulation de la croissance cellulaire normale. Une anomalie spécifique, le saut de l'exon 14 de MET, entraîne une activation prolongée de la protéine MET, permettant ainsi aux cellules tumorales de proliférer de manière incontrôlée. Ce biomarqueur est important car les tumeurs présentant un saut de l'exon 14 de MET répondent souvent aux thérapies ciblées.
Le test MET est généralement réalisé à l'aide du séquençage de nouvelle génération pour détecter le saut de l'exon 14 du gène MET ou d'autres mutations du gène MET.
Votre tumeur sera classée comme MET-positive si une mutation du gène MET est détectée, et comme MET-négative si aucune mutation n'est trouvée.
RET
RET est un gène qui peut fusionner avec un autre gène, créant ainsi une protéine anormale qui stimule la croissance tumorale. Les fusions du gène RET sont importantes car les tumeurs présentant cette altération répondent souvent exceptionnellement bien aux thérapies ciblées contre RET.
Les fusions RET sont identifiées par séquençage de nouvelle génération ou par FISH, deux techniques capables de détecter le réarrangement anormal.
Votre tumeur sera décrite comme RET-positive si une fusion est présente et RET-négative si elle ne l'est pas.
NTRK (NTRK1, NTRK2, NTRK3)
Les gènes NTRK peuvent fusionner avec d'autres gènes, créant des protéines de fusion TRK anormales qui favorisent fortement la croissance tumorale. Bien que rares, ces fusions sont importantes car les cancers présentant des altérations des gènes NTRK montrent souvent des réponses spectaculaires et durables aux thérapies ciblées anti-TRK.
Les tests NTRK peuvent impliquer une immunohistochimie pour dépister une expression anormale de la protéine TRK, suivie d'une FISH ou d'un séquençage de nouvelle génération pour confirmer la présence d'une fusion de gènes.
Votre tumeur sera qualifiée de NTRK-positive si une fusion est détectée et de NTRK-négative si aucune fusion n'est détectée.
KRAS
Le gène KRAS est impliqué dans la régulation de la croissance et de la division cellulaires. Les mutations du gène KRAS figurent parmi les biomarqueurs les plus fréquents de l'adénocarcinome pulmonaire, notamment chez les fumeurs. Ces mutations sont importantes car elles permettent de prédire l'évolution tumorale et parce qu'une mutation spécifique, KRAS G12C, peut être traitée par de nouveaux médicaments ciblant KRAS.
Les mutations du gène KRAS sont détectées par PCR ou par séquençage de nouvelle génération pour analyser l'ADN tumoral.
Votre tumeur sera qualifiée de KRAS-positive si une mutation est identifiée et de KRAS-négative si aucune mutation n'est trouvée.
ERBB2 (HER2)
ERBB2, également connu sous le nom de HER2, est un gène susceptible de subir des mutations entraînant une signalisation anormale et la croissance tumorale. Les altérations de HER2 sont importantes car les thérapies ciblées – et les essais cliniques en cours – s'attaquent aux tumeurs présentant des mutations de HER2.
Le test HER2 est réalisé à l'aide du séquençage de nouvelle génération pour détecter les mutations ERBB2 dans l'ADN de la tumeur.
Votre tumeur sera qualifiée d'ERBB2-positive si une mutation est détectée, et d'ERBB2-négative si aucune mutation n'est détectée.
NRAS
NRAS est un gène similaire à KRAS qui intervient dans les voies de croissance cellulaire. Les mutations de NRAS sont plus fréquentes chez les fumeurs. Bien qu'il n'existe pas encore de traitements spécifiques ciblant NRAS, l'identification d'une mutation de ce gène aide les médecins à comprendre le comportement tumoral et à envisager des essais cliniques.
Le test NRAS est réalisé à l'aide du séquençage de nouvelle génération pour rechercher des mutations dans l'ADN de la tumeur.
Votre tumeur sera qualifiée de NRAS-positive si une mutation est détectée et de NRAS-négative si aucune mutation n'est trouvée.
MAP2K1 (MEK1)
MAP2K1, également appelé MEK1, est un gène impliqué dans une voie de signalisation qui régule la croissance cellulaire. Les mutations de MAP2K1 sont importantes car des thérapies ciblées sur cette voie sont à l'étude et pourraient devenir des options thérapeutiques.
Le test MAP2K1 est réalisé à l'aide du séquençage de nouvelle génération pour détecter les mutations de l'ADN tumoral.
Votre tumeur sera qualifiée de MAP2K1-positive si une mutation est identifiée et de MAP2K1-négative si aucune mutation n'est trouvée.
NRG1
Le gène NRG1 peut subir des réarrangements ou des fusions favorisant la croissance tumorale. Bien que rares, ces réarrangements sont importants car ils pourraient être sensibles aux nouvelles thérapies ciblées contre NRG1 actuellement à l'étude.
Le test NRG1 est réalisé à l'aide du séquençage de nouvelle génération pour examiner l'ADN tumoral afin de déceler une éventuelle réorganisation génique.
Votre tumeur sera décrite comme NRG1-positive si un réarrangement est détecté et comme NRG1-négative si aucun réarrangement n'est trouvé.
PD-L1
PD-L1 est une protéine présente à la surface de certaines cellules cancéreuses. Elle interagit avec les cellules immunitaires, permettant ainsi à la tumeur d'échapper au système immunitaire et d'éviter sa destruction. PD-L1 est important car les tumeurs présentant une forte expression de PD-L1 sont plus susceptibles de répondre à l'immunothérapie, un traitement qui stimule le système immunitaire pour qu'il reconnaisse et attaque les cellules cancéreuses. Les médicaments d'immunothérapie appelés inhibiteurs de PD-1 ou de PD-L1 constituent désormais le traitement standard pour de nombreux patients atteints d'adénocarcinome pulmonaire, notamment lorsque la tumeur présente des niveaux élevés de PD-L1.
Les pathologistes recherchent l'expression de PD-L1 par immunohistochimie, une méthode de laboratoire qui utilise des anticorps couplés à des colorants pour se fixer à la protéine PD-L1 et la rendre visible au microscope. Ce test permet de quantifier le nombre de cellules tumorales exprimant PD-L1 à leur surface et d'évaluer l'intensité de cette expression. Il est généralement réalisé sur un échantillon de biopsie avant le début du traitement.
Les résultats PD-L1 sont exprimés en pourcentage, représentant la proportion de cellules tumorales présentant un marquage PD-L1. On parle alors de score de proportion tumorale (TPS).
-
Un TPS <1% est considéré comme PD-L1-négatif ou très faible.
-
Un TPS de 1 à 49 % est considéré comme une expression faible à intermédiaire.
-
Un TPS de 50 % ou plus est considéré comme une expression élevée.
Certains rapports peuvent également inclure des scores pour les cellules immunitaires ou utiliser le score positif combiné (CPS), selon la méthode de test utilisée.
Après le diagnostic
Une fois votre diagnostic confirmé, votre médecin examinera le rapport d'anatomopathologie, les examens d'imagerie et votre état de santé général afin d'établir un plan de traitement personnalisé. Ce traitement peut comprendre une intervention chirurgicale, une chimiothérapie, une immunothérapie, une thérapie ciblée, une radiothérapie ou une combinaison de ces approches.
Il est important de réaliser des tests moléculaires sur votre tumeur. De nombreux adénocarcinomes pulmonaires présentent des altérations génétiques spécifiques, telles que des mutations des gènes EGFR, ALK, ROS1, KRAS ou RET, qui peuvent être ciblées par des thérapies très efficaces. Les tests moléculaires sont désormais une pratique courante et essentielle dans la prise en charge du cancer du poumon, même à un stade précoce.
Votre équipe soignante pourra également vous proposer des examens d'imagerie complémentaires pour rechercher une éventuelle propagation, des tests de fonction pulmonaire pour évaluer votre capacité pulmonaire, et des stratégies pour gérer les symptômes tels que la toux ou l'essoufflement. Un suivi après le traitement est important pour surveiller toute récidive ou l'apparition de nouveaux nodules pulmonaires.
Questions à poser à votre médecin
-
À quel stade se trouve mon cancer, et qu'est-ce que cela implique pour mon plan de traitement ?
-
A-t-on constaté une invasion pleurale, une invasion lymphovasculaire ou un STAS dans ma tumeur ?
-
Les marges chirurgicales étaient-elles claires ?
-
Le cancer s’est-il propagé à des ganglions lymphatiques ?
-
Ai-je besoin de tests moléculaires pour EGFR, ALK, KRAS ou d'autres biomarqueurs ?
-
Quels traitements recommandez-vous et quels sont leurs objectifs ?
-
Devrais-je consulter un oncologue médical, un radio-oncologue ou un chirurgien pour la suite de mes soins ?
-
Quel est le calendrier de suivi que vous recommandez après le traitement ?