Jason Wasserman MD PhD FRCPC
22 september 2023
Wat is een ductaal adenocarcinoom van de pancreas?
Ductaal adenocarcinoom (ook wel ductaal carcinoom genoemd) is de meest voorkomende vorm van pancreaskanker. Het begint in de alvleesklier vanuit gespecialiseerde cellen aan de binnenkant van kleine kanaaltjes genaamd leidingen. Ductaal adenocarcinoom kan overal langs de lengte van de alvleesklier beginnen, maar meestal betreft het het deel van de alvleesklier dat zich het dichtst bij de dunne darm bevindt (ook wel de 'kop' genoemd). Ductaal adenocarcinoom is een zeer agressieve vorm van kanker die zich snel kan verspreiden naar omliggende organen en de lever.
Wat zijn de symptomen van ductaal adenocarcinoom van de pancreas?
De symptomen van ductaal adenocarcinoom van de pancreas zijn niet-specifiek en de meeste mensen ervaren geen symptomen totdat de tumor zich buiten de pancreas heeft verspreid. Mogelijke symptomen zijn verlies van eetlust, misselijkheid, indigestie, rugpijn, vermoeidheid en onverklaarbaar gewichtsverlies. Geelzucht (het geel worden van de huid en ogen) is vaak een laat teken.
Wat veroorzaakt ductaal adenocarcinoom van de pancreas?
Er is geen enkele oorzaak voor ductaal adenocarcinoom van de alvleesklier vastgesteld. De belangrijkste risicofactor is echter roken, dat het risico van een persoon 2 tot 3 keer verhoogt in vergelijking met niet-rokers. Andere risicofactoren zijn zwaarlijvigheid, gebrek aan lichaamsbeweging, hoge inname van verzadigde vetten en lage inname van groenten en fruit.
Hoe wordt ductaal adenocarcinoom van de alvleesklier gediagnosticeerd?
De eerste diagnose van ductaal adenocarcinoom wordt meestal gesteld nadat een procedure is uitgevoerd om een klein stukje weefsel te verwijderen. Afhankelijk van de hoeveelheid verwijderd weefsel, kan de procedure een a fijne naaldaspiratiebiopsie FNAB) of een kernnaald biopsie. Vervolgens wordt een operatie uitgevoerd om de gehele tumor te verwijderen. Vaak wordt de tumor verwijderd met een deel van de alvleesklier, de dunne darm en de maag in een procedure die een "Whipple" wordt genoemd.
Wat betekent het als de tumor wordt beschreven als goed gedifferentieerd, matig gedifferentieerd of slecht gedifferentieerd?
Pathologen gebruiken de term gedifferentieerd om ductaal adenocarcinoom van de pancreas in drie graden te verdelen: goed gedifferentieerd, matig gedifferentieerd en slecht gedifferentieerd. Om de graad te bepalen kijken pathologen naar het percentage tumorcellen dat ronde structuren wordt genoemd klieren. De graad is belangrijk omdat slecht gedifferentieerde tumoren agressiever zijn en zich waarschijnlijker buiten de pancreas en naar andere organen verspreiden.
- Goed gedifferentieerd – Meer dan 95% van de tumor bestaat uit klieren.
- Matig gedifferentieerd – 50 tot 95% van de tumor bestaat uit klieren.
- Slecht gedifferentieerd – Minder dan 50% van de tumor bestaat uit klieren.
Waarom is de tumorgrootte belangrijk voor ductaal adenocarcinoom van de alvleesklier?
Nadat de tumor volledig is verwijderd, wordt deze opgemeten en wordt de maat vermeld in uw rapport. De tumorgrootte is belangrijk omdat deze wordt gebruikt om het pathologische tumorstadium (pT) te bepalen. Grotere tumoren worden geassocieerd met een slechter algemeen prognose.
Wat betekent tumorextensie en waarom is het belangrijk?
De alvleesklier zit heel dicht bij andere organen en weefsels zoals de lever, dunne darm, maag en bloedvaten. De term tumoruitbreiding wordt gebruikt om kankercellen te beschrijven die zich buiten de alvleesklier en in een van deze organen verspreiden. Alle organen of weefsels die tekenen van tumoruitbreiding vertonen, worden in uw rapport vermeld. Tumoruitbreiding is belangrijk omdat het wordt gebruikt om het pathologische tumorstadium (pT) te bepalen en omdat tumoruitbreiding naar omliggende organen of weefsels wordt geassocieerd met een slechter prognose.
Wat is pancreas intra-epitheliale neoplasie (PanIN)?
Ductaal adenocarcinoom begint vaak met een precancereuze ziekte die pancreas intra-epitheliale neoplasie (PanIN) wordt genoemd. Wanneer ze onder de microscoop worden onderzocht, lijken de abnormale cellen in PanIN op de kankercellen in ductaal adenocarcinoom. Het belangrijkste verschil is dat de abnormale cellen in PanIN alleen te zien zijn in de kanaal. Er zijn geen abnormale cellen in het weefsel rond het kanaal. Zodra de abnormale cellen uit het kanaal breken en het omringende weefsel binnendringen, wordt de diagnose ductaal adenocarcinoom. De beweging van abnormale cellen in het omringende weefsel wordt genoemd invasie.
Wat betekent perineurale invasie en waarom is het belangrijk?
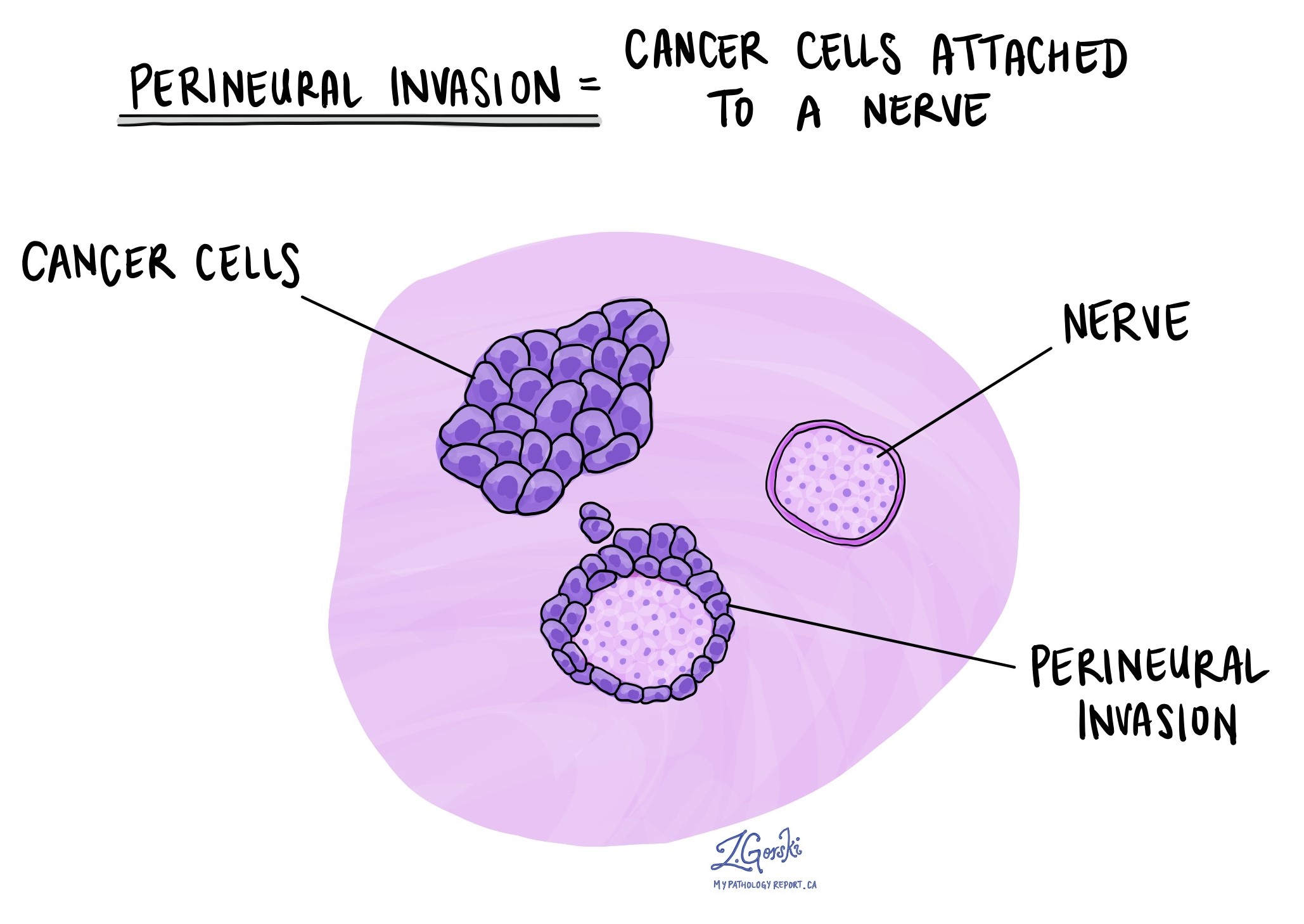
Perineurale invasie is een term die pathologen gebruiken om kankercellen te beschrijven die aan of in een zenuw zijn bevestigd. Een vergelijkbare term, intraneurale invasie, wordt gebruikt om kankercellen in een zenuw te beschrijven. Zenuwen zijn als lange draden die bestaan uit groepen cellen die neuronen worden genoemd. Zenuwen bevinden zich over het hele lichaam en zijn verantwoordelijk voor het verzenden van informatie (zoals temperatuur, druk en pijn) tussen uw lichaam en uw hersenen. Perineurale invasie is belangrijk omdat de kankercellen de zenuw kunnen gebruiken om zich naar omliggende organen en weefsels te verspreiden. Dit verhoogt het risico dat de tumor na de operatie teruggroeit.
Wat betekent lymfovasculaire invasie en waarom is het belangrijk?
Lymfovasculaire invasie betekent dat kankercellen werden gezien in een bloedvat of lymfevat. Bloedvaten zijn lange dunne buizen die bloed door het lichaam vervoeren. Lymfevaten zijn vergelijkbaar met kleine bloedvaten, behalve dat ze een vloeistof vervoeren die lymfe wordt genoemd in plaats van bloed. De lymfevaten zijn verbonden met kleine immuunorganen die lymfeklieren worden genoemd en die door het hele lichaam worden aangetroffen. Lymfovasculaire invasie is belangrijk omdat kankercellen bloedvaten of lymfevaten kunnen gebruiken om zich naar andere delen van het lichaam te verspreiden, zoals lymfeklieren of de longen.

Wat is een marge en waarom zijn marges belangrijk?
In de pathologie is een marge de rand van een weefsel dat wordt doorgesneden bij het verwijderen van een tumor uit het lichaam. De marges die in een pathologierapport worden beschreven, zijn erg belangrijk omdat ze je vertellen of de hele tumor is verwijderd of dat er een deel van de tumor is achtergebleven. De margestatus bepaalt welke (eventuele) aanvullende behandeling u nodig heeft.
De meeste pathologierapporten beschrijven alleen marges na een chirurgische ingreep genaamd an uitsnijding or resectie is uitgevoerd om de gehele tumor te verwijderen. Om deze reden worden marges meestal niet beschreven na een procedure die a . wordt genoemd biopsie wordt uitgevoerd om slechts een deel van de tumor te verwijderen. Het aantal marges dat in een pathologierapport wordt beschreven, is afhankelijk van het soort weefsel dat wordt verwijderd en de locatie van de tumor. De grootte van de marge (de hoeveelheid normaal weefsel tussen de tumor en de snijrand) hangt af van het type tumor dat wordt verwijderd en de locatie van de tumor.
De twee belangrijkste marges in de alvleesklier zijn:
- Het gemeenschappelijke galkanaal marge - De gemeenschappelijke galweg is een kanaal dat de lever met de pancreas verbindt.
- De pancreasmarge – Dit is het deel van de alvleesklier dat is doorgesneden om de tumor te verwijderen. De hoeveelheid verwijderde pancreas hangt af van de locatie van de tumor in de pancreas.
Andere marges die in uw rapport kunnen worden beschreven, zijn onder meer:
- Het uncinate proces – Dit is het deel van de alvleesklier dat tegen de achterkant van de buik aanligt. Het weefsel rond dit deel van de alvleesklier moet worden doorgesneden om de alvleesklier uit het lichaam te verwijderen.
- De marge van de twaalfvingerige darm (of dunne darm) – Een deel van de dunne darm wordt gewoonlijk tegelijk met de tumor in de pancreas verwijderd. De dunne darmrand is een plaats waar de chirurg de dunne darm doorsnijdt om de tumor te verwijderen.
- De maag (of maag) marge – Een deel van de maag wordt gewoonlijk tegelijk met de tumor in de alvleesklier verwijderd. De maagrand is de plaats waar de chirurg de maag doorsnijdt om de tumor te verwijderen.
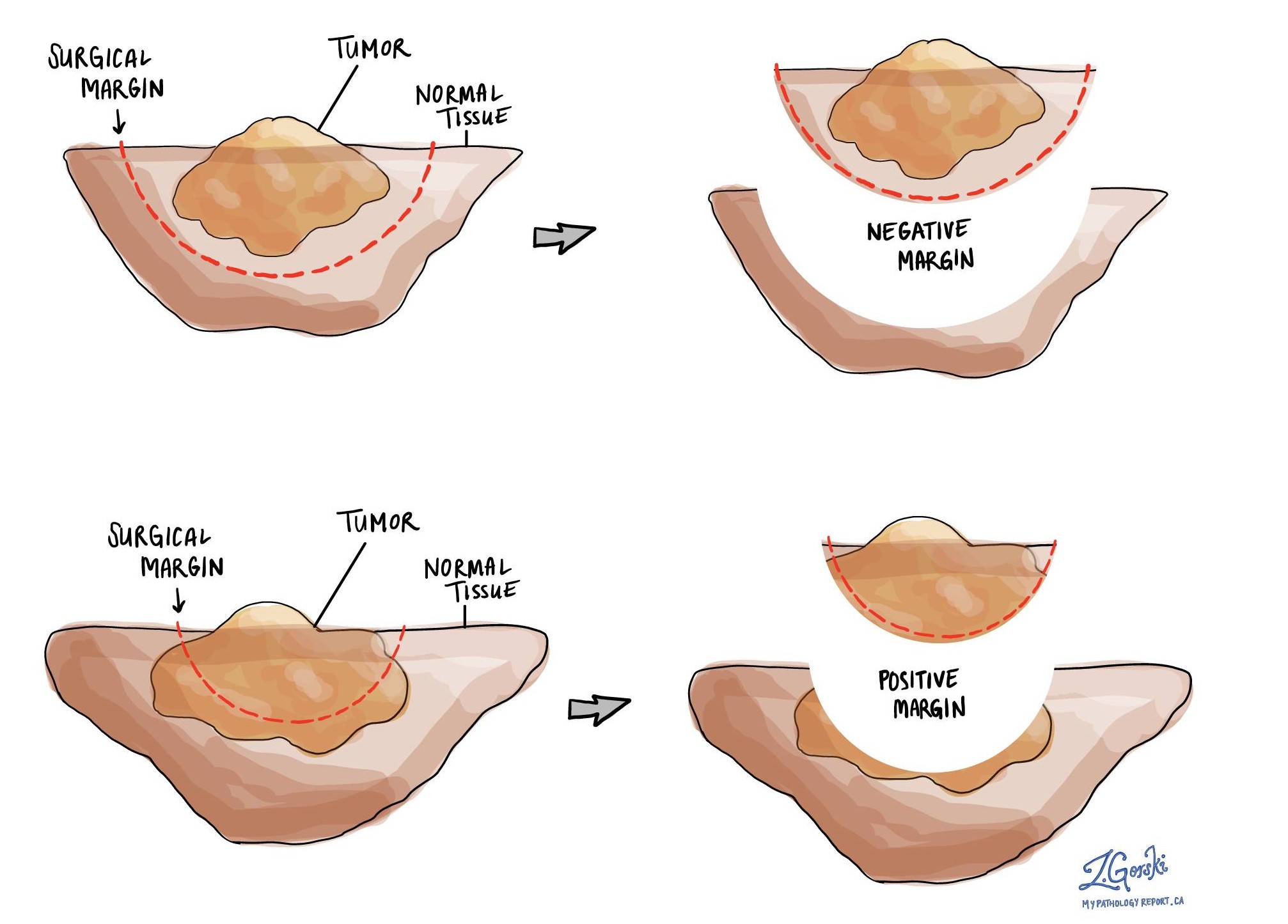
Pathologen onderzoeken zorgvuldig de marges om te zoeken naar tumorcellen aan de snijrand van het weefsel. Als er tumorcellen worden gezien aan de snijrand van het weefsel, wordt de marge als positief beschreven. Als er geen tumorcellen worden gezien aan de snijrand van het weefsel, wordt een marge als negatief beschreven. Zelfs als alle marges negatief zijn, zullen sommige pathologierapporten ook een meting geven van de tumorcellen die zich het dichtst bij de snijrand van het weefsel bevinden.
Een positieve (of zeer nauwe) marge is belangrijk omdat dit betekent dat er tumorcellen in uw lichaam kunnen zijn achtergebleven toen de tumor operatief werd verwijderd. Om deze reden kan aan patiënten met een positieve marge een andere operatie worden aangeboden om de rest van de tumor te verwijderen of bestralingstherapie naar het deel van het lichaam met de positieve marge. De beslissing om aanvullende behandeling aan te bieden en het soort behandelingsopties dat wordt aangeboden, hangt af van een aantal factoren, waaronder het type tumor dat is verwijderd en het betrokken lichaamsgebied. Een aanvullende behandeling kan bijvoorbeeld niet nodig zijn voor een goedaardig (niet-kankerachtig) type tumor, maar kan sterk worden aanbevolen voor een kwaadaardig (kankerachtig) type tumor.
Wat betekent behandeleffect?
Als u een behandeling (chemotherapie of bestralingstherapie) voor uw kanker heeft ondergaan voordat de tumor werd verwijderd, zal uw patholoog al het ingediende weefsel onderzoeken om te zien hoeveel van de tumor nog leeft (levensvatbaar). Er zijn verschillende systemen die worden gebruikt om behandeleffecten te beschrijven. In het meest gebruikelijke systeem wordt het behandelingseffect beschreven op een schaal van 0 tot 3, waarbij 0 geen resterende levensvatbare tumor is (alle kankercellen zijn dood) en 3 geen respons op therapie is (alle of de meeste kankercellen zijn in leven). ). Lymfeklieren met kankercellen zal ook worden onderzocht op behandelingseffecten.
Werden lymfeklieren onderzocht en bevatten deze kankercellen?
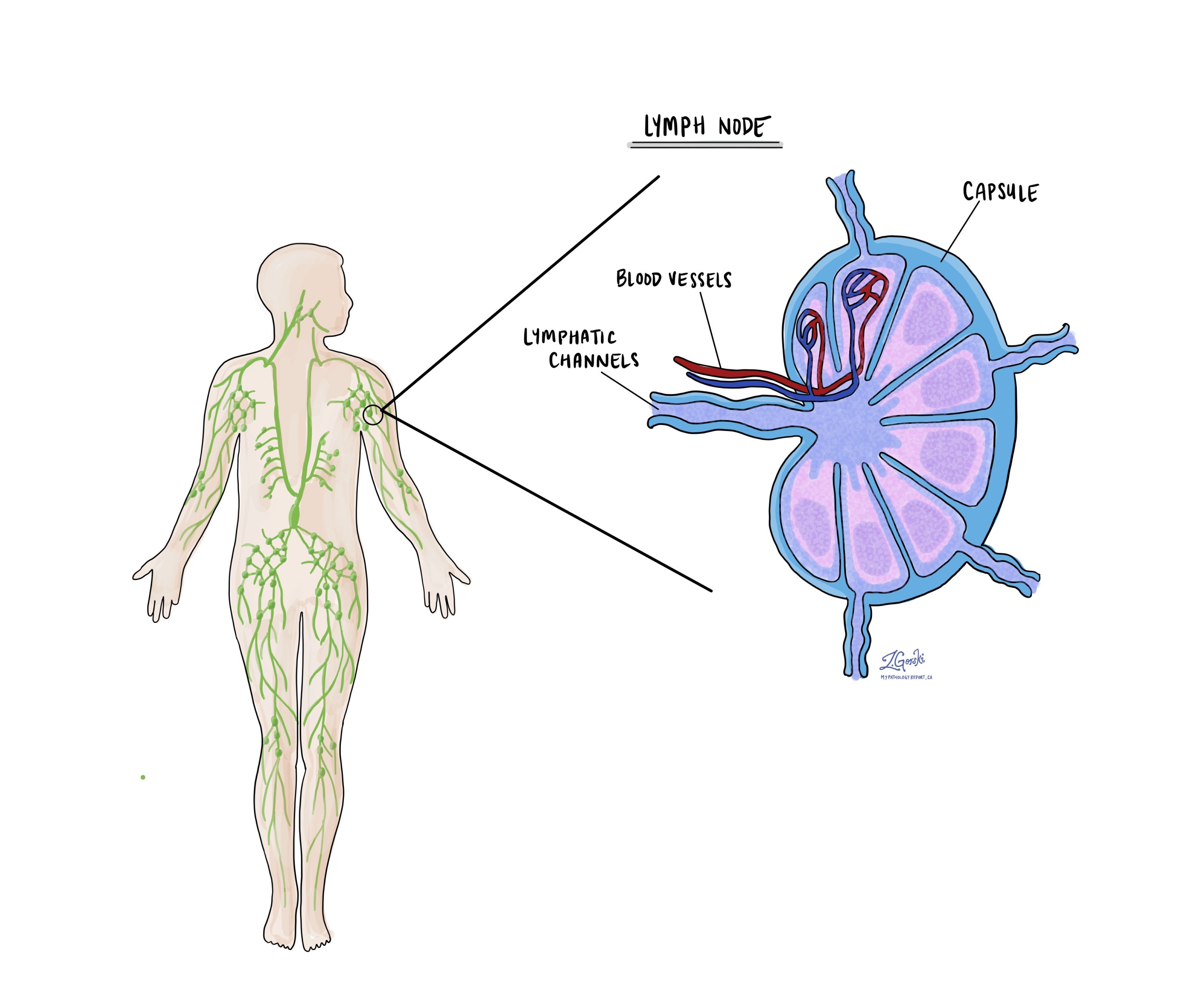
Lymfeklieren zijn kleine immuunorganen die door het hele lichaam worden aangetroffen. Kankercellen kunnen zich van een tumor naar de lymfeklieren verspreiden via kleine bloedvaten die lymfevaten worden genoemd. Om deze reden worden lymfeklieren vaak verwijderd en onder een microscoop onderzocht om naar kankercellen te zoeken. De verplaatsing van kankercellen van de tumor naar een ander deel van het lichaam, zoals een lymfeklier, wordt a . genoemd uitzaaiing.
Kankercellen verspreiden zich meestal eerst naar lymfeklieren dicht bij de tumor, hoewel lymfeklieren ver weg van de tumor ook betrokken kunnen zijn. Om deze reden bevinden de eerste verwijderde lymfeklieren zich meestal dicht bij de tumor. Lymfeklieren verder weg van de tumor worden meestal alleen verwijderd als ze vergroot zijn en er een groot klinisch vermoeden bestaat dat er kankercellen in de lymfeklier zitten.
Als er lymfeklieren uit uw lichaam zijn verwijderd, worden deze onder de microscoop onderzocht door een patholoog en de resultaten van dit onderzoek worden beschreven in uw rapport. De meeste rapporten bevatten het totale aantal onderzochte lymfeklieren, waar in het lichaam de lymfeklieren werden gevonden en het aantal (indien aanwezig) dat kankercellen bevat. Als er kankercellen werden gezien in een lymfeklier, wordt ook de grootte van de grootste groep kankercellen (vaak beschreven als "focus" of "afzetting") opgenomen.
Het onderzoek van lymfeklieren is om twee redenen belangrijk. Eerst wordt deze informatie gebruikt om het pathologische nodale stadium (pN) te bepalen. Ten tweede verhoogt het vinden van kankercellen in een lymfeklier het risico dat kankercellen in de toekomst in andere delen van het lichaam worden gevonden. Als gevolg hiervan zal uw arts deze informatie gebruiken bij de beslissing of aanvullende behandeling zoals chemotherapie, bestralingstherapie of immunotherapie nodig is.
Wat betekent het als een lymfeklier als positief wordt beschreven?
Pathologen gebruiken de term 'positief' vaak om een lymfeklier te beschrijven die kankercellen bevat. Een lymfeklier die kankercellen bevat, kan bijvoorbeeld 'positief voor maligniteit' of 'positief voor uitgezaaid carcinoom' worden genoemd.
Wat betekent het als een lymfeklier als negatief wordt beschreven?
Pathologen gebruiken de term 'negatief' vaak om een lymfeklier te beschrijven die geen kankercellen bevat. Een lymfeklier die geen kankercellen bevat, kan bijvoorbeeld "negatief voor maligniteit" of "negatief voor gemetastaseerd carcinoom" worden genoemd.
Wat is het pathologische stadium van ductaal adenocarcinoom van de pancreas?
Het pathologische stadium voor ductaal adenocarcinoom van de pancreas is gebaseerd op het TNM-stadiëringssysteem, een internationaal erkend systeem dat oorspronkelijk is ontwikkeld door de Amerikaans Gemengd Comité voor Kanker. Dit systeem gebruikt informatie over de primaire tumor (T), lymfeklieren (N), en verre metastatische ziekte (M) om het volledige pathologische stadium (pTNM) te bepalen. Uw patholoog onderzoekt het ingeleverde weefsel en geeft elk onderdeel een nummer. Over het algemeen betekent een hoger aantal een meer gevorderde ziekte en een slechtere prognose.
Tumorstadium (pT) voor ductaal adenocarcinoom
Ductaal adenocarcinoom krijgt een tumorstadium tussen 1 en 4 op basis van de grootte van de tumor en tumoruitbreiding in nabijgelegen organen.
- T1 – De grootte van de tumor is 2 cm of minder.
- T2 – De grootte van de tumor is groter dan 2 cm maar niet groter dan 4 cm.
- T3 – De grootte van de tumor is groter dan 4 cm.
- T4 – De tumor heeft zich buiten de pancreas verspreid en is een van de grote bloedvaten in de buurt binnengedrongen.
Knoopstadium (pN) voor ductaal adenocarcinoom
Ductaal adenocarcinoom krijgt een knoopstadium tussen 0 en 2 op basis van de aan- of afwezigheid van kankercellen in een lymfeklier en het aantal lymfeklieren met kankercellen.
- N0 – In geen van de onderzochte lymfeklieren werden kankercellen gezien.
- N1 – Kankercellen werden gezien in ten minste één lymfeklier, maar niet meer dan 3 lymfeklieren.
- N2 – Kankercellen werden gezien in meer dan 3 lymfeklieren.
- NX – Er zijn geen lymfeklieren opgestuurd voor pathologisch onderzoek.
Gemetastaseerd stadium (pM) voor ductaal adenocarcinoom
Ductaal adenocarcinoom krijgt een gemetastaseerd stadium van 0 of 1 op basis van de aanwezigheid van kankercellen op een afgelegen plaats in het lichaam (bijvoorbeeld de longen). Het metastatische stadium kan alleen worden bepaald als weefsel van een verre locatie wordt opgestuurd voor pathologisch onderzoek. Omdat dit weefsel zelden aanwezig is, kan het metastatische stadium niet worden bepaald en wordt het vermeld als MX.


