por Jason Wasserman MD PhD FRCPC e Zuzanna Gorski MD
28 de novembro de 2025
Adenocarcinoma do cólon É o tipo mais comum de câncer de cólon. Ele começa nas células glandulares que revestem a superfície interna do cólon. Essas células normalmente produzem muco, que ajuda as fezes a se moverem pelo intestino grosso. Quando essas células se tornam anormais e crescem descontroladamente, formam um tumor chamado adenocarcinoma.
O que causa o adenocarcinoma do cólon?
A maioria dos adenocarcinomas de cólon se desenvolve lentamente ao longo do tempo devido a alterações no DNA das células que revestem o cólon. Essas alterações no DNA podem ocorrer aleatoriamente, ser influenciadas pelo estilo de vida ou serem hereditárias. Em muitos casos, o tumor começa como um crescimento não canceroso chamado adenocarcinoma. Adenoma or pólipo e então evolui para câncer.
Fatores de risco importantes incluem histórico pessoal ou familiar de pólipos ou câncer colorretal, condições hereditárias como a síndrome de Lynch ou polipose adenomatosa familiar (PAF) e histórico prolongado de câncer colorretal. inflamação no cólon devido a doenças como colite ulcerativa ou doença de Crohn. Dietas ricas em carne vermelha ou processada e pobres em fibras, atividade física limitada, tabagismo e consumo excessivo de álcool também aumentam o risco.
Quais são os sintomas?
O adenocarcinoma de cólon geralmente não causa sintomas em seus estágios iniciais. À medida que o tumor cresce, os sintomas podem incluir alterações nos hábitos intestinais, como constipação, diarreia ou alteração no formato das fezes; sangramento retal ou sangue misturado às fezes; desconforto abdominal, inchaço ou dor; perda de peso inexplicável; e fadiga ou fraqueza devido a anemia, que é uma baixa contagem de glóbulos vermelhos. Os sintomas dependem do tamanho e da localização do tumor. Qualquer alteração persistente nos hábitos intestinais ou sinais de sangramento devem ser discutidos com seu médico.
Como é feito o diagnóstico?
O diagnóstico de adenocarcinoma de cólon é feito após uma biopsia é examinado por um patologistaUm médico que diagnostica doenças estudando tecidos ao microscópio. A avaliação normalmente envolve uma série de etapas que identificam uma área anormal, confirmam o câncer ao microscópio e determinam a extensão da doença.
Avaliação clínica e preparação
Seu médico analisará seus sintomas, histórico médico e familiar, e fatores de risco como pólipos prévios, doença inflamatória intestinal, tabagismo, dieta e consumo de álcool. Você receberá instruções para o preparo intestinal, de modo que o cólon esteja limpo para o exame.
Colonoscopia e biópsia
A colonoscopia é realizada para examinar todo o cólon e o reto. Durante o procedimento, o médico insere uma câmera fina e flexível (o colonoscópio) pelo reto para examinar diretamente o revestimento do cólon. Se for detectada alguma anormalidade — como um pólipo, uma massa ulcerada ou mucosa irregular — o médico coleta amostras de tecido (biópsias). Se um pólipo parecer canceroso, ele pode ser removido completamente durante o procedimento, desde que seja seguro fazê-lo. As biópsias são preservadas e enviadas ao laboratório de patologia para análise.
Exame microscópico
Um patologista examina a biópsia ao microscópio. O câncer é diagnosticado quando as estruturas glandulares normais são substituídas por glândulas malignas ou células cancerígenas pouco coesas que invadem camadas de tecido mais profundas. As células tumorais geralmente apresentam núcleos aumentados e irregulares e podem produzir mucina, um tipo de muco, embora não nas grandes quantidades observadas no adenocarcinoma mucinoso.
O relatório descreve a aparência do tumor (tipo histológico), o grau de semelhança com as células normais (grau do tumor) e se apresenta características agressivas, como invasão linfática (células cancerosas dentro dos canais linfáticos), invasão vascular (células cancerosas dentro dos vasos sanguíneos) e invasão perineural (células cancerosas crescendo ao longo dos nervos).
Estudos de imagem e estadiamento
Se o câncer for diagnosticado, exames de imagem, como tomografia computadorizada do tórax, abdômen e pelve, ajudam a determinar se o câncer se espalhou para os linfonodos ou órgãos distantes. Em casos específicos, podem ser realizados exames adicionais, como ressonância magnética ou PET-CT. A cirurgia pode então ser planejada para remover o tumor juntamente com os linfonodos próximos, tanto para tratar o câncer quanto para fornecer um estadiamento patológico preciso.
Grau do tumor
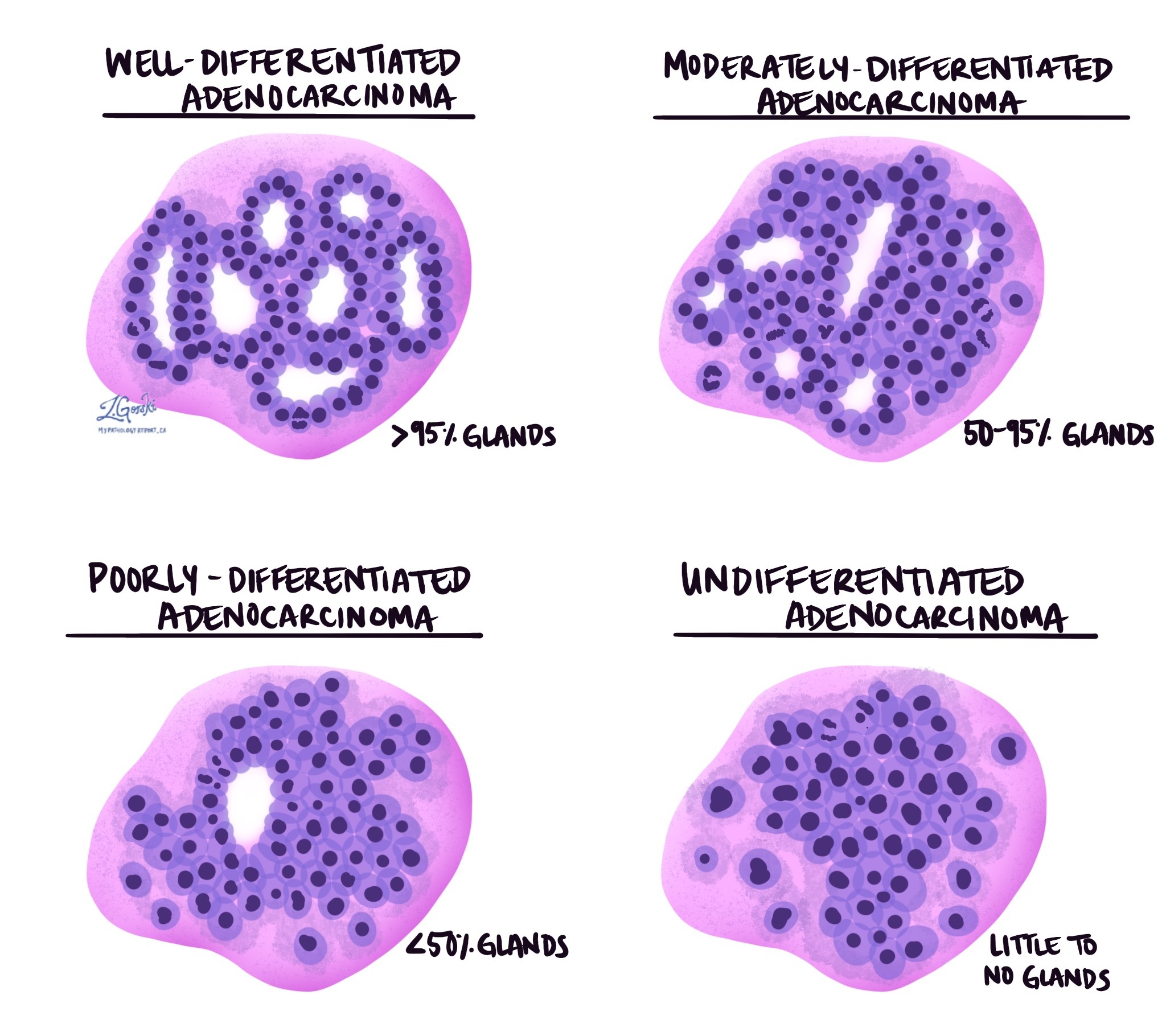
O grau do tumor descreve o quão semelhantes as células tumorais são às células normais do cólon. No adenocarcinoma de cólon, o grau é baseado na quantidade de estruturas glandulares formadas pelo tumor.
-
Grau 1 (bem diferenciado) – Mais de 95% dos tumores formam glândulas.
-
Grau 2 (moderadamente diferenciado) – Entre 50 e 95 por cento dos tumores formam glândulas.
-
Grau 3 (pouco diferenciado) – Menos de 50% do tumor forma glândulas.
-
4º ano (não diferenciado) – Não se observa formação glandular.
Tumores de grau mais elevado são mais agressivos e têm maior probabilidade de se disseminarem. As diretrizes mais recentes da Organização Mundial da Saúde também permitem um sistema simplificado de dois níveis, no qual o grau baixo inclui os graus 1 e 2, e o grau alto inclui os graus 3 e 4.
Diferenciação mucinosa
A diferenciação mucinosa significa que o tumor contém uma grande quantidade de mucina extracelular, ou muco, fora das células tumorais. Quando mais de 50% do tumor é composto de mucina, ele é classificado como adenocarcinoma mucinoso. Esse subtipo pode apresentar comportamento mais agressivo e disseminação mais fácil.
Nível de invasão
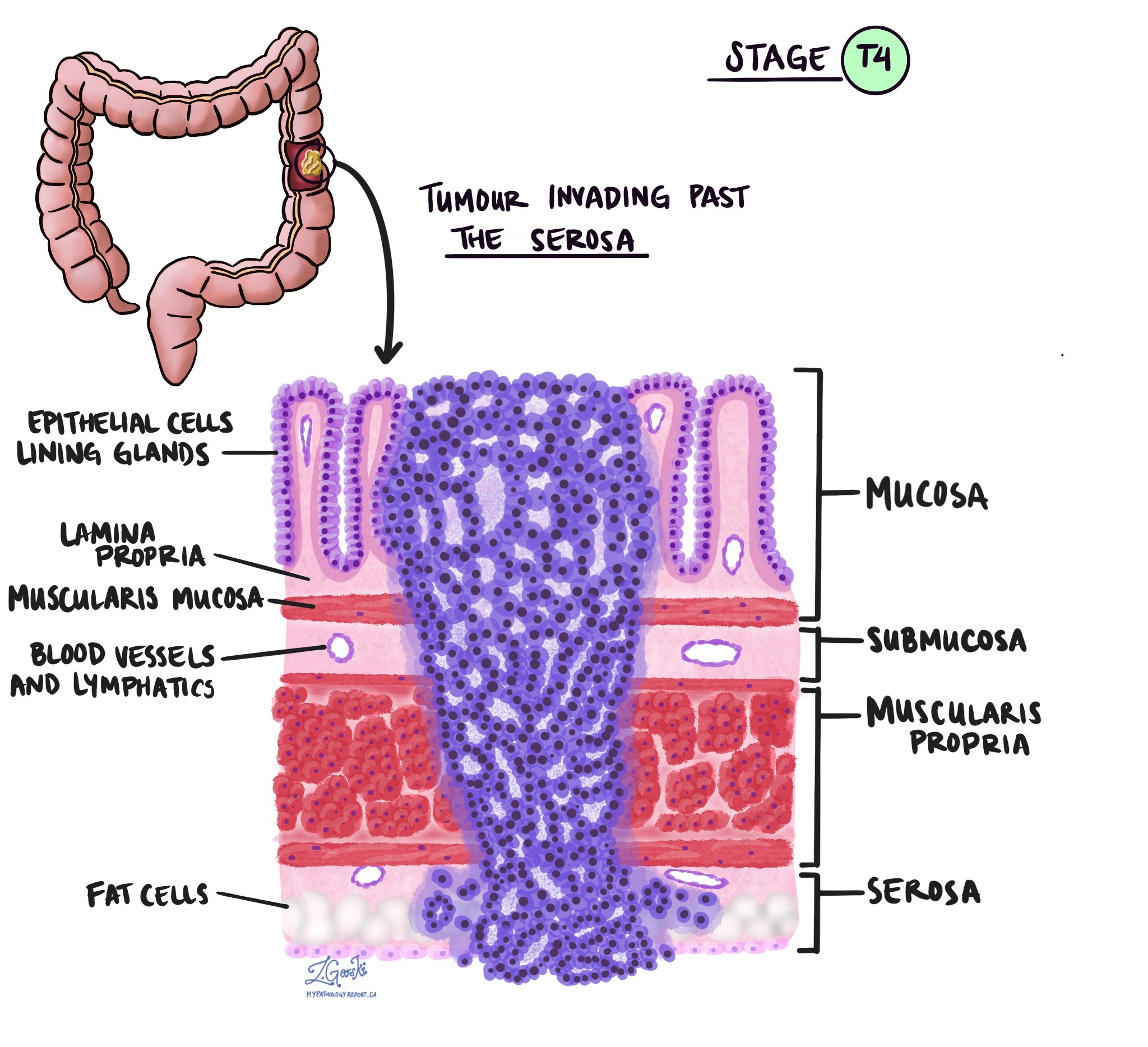
Invasão Descreve a profundidade com que o tumor se infiltrou na parede do cólon. O adenocarcinoma de cólon começa na mucosa, a fina camada interna que reveste o cólon, e pode se espalhar para camadas mais profundas.
As camadas da parede do cólon são descritas abaixo para facilitar a compreensão de seus nomes em um laudo anatomopatológico.
-
Mucosa – Este revestimento interno contém as células epiteliais que formam as glândulas e onde os cânceres começam.
-
Submucosa – Essa camada de suporte de tecido conjuntivo fica logo abaixo da mucosa e contém vasos sanguíneos e canais linfáticos.
-
Muscular própria – Essa espessa camada muscular se contrai para mover os resíduos através do cólon.
-
Tecido subseroso – Essa camada é uma fina faixa de gordura ou tecido conjuntivo localizada externamente ao músculo em algumas partes do cólon.
-
serosa – Esta é a superfície externa lisa que reveste partes do cólon, embora não esteja presente em todas as regiões.

À medida que um tumor cresce em camadas mais profundas, a probabilidade de disseminação para os gânglios linfáticos ou órgãos distantes aumenta. A camada mais profunda atingida pelo tumor é relatada como o nível de invasão e é usada para determinar o estágio patológico do tumor (pT). Os patologistas determinam esse nível apenas examinando o tecido ao microscópio. Essa informação auxilia no planejamento do tratamento e na estimativa do risco de recorrência do câncer.
Brotamento de tumor
A brotação tumoral refere-se a células cancerígenas isoladas ou pequenos aglomerados de células observados na borda de avanço do tumor ao microscópio. O número de brotos é contado e usado para atribuir uma pontuação baixa, intermediária ou alta. Uma alta pontuação de brotação tumoral está associada a um maior risco de disseminação do câncer.
Invasão linfática
A invasão linfática significa que células cancerígenas estão presentes dentro dos canais linfáticos, que são minúsculos vasos que drenam fluidos e transportam células imunológicas. Uma fina camada de células reveste esses canais e geralmente não contém glóbulos vermelhos. A detecção de células tumorais dentro dos canais linfáticos sugere uma maior probabilidade de disseminação para os linfonodos próximos. Os patologistas podem utilizar a imuno-histoquímica, um método especial de coloração, para identificar células cancerígenas nesses minúsculos vasos.
Invasão vascular
A invasão vascular significa que há células cancerígenas presentes dentro dos vasos sanguíneos. Isso pode ocorrer na parede do cólon (invasão vascular intramural) ou no tecido circundante (invasão vascular extramural). Ambas estão associadas a um risco maior de disseminação do câncer para outros órgãos, como o fígado ou os pulmões, sendo a invasão vascular extramural considerada particularmente importante. Colorações especiais podem ser utilizadas para confirmar a presença de células tumorais dentro dos vasos sanguíneos.
Invasão perineural
A invasão perineural significa que as células cancerígenas estão crescendo ao longo ou ao redor de um nervo. Essa característica é mais comum em tumores avançados e está associada a um risco maior de o câncer se espalhar ou retornar após o tratamento. Ao microscópio, os patologistas procuram células tumorais que circundam pelo menos um terço da parte externa de um nervo.
Resposta imune
O organismo frequentemente desencadeia uma resposta imune a um tumor, enviando linfócitos e outras células imunes para cercá-lo. Quando uma forte resposta imune é observada ao microscópio, isso pode sugerir que o organismo está contendo ou retardando o crescimento do tumor. Um padrão específico, denominado reação semelhante à de Crohn, mostra grupos de células imunes agrupadas perto do tumor e geralmente está associado a um melhor prognóstico. Os patologistas podem utilizar a imuno-histoquímica para avaliar as células imunes e, embora isso nem sempre esteja incluído nos laudos padrão, a resposta imune é cada vez mais reconhecida como uma característica importante.
margens
As margens são as bordas do tecido removido durante a cirurgia. Os patologistas examinam as margens para determinar se o tumor foi removido completamente.
-
As margens proximal e distal descrevem as extremidades do segmento de cólon removido.
-
A margem de ressecção circunferencial (MRC) refere-se à borda mais externa do tecido mole, que é particularmente importante no câncer retal.
-
A margem mesocólica é importante para tumores no ceco e no cólon adjacente.
Uma margem negativa significa que não foram observadas células cancerígenas na borda. Uma margem positiva significa que há células cancerígenas presentes na borda, sugerindo que algum tumor pode permanecer e que tratamento adicional pode ser necessário.
Efeito do tratamento
Se um tratamento como quimioterapia ou radioterapia for administrado antes da cirurgia, o tumor pode diminuir de tamanho. Os patologistas avaliam a quantidade de tumor viável remanescente e atribuem uma pontuação de resposta ao tratamento.
-
Pontuação 0 – Ausência de células cancerígenas viáveis (resposta completa).
-
Pontuação 1 – Células isoladas ou pequenos grupos raros de células cancerígenas (resposta quase completa).
-
Pontuação 2 – Câncer residual com evidência de regressão tumoral, mas mais do que células isoladas ou pequenos grupos raros (resposta parcial).
-
Pontuação 3 – Câncer residual extenso sem regressão tumoral evidente (resposta fraca ou nenhuma resposta).
Essas informações ajudam os médicos a entender como o tumor respondeu à terapia e se um tratamento adicional é apropriado.
Depósitos tumorais
Os depósitos tumorais são pequenos nódulos de células cancerígenas localizados na gordura que circunda o cólon ou o reto, na área de drenagem linfática do tumor primário. Esses depósitos não contêm tecido linfonodal ou vasos sanguíneos identificáveis. Se um foco tumoral for encontrado dentro de um vaso sanguíneo, é classificado como invasão vascular; se for encontrado próximo a um nervo, é classificado como invasão perineural.
Os depósitos tumorais são importantes porque sua presença aumenta o risco de disseminação. Se houver depósitos tumorais, mas os linfonodos forem negativos, o estágio nodal é N1c, independentemente do estágio do tumor. Se também houver linfonodos positivos, o câncer é estadiado pelo número de linfonodos positivos, e a presença e o número de depósitos tumorais ainda são registrados, pois são fatores prognósticos adversos que podem influenciar as decisões de tratamento.
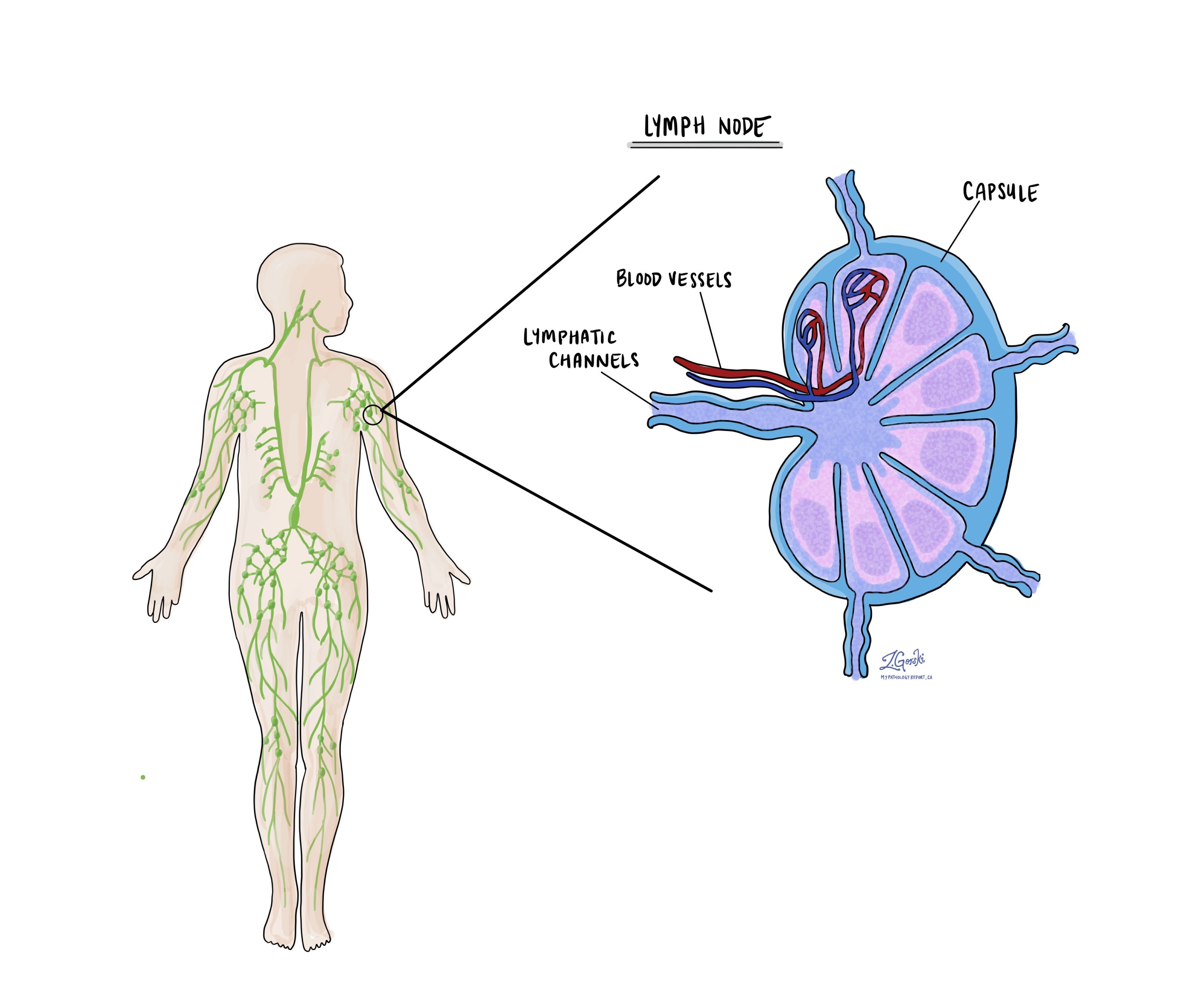
Gânglios linfáticos
Os gânglios linfáticos são pequenos órgãos imunológicos que filtram o fluido linfático e podem reter células cancerígenas que se disseminaram a partir do tumor primário. Durante a cirurgia, os gânglios linfáticos próximos ao tumor são removidos e examinados. Os patologistas classificam os gânglios linfáticos como positivos se contiverem câncer e negativos se não contiverem. Caso seja detectado câncer, o laudo pode incluir o tamanho do maior foco tumoral e se há extensão extranodal, o que significa que as células tumorais romperam a cápsula do gânglio linfático e invadiram o tecido circundante.
O exame dos linfonodos é essencial para determinar o estágio nodal patológico (pN) e para estimar o risco de disseminação para outras partes do corpo. Essas informações ajudam os médicos a decidir se são necessários tratamentos adicionais, como quimioterapia, radioterapia ou imunoterapia.
Biomarcadores para adenocarcinoma do cólon
Biomarcadores Os biomarcadores são características mensuráveis dentro das células tumorais — geralmente envolvendo genes ou proteínas específicos — que ajudam os médicos a entender como o câncer se comporta e como ele pode responder ao tratamento. No adenocarcinoma de cólon, os testes de biomarcadores são essenciais porque os resultados podem identificar síndromes de câncer hereditárias, determinar se a imunoterapia provavelmente será eficaz e orientar o uso de tratamentos direcionados. Os testes de biomarcadores agora fazem parte do diagnóstico e tratamento padrão do câncer colorretal.
Que tipos de biomarcadores são testados para adenocarcinoma de cólon?
A maioria dos testes de biomarcadores para câncer de cólon se concentra em mutações genéticas, rearranjos de genes e expressão de proteínas. Isso inclui testes que avaliam a capacidade do tumor de reparar danos ao DNA, testes que identificam mutações específicas em genes promotores do crescimento e testes que ajudam a determinar se tratamentos direcionados podem ser eficazes. Os patologistas geralmente realizam esses testes em uma amostra de biópsia ou no tumor removido durante a cirurgia, utilizando métodos como imuno-histoquímica (IHQ), que usa anticorpos ligados a corantes para destacar proteínas específicas, e testes moleculares como PCR e sequenciamento de nova geração (NGS), que analisam o DNA do tumor.
Proteínas de reparo de erros de pareamento (MMR: MLH1, PMS2, MSH2, MSH6)
As proteínas de reparo de erros de pareamento (MMR) fazem parte do sistema de reparo do DNA da célula. Quando alguma dessas proteínas — MLH1, PMS2, MSH2 ou MSH6 — está ausente, o tumor torna-se deficiente em reparo de erros de pareamento (dMMR) e pode acumular erros de DNA mais rapidamente. Esse biomarcador é importante porque tumores dMMR têm maior probabilidade de responder à imunoterapia, e a descoberta também pode indicar a síndrome de Lynch, uma condição hereditária que aumenta o risco de câncer de cólon e outros tipos de câncer.
Os patologistas testam as proteínas MMR usando imuno-histoquímica. Este teste destaca cada proteína para mostrar se ela está presente nos núcleos das células tumorais. A perda de uma ou mais proteínas indica deficiência no reparo de erros de pareamento.
Seu laudo descreverá o tumor como MMR-proficiente (pMMR) se todas as proteínas estiverem presentes, ou MMR-deficiente (dMMR) se alguma estiver ausente. O laudo também poderá especificar quais proteínas estão ausentes.
Hipermetilação do promotor MLH1
A hipermetilação do promotor MLH1 é uma alteração química que "desativa" o gene MLH1, levando à perda de MLH1 e de seu parceiro PMS2. Isso causa deficiência no reparo de erros de pareamento (dMMR), mas geralmente é um evento esporádico e não hereditário. Esse biomarcador é importante porque a hipermetilação de MLH1 ajuda a distinguir tumores dMMR esporádicos de tumores causados pela síndrome de Lynch.
Os testes são realizados utilizando métodos moleculares, como PCR específica para metilação ou sequenciamento de nova geração, para determinar se o promotor do gene MLH1 está hipermetilado.
Seu laudo indicará se o gene MLH1 está hipermetilado ou não. Tumores com hipermetilação de MLH1 geralmente não estão associados à síndrome de Lynch.
KRAS e NRAS
KRAS e NRAS são genes que controlam o crescimento celular. Mutações nesses genes são comuns no câncer de cólon e são importantes porque tumores com mutações em KRAS ou NRAS não respondem a medicamentos anti-EGFR, como cetuximabe ou panitumumabe. Essas mutações também são úteis para entender o comportamento do tumor e escolher tratamentos alternativos.
Os testes geralmente são realizados usando PCR ou sequenciamento de nova geração para examinar porções específicas dos genes onde as mutações ocorrem com frequência, incluindo os códons 12, 13, 61 e 146.
Seu laudo descreverá o tumor como KRAS-positivo ou NRAS-positivo se uma mutação for encontrada e KRAS-negativo ou NRAS-negativo se nenhuma mutação for detectada.
IRMÃO
BRAF é um gene da mesma via de crescimento que KRAS e NRAS. A mutação BRAF V600E está associada a um comportamento tumoral mais agressivo e maior probabilidade de disseminação. Esse biomarcador é importante porque tumores com mutação BRAF geralmente não respondem bem à terapia anti-EGFR, e a identificação de uma mutação BRAF também auxilia na interpretação dos resultados do reparo de erros de pareamento. Uma mutação BRAF V600E sugere fortemente um tumor esporádico em vez da síndrome de Lynch.
O teste BRAF é geralmente realizado por meio de PCR ou sequenciamento de nova geração para detectar a mutação V600E ou outras alterações no gene BRAF.
Seu laudo indicará que o tumor é BRAF-positivo se houver uma mutação presente e BRAF-negativo se nenhuma mutação for encontrada.
PIK3CA
PIK3CA é um gene envolvido em vias que auxiliam no crescimento e na sobrevivência celular. Mutações em PIK3CA ocorrem em cerca de 10 a 20% dos cânceres de cólon. Esse biomarcador é importante porque mutações em PIK3CA — especialmente quando combinadas com mutações em KRAS ou NRAS — podem reduzir o benefício da terapia anti-EGFR. Algumas pesquisas sugerem que pacientes com mutações em PIK3CA podem se beneficiar do uso de aspirina após a cirurgia, embora isso ainda não seja um tratamento padrão.
O teste para mutações no gene PIK3CA é realizado utilizando sequenciamento de nova geração para analisar o DNA do tumor.
Seu tumor será descrito como PIK3CA-positivo se uma mutação estiver presente e PIK3CA-negativo se nenhuma mutação for detectada.
PTEN
O PTEN é um gene supressor de tumor que ajuda a controlar o crescimento celular. Quando o PTEN é perdido ou deixa de funcionar corretamente, as células tumorais podem crescer com mais facilidade e responder menos bem ao tratamento anti-EGFR. O teste de PTEN é importante porque ajuda a explicar a resistência a certas terapias.
A expressão de PTEN pode ser avaliada por meio de testes moleculares para detectar alterações genéticas ou por imuno-histoquímica para verificar a presença da proteína PTEN nas células tumorais.
Seu laudo pode descrever o tumor como PTEN-intacto se a proteína estiver presente ou PTEN-desaparecer se a proteína estiver ausente. Os resultados dos testes moleculares também podem indicar a presença de uma mutação.
EGFR
O EGFR é uma proteína presente na superfície de algumas células cancerígenas que ajuda a controlar as vias normais de crescimento. Medicamentos anti-EGFR, como o cetuximabe e o panitumumabe, têm como alvo essa proteína. Embora o próprio EGFR não seja usado para selecionar o tratamento no câncer de cólon, o teste é realizado, por vezes, para fins de pesquisa ou ensaios clínicos. As decisões de tratamento baseiam-se mais fortemente nos genes KRAS, NRAS e BRAF, que predizem se a terapia anti-EGFR será eficaz.
Quando realizado, o teste de EGFR pode envolver imuno-histoquímica para avaliar a expressão da proteína ou testes moleculares para examinar o estado do gene EGFR.
Os resultados podem descrever a expressão ou o estado de mutação do EGFR, embora essas descobertas não sejam usadas rotineiramente para orientar o tratamento do adenocarcinoma de cólon.
PD-L1
PD-L1 é uma proteína presente na superfície de algumas células tumorais que ajuda o câncer a se esconder do sistema imunológico. Embora o teste de PD-L1 desempenhe um papel importante em alguns tipos de câncer, sua utilidade no câncer de cólon ainda está sendo estudada e não é utilizado rotineiramente para orientar o tratamento. Em certas situações, no entanto, o PD-L1 pode fornecer informações adicionais sobre a capacidade do tumor de responder à imunoterapia.
Os patologistas testam a presença de PD-L1 usando imuno-histoquímica, um método que utiliza anticorpos ligados a corantes para destacar a proteína PD-L1 nas células tumorais e nas células imunes próximas.
Os resultados são frequentemente relatados usando uma Pontuação Positiva Combinada (CPS), que mede a porcentagem de células tumorais e imunes que apresentam coloração para PD-L1. Valores de CPS mais altos indicam níveis mais elevados de expressão de PD-L1, mas o significado dessas pontuações no câncer de cólon permanece incerto.
HER2 (ERBB2)
HER2 é um gene que ajuda a controlar o crescimento celular. Em um pequeno número de cânceres de cólon — especialmente aqueles sem mutações em KRAS ou BRAF — o gene HER2 pode se tornar hiperativo. O HER2 é importante porque tumores com superexpressão ou amplificação de HER2 podem responder a terapias direcionadas a HER2, particularmente em estágios avançados da doença ou quando outros tratamentos não são mais eficazes.
Os testes geralmente são realizados por meio de imuno-histoquímica para avaliar os níveis da proteína HER2 e, quando necessário, testes moleculares adicionais, como FISH ou sequenciamento de nova geração, para determinar se o gene HER2 está amplificado.
Os níveis da proteína HER2 são relatados usando uma pontuação IHC de 0, 1+, 2+ ou 3+.
-
Resultados de 0 ou 1+ são considerados HER2-negativos.
-
Uma pontuação de 3 ou mais é considerada HER2-positiva.
-
Uma pontuação de 2 ou mais é considerada inconclusiva, e o tumor é testado posteriormente para amplificação do gene HER2.
Um tumor é classificado como HER2-positivo se apresentar forte expressão proteica (3+) ou se a amplificação do gene for confirmada.
Estágio patológico (pTNM)
O estadiamento patológico descreve o quanto o câncer se disseminou quando o tumor é removido e examinado ao microscópio. Ele utiliza três componentes: T (profundidade do tumor), N (linfonodos) e M (metástase). Os patologistas determinam os estágios pT e pN a partir da peça cirúrgica. O estágio M geralmente é determinado por exames de imagem.
Estágio do tumor (pT)
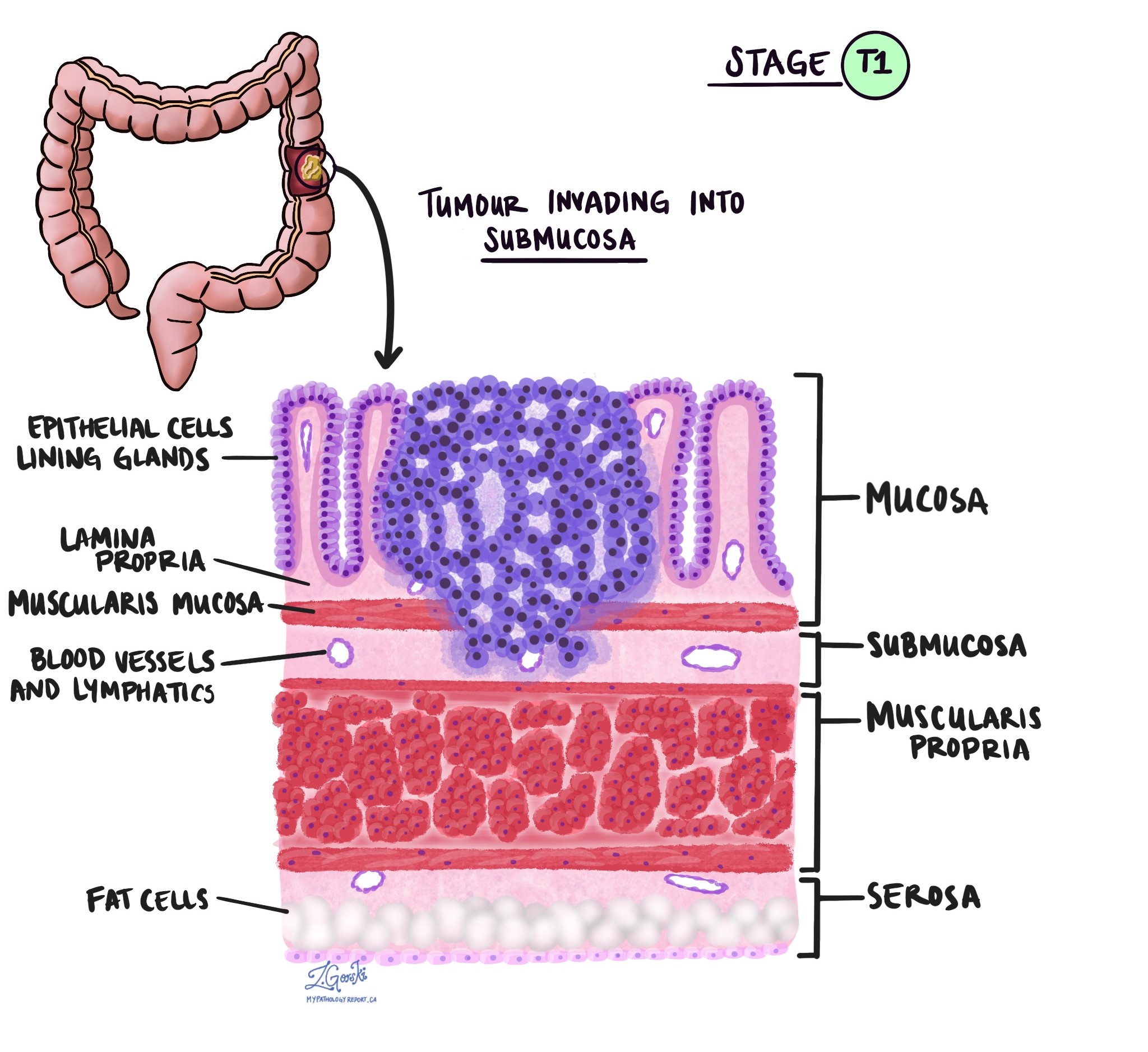
O estágio pT descreve a profundidade com que o tumor se infiltrou na parede do cólon ou nos tecidos adjacentes. A parede do cólon possui diversas camadas, de dentro para fora: mucosa, submucosa, muscular própria, subserosa e tecido adiposo circundante, além da serosa (que não está presente em todas as partes do cólon).
-
pT1 – O câncer cresceu na submucosa, que é a camada logo abaixo do revestimento interno.
-
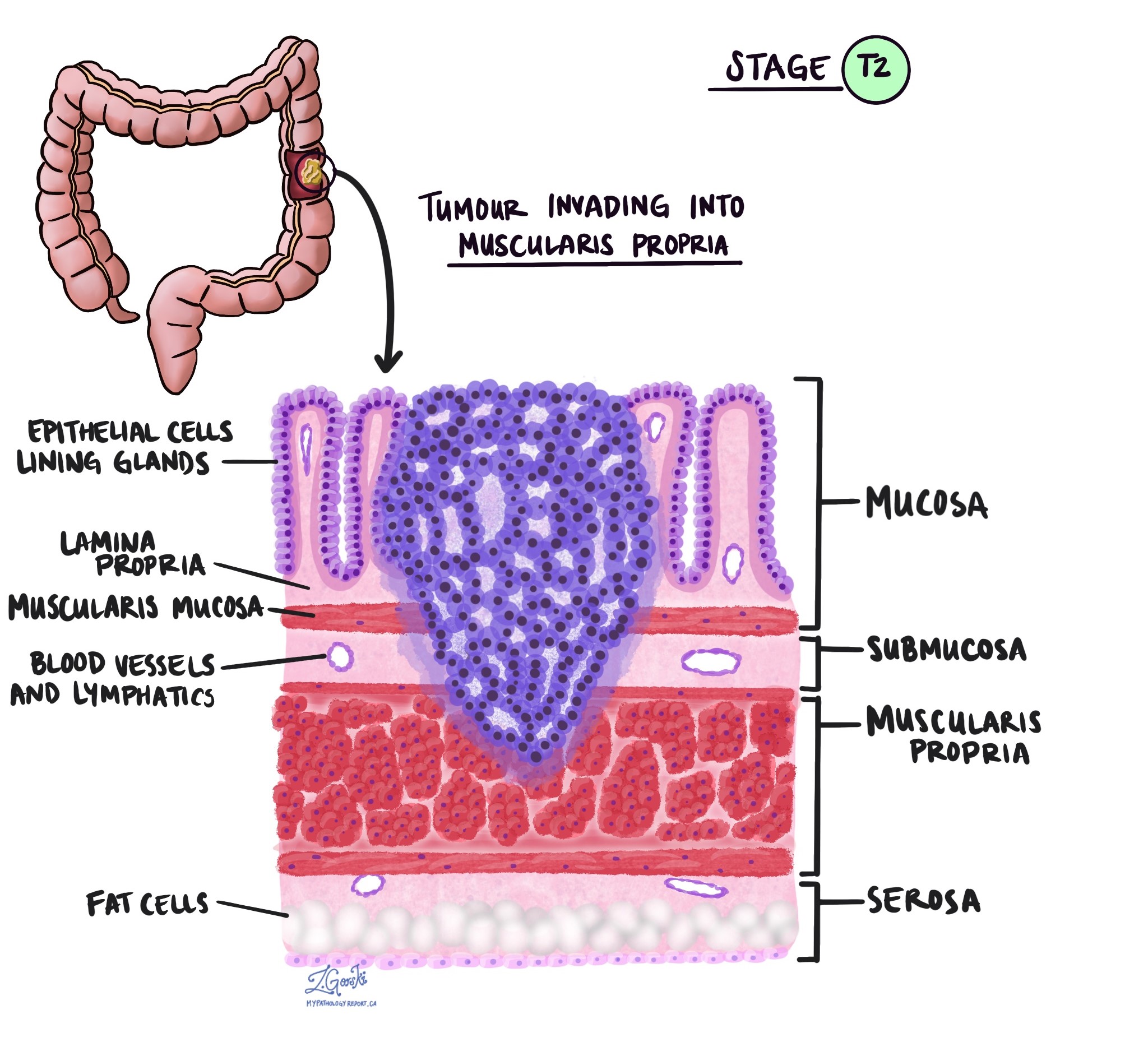
pT2 – O câncer cresceu e invadiu a muscular própria, que é a espessa camada muscular do cólon.
-
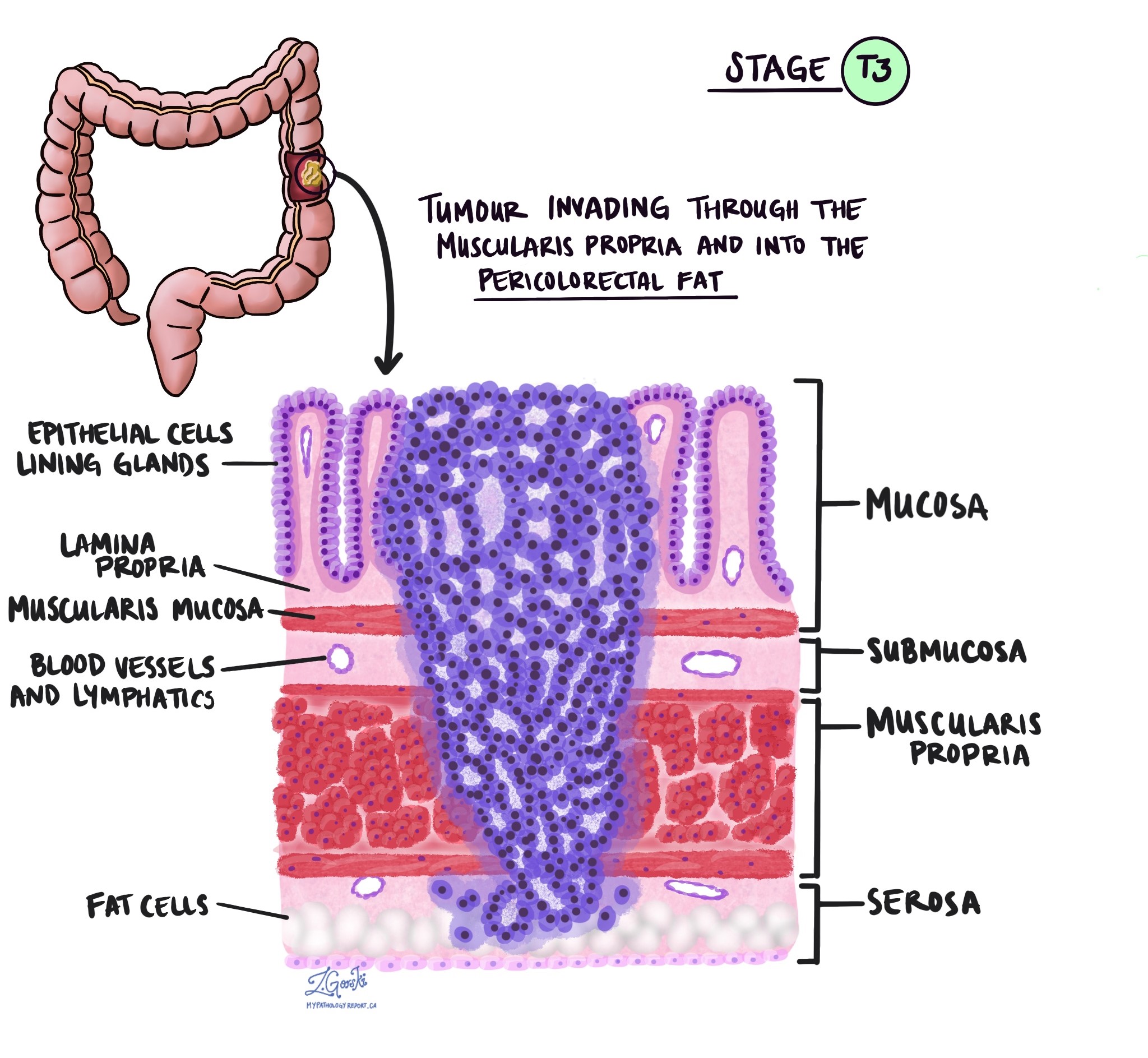
pT3 – O câncer cresceu através da muscular própria e atingiu a gordura e o tecido circundante do cólon.
-
pT4a – O câncer atingiu a superfície externa do cólon, chamada serosa, ou causou uma perfuração na parede.
-
pT4b – O câncer cresceu diretamente para órgãos ou estruturas próximas, como a bexiga, o útero ou a parede abdominal.
Estágio nodal (pN)
O estágio pN descreve se o câncer se espalhou para os linfonodos próximos.
-
pN0 – Não foi encontrado câncer em nenhum dos linfonodos examinados.
-
pN1 – O câncer é encontrado em um a três linfonodos, ou há depósitos tumorais nos tecidos circundantes, mesmo que todos os linfonodos sejam negativos.
-
pN1a – Um gânglio linfático contém câncer.
-
pN1b – Dois ou três gânglios linfáticos contêm câncer.
-
pN1c – Não há câncer nos linfonodos, mas depósitos tumorais estão presentes na gordura ou no tecido próximo ao cólon.
-
pN2 – O câncer é encontrado em quatro ou mais linfonodos.
-
pN2a – Quatro a seis gânglios linfáticos estão envolvidos.
-
pN2b – Sete ou mais gânglios linfáticos estão envolvidos.
Caso nenhum linfonodo tenha sido submetido à análise ou não tenha podido ser avaliado, o estágio pode ser listado como pNX, o que significa não avaliável.
Por que a encenação é importante?
O estadiamento ajuda o seu médico a entender o quão avançado está o câncer e qual tratamento provavelmente será mais eficaz. Estágios mais baixos, como pT1 ou pN0, sugerem doença em estágio inicial e uma maior chance de cura. Estágios mais altos, como pT4 ou pN2, sugerem doença mais avançada e um risco maior de recorrência. O estadiamento é considerado juntamente com outras características, incluindo o grau do tumor, invasão linfovascular ou perineural e resultados de biomarcadores, para orientar as decisões sobre quimioterapia e acompanhamento pós-tratamento.
O que acontece após o diagnóstico?
Após o diagnóstico, sua equipe de saúde utiliza o laudo anatomopatológico, os resultados dos exames de imagem e seu estado geral de saúde para planejar o tratamento. A equipe geralmente inclui um cirurgião, um oncologista clínico, um radiooncologista e um patologista. O tratamento depende do estágio da doença, das características do tumor e dos resultados dos biomarcadores.
Para muitos pacientes, a cirurgia para remover o segmento do cólon que contém o tumor e os linfonodos próximos é o primeiro passo. A quimioterapia pode ser recomendada após a cirurgia se o estágio ou as características do tumor sugerirem um risco maior de recorrência. Em algumas situações — especialmente para cânceres retais ou tumores de cólon muito volumosos — a quimioterapia ou a radioterapia podem ser administradas antes da cirurgia para reduzir o tamanho do tumor. Suponha que o tumor apresente biomarcadores específicos, como dMMR, amplificação de HER2 ou alterações específicas de BRAF. Nesse caso, seu oncologista pode discutir a imunoterapia ou a terapia-alvo como parte do tratamento padrão ou como parte de um ensaio clínico.
Após o tratamento, você terá acompanhamento regular, incluindo consultas na clínica, exames de sangue e exames de imagem periódicos. A colonoscopia é utilizada para detectar novos pólipos ou recidivas precoces. Se parte do cólon foi removida, sua equipe também monitorará o funcionamento intestinal, sua nutrição e os níveis de ferro ou vitaminas, além de recomendar estratégias para otimizar a recuperação.
Perguntas para fazer ao seu médico
-
Qual é o estágio e o grau do meu tumor?
-
Os gânglios linfáticos, os canais linfáticos ou os vasos sanguíneos estavam envolvidos?
-
As margens cirúrgicas estavam negativas e o tumor foi completamente removido?
-
Preciso de tratamento adicional, como quimioterapia, radioterapia, imunoterapia ou terapia direcionada?
-
O tumor foi testado para deficiência no sistema de reparo de erros de pareamento ou outros marcadores moleculares, como KRAS, NRAS, BRAF, PIK3CA, PTEN, HER2 e PD-L1?
-
Quais exames ou procedimentos de acompanhamento eu precisarei fazer e com que frequência?



