bởi Jason Wasserman MD Tiến sĩ FRCPC và Zuzanna Gorski MD
15 Tháng một, 2024
Ung thư biểu mô tuyến xâm lấn (còn được gọi là ung thư biểu mô tuyến đại tràng) là loại ung thư ruột kết phổ biến nhất. Nó được tạo thành từ các tế bào thường bao phủ bề mặt bên trong của ruột kết. Loại ung thư này thường bắt đầu ở một polyp như u tuyến ống, u tuyến tubulovillous, hoặc là u tuyến nhung.
Bài viết này sẽ giúp bạn hiểu rõ chẩn đoán và báo cáo bệnh lý về ung thư biểu mô tuyến xâm lấn đại tràng.
Dấu hai chấm
Đại tràng là một phần của hệ thống tiêu hóa và là phần đầu tiên của ruột già. Nó là một ống rỗng dài bắt đầu từ cuối ruột non và kết thúc ở trực tràng. Đại tràng được chia thành bốn phần: tăng dần (phải), ngang, giảm dần (trái) và sigmoid. Nó đóng một vai trò quan trọng trong việc xử lý các chất thải và hấp thụ nước, chất điện giải và một số vitamin. Ung thư biểu mô tuyến xâm lấn có thể phát sinh ở bất kỳ phần nào của đại tràng.
Nguyên nhân gây ung thư biểu mô tuyến xâm lấn ở đại tràng?
Ung thư biểu mô tuyến xâm lấn ở đại tràng được cho là do sự kết hợp của các yếu tố môi trường và di truyền. Các yếu tố nguy cơ được xác định bao gồm tiêu thụ quá nhiều thịt chế biến sẵn, thịt đỏ và rượu. Những người có lượng mỡ thừa trong cơ thể cũng có nguy cơ cao mắc loại ung thư này. Kéo dài viêm ở đại tràng, có thể thấy trong bệnh viêm ruột (viêm loét đại tràng và bệnh Crohn), cũng có liên quan đến việc tăng nguy cơ phát triển ung thư biểu mô tuyến xâm lấn.
Các triệu chứng của ung thư biểu mô tuyến xâm lấn của đại tràng là gì?
Các triệu chứng của ung thư biểu mô tuyến xâm lấn phụ thuộc vào vị trí của khối u trong đại tràng. Các khối u ở đại tràng trái (đại tràng xuống) hoặc trực tràng có thể gây ra những thay đổi trong thói quen đại tiện, phân có máu, đau bụng hoặc đầy hơi. Các khối u ở đại tràng phải (đại tràng lên) có thể không gây ra bất kỳ triệu chứng nào cho đến khi khối u rất lớn hoặc đã lan sang các bộ phận khác của cơ thể.
Ung thư biểu mô tuyến xâm lấn bắt đầu ở đâu trong đại tràng?
Ung thư biểu mô tuyến xâm lấn đại tràng phát sinh từ các tế bào biểu mô thường được tìm thấy ở bề mặt bên trong của đại tràng. Những tế bào biểu mô này kết nối với nhau để tạo thành các cấu trúc gọi là các tuyến. Các tuyến cùng với lớp đệm và cơ niêm bên dưới tạo thành một lớp mô mỏng gọi là niêm mạc. Khi các tế bào khối u nằm hoàn toàn trong niêm mạc, tình trạng này được gọi là chứng loạn sản cao cấp.
Chứng loạn sản cấp độ cao được coi là một tình trạng tiền ung thư không xâm lấn và các tế bào khối u không thể di căn (lây lan) sang các bộ phận cơ thể khác. Tuy nhiên, khi khối u phát triển và các tế bào xâm lấn các lớp mô bên dưới, chẩn đoán sẽ thay đổi thành ung thư biểu mô tuyến xâm lấn. Ngược lại với chứng loạn sản cấp độ cao, các tế bào khối u trong ung thư biểu mô xâm lấn có thể di căn (lan rộng) đến hạch bạch huyết và các bộ phận khác của cơ thể.

Đặc điểm vi thể của khối u này
Dưới sự kiểm tra bằng kính hiển vi, ung thư biểu mô tuyến xâm lấn của đại tràng bao gồm các nhóm bất thường các tế bào biểu mô thường được sắp xếp có kích thước không đổi các tuyến (trông có thể giống với các tuyến bình thường ở đại tràng), tổ hoặc tấm.
Những điều cần tìm trong báo cáo bệnh lý của bạn về ung thư biểu mô tuyến xâm lấn đại tràng:
Sự biệt hóa chất nhầy
Các nhà nghiên cứu bệnh học sử dụng thuật ngữ biệt hóa chất nhầy để mô tả các khối u chứa một lượng lớn tế bào ngoại bào. chất nhày. Mucin là một loại protein chuyên biệt được tạo ra bởi cả tế bào bình thường và tế bào khối u. Ngoại bào có nghĩa là mucin được nhìn thấy bên ngoài các tế bào khối u. Nếu hơn 50% khối u được tạo thành từ mucin, khối u được gọi là ung thư biểu mô tuyến niêm mạc.
Lớp mô học
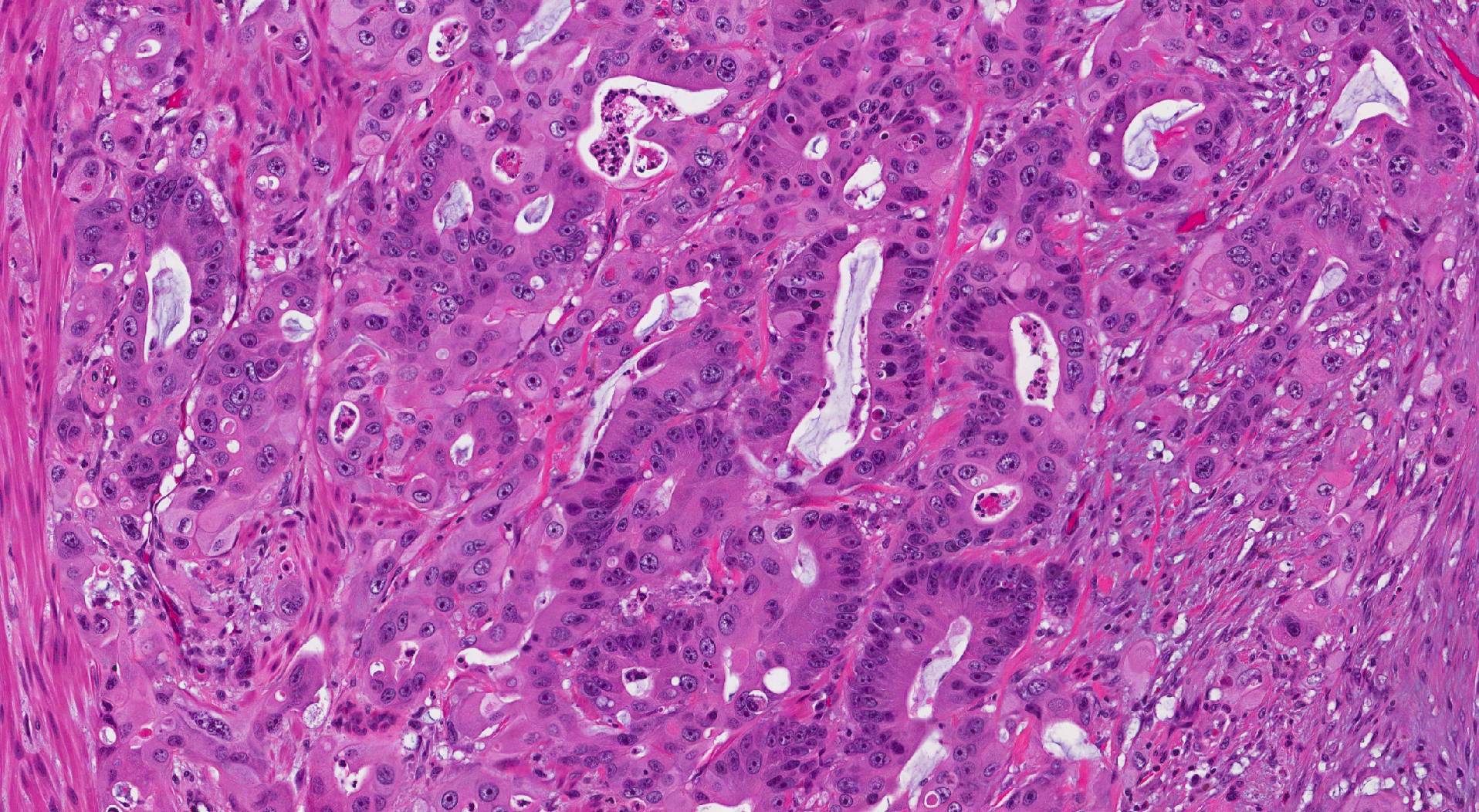
Ung thư biểu mô tuyến xâm lấn của đại tràng được chia thành ba loại - biệt hóa tốt, biệt hóa vừa và biệt hóa kém. Cấp độ được dựa trên tỷ lệ phần trăm của các tế bào khối u hình thành các cấu trúc tròn gọi là các tuyến. Một khối u không hình thành bất kỳ tuyến nào được gọi là không biệt hóa. Cấp độ này rất quan trọng vì các khối u biệt hóa kém và không biệt hóa có xu hướng hoạt động mạnh mẽ hơn; ví dụ, những khối u này có nhiều khả năng lây lan sang hạch bạch huyết và các bộ phận khác của cơ thể.
- Biệt hóa rõ: Hơn 95% khối u bao gồm các tuyến. Các nhà nghiên cứu bệnh học cũng mô tả những khối u này là loại 1.
- Biệt hóa vừa phải: 50 đến 95% khối u bao gồm các tuyến. Các nhà nghiên cứu bệnh học cũng mô tả những khối u này là loại 2.
- Biệt hóa kém: Ít hơn 50% khối u có chứa các tuyến. Các nhà nghiên cứu bệnh học cũng mô tả những khối u này là độ 3.
- Không biệt hóa: Rất ít tuyến được nhìn thấy ở bất kỳ vị trí nào trong khối u.
Độ sâu xâm lấn và giai đoạn khối u bệnh lý (pT)
Trong bệnh học, thuật ngữ cuộc xâm lăng mô tả sự lây lan của tế bào ung thư vào các cơ quan hoặc mô xung quanh vị trí khối u bắt đầu. Bởi vì ung thư biểu mô tuyến xâm lấn của đại tràng bắt đầu ở một lớp mô mỏng ở bề mặt bên trong của đại tràng gọi là niêm mạc, sự xâm lấn được định nghĩa là sự lây lan của các tế bào ung thư vào các lớp mô khác trong đại tràng hoặc bất kỳ cơ quan nào khác bên ngoài đại tràng. Sự xâm lấn chỉ có thể được nhìn thấy sau khi khối u đã được bác sĩ giải phẫu bệnh kiểm tra dưới kính hiển vi.
Khi kiểm tra khối u dưới kính hiển vi, bác sĩ giải phẫu bệnh sẽ xem các tế bào ung thư đã lan rộng từ niêm mạc đến các mô xung quanh bao xa. Đây được gọi là độ sâu hoặc mức độ xâm lấn. Độ sâu xâm lấn rất quan trọng vì các khối u xâm lấn sâu hơn vào thành đại tràng có nhiều khả năng lan sang các bộ phận khác của cơ thể, chẳng hạn như hạch bạch huyết, gan hoặc phổi. Mức độ xâm lấn cũng được sử dụng để xác định giai đoạn khối u bệnh lý (pT). Những hình ảnh dưới đây cho thấy mối liên quan giữa độ sâu xâm lấn và giai đoạn bệnh lý của khối u.
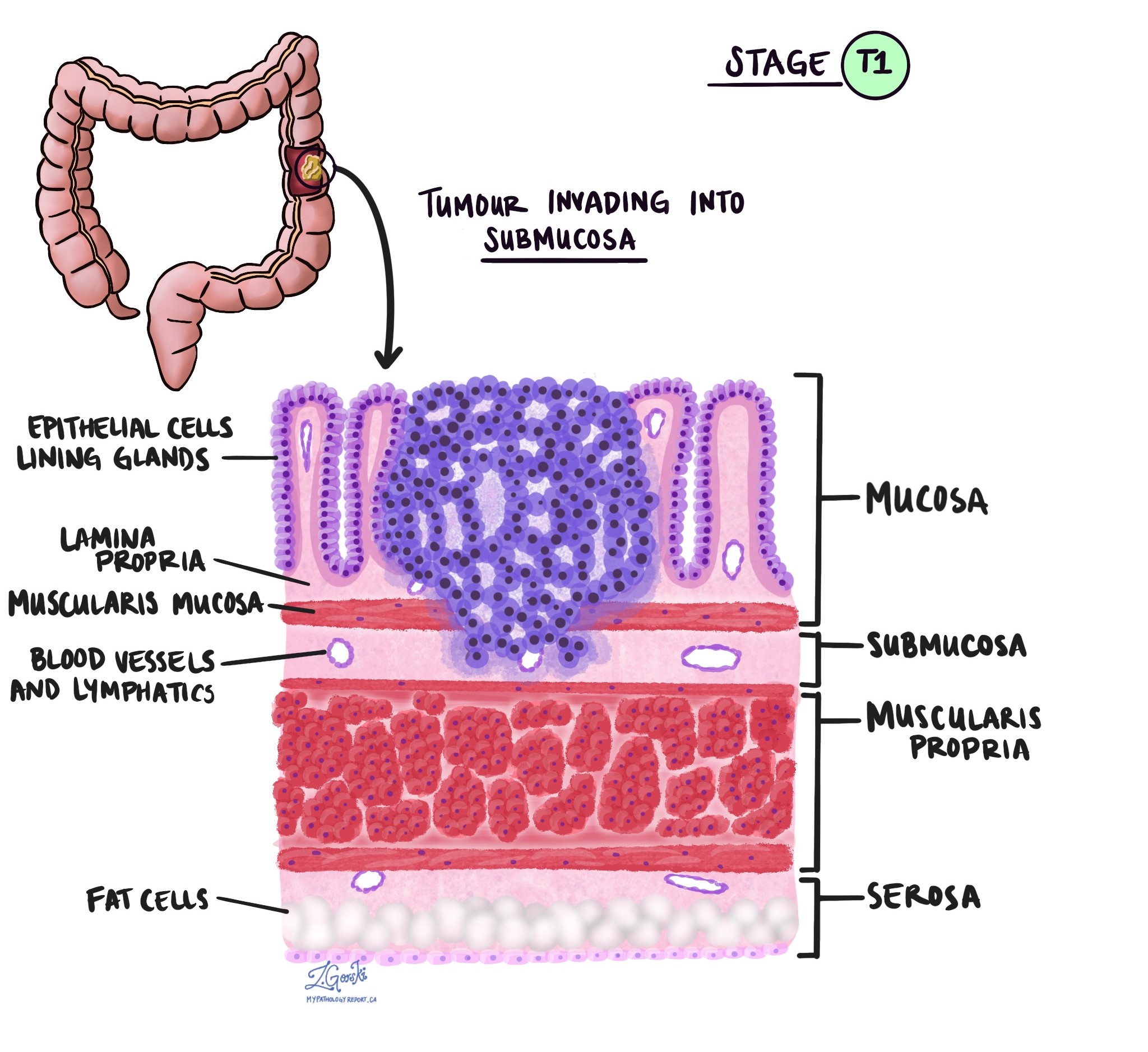
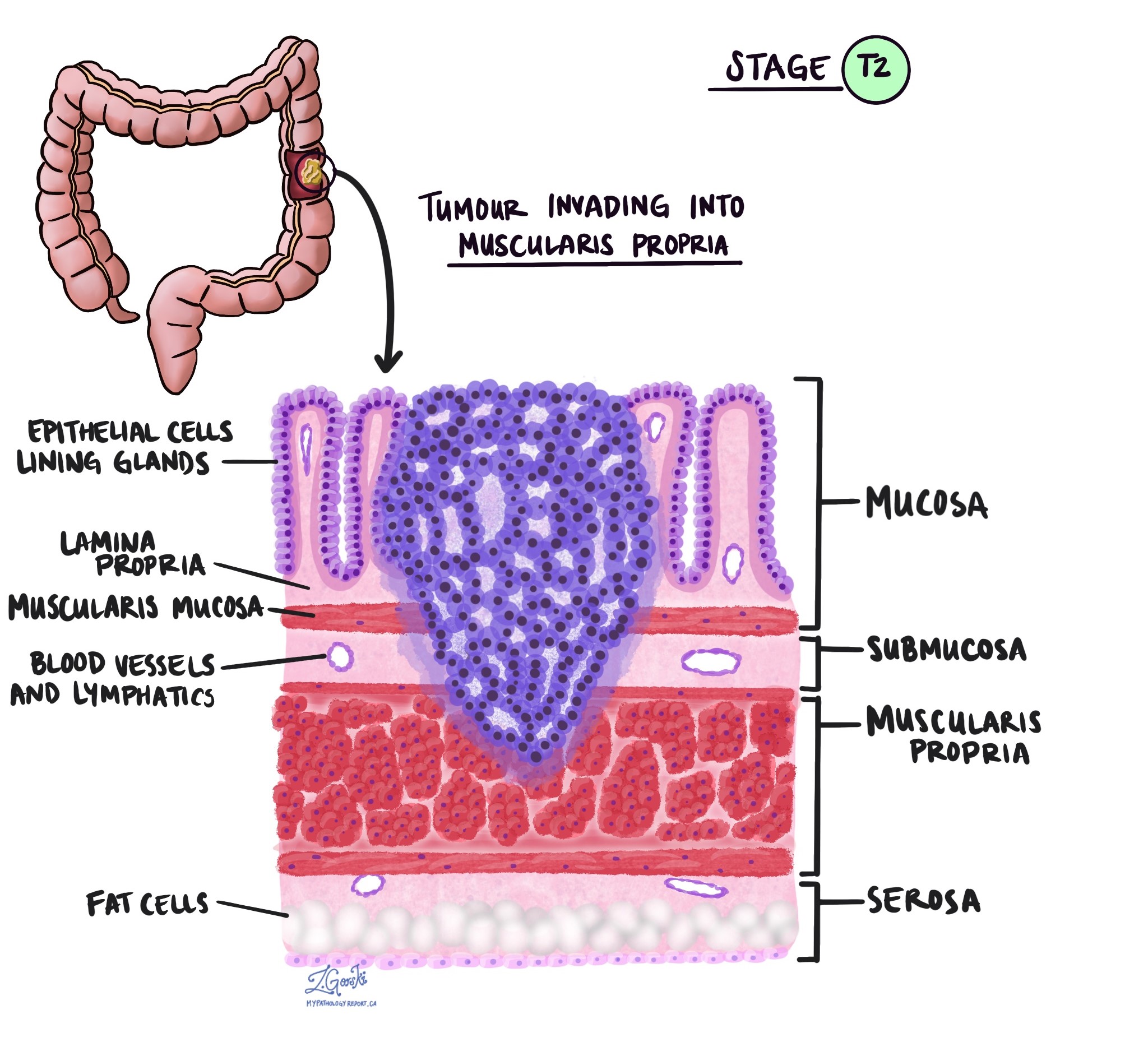
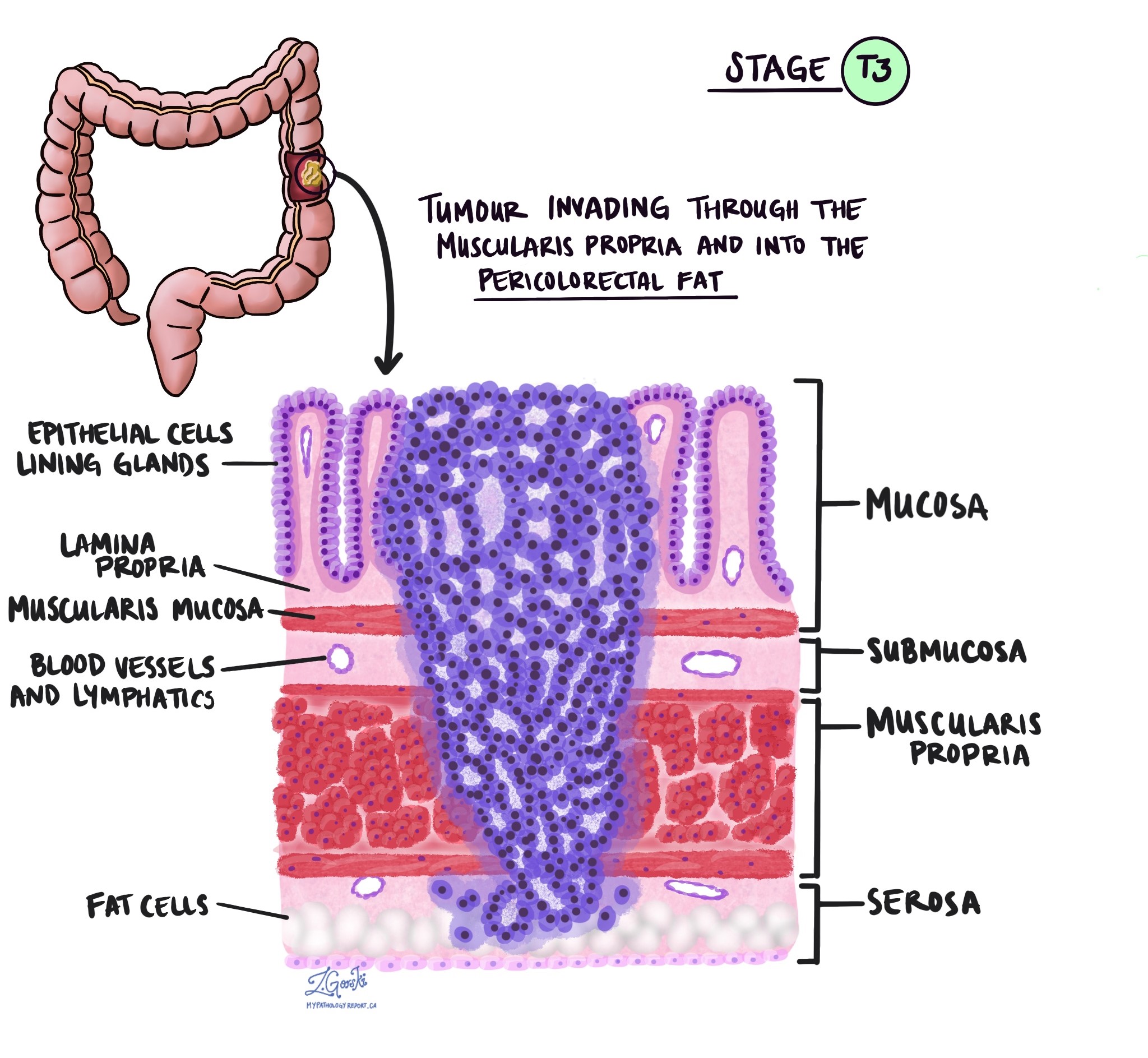
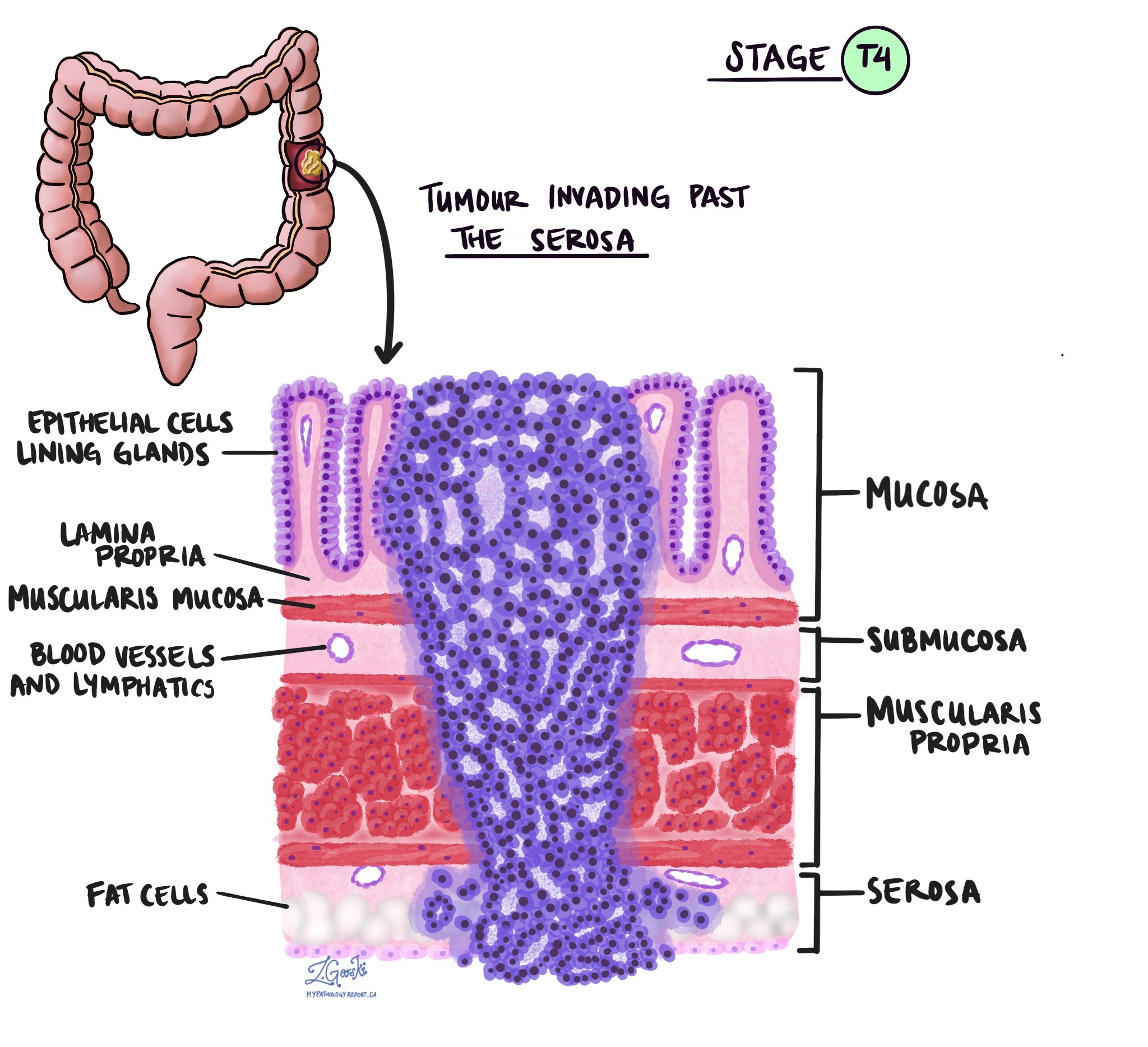
Sự xâm lấn quanh dây thần kinh
Các nhà nghiên cứu bệnh học sử dụng thuật ngữ “xâm lấn quanh dây thần kinh” để mô tả tình trạng tế bào ung thư bám vào hoặc xâm lấn dây thần kinh. “Xâm lấn nội thần kinh” là một thuật ngữ liên quan đặc biệt đề cập đến các tế bào ung thư được tìm thấy bên trong dây thần kinh. Dây thần kinh, giống như những sợi dây dài, bao gồm các nhóm tế bào được gọi là tế bào thần kinh. Những dây thần kinh này hiện diện khắp cơ thể, truyền thông tin như nhiệt độ, áp suất và cơn đau giữa cơ thể và não. Sự hiện diện của sự xâm lấn quanh dây thần kinh rất quan trọng vì nó cho phép các tế bào ung thư di chuyển dọc theo dây thần kinh vào các cơ quan và mô lân cận, làm tăng nguy cơ khối u tái phát sau phẫu thuật.
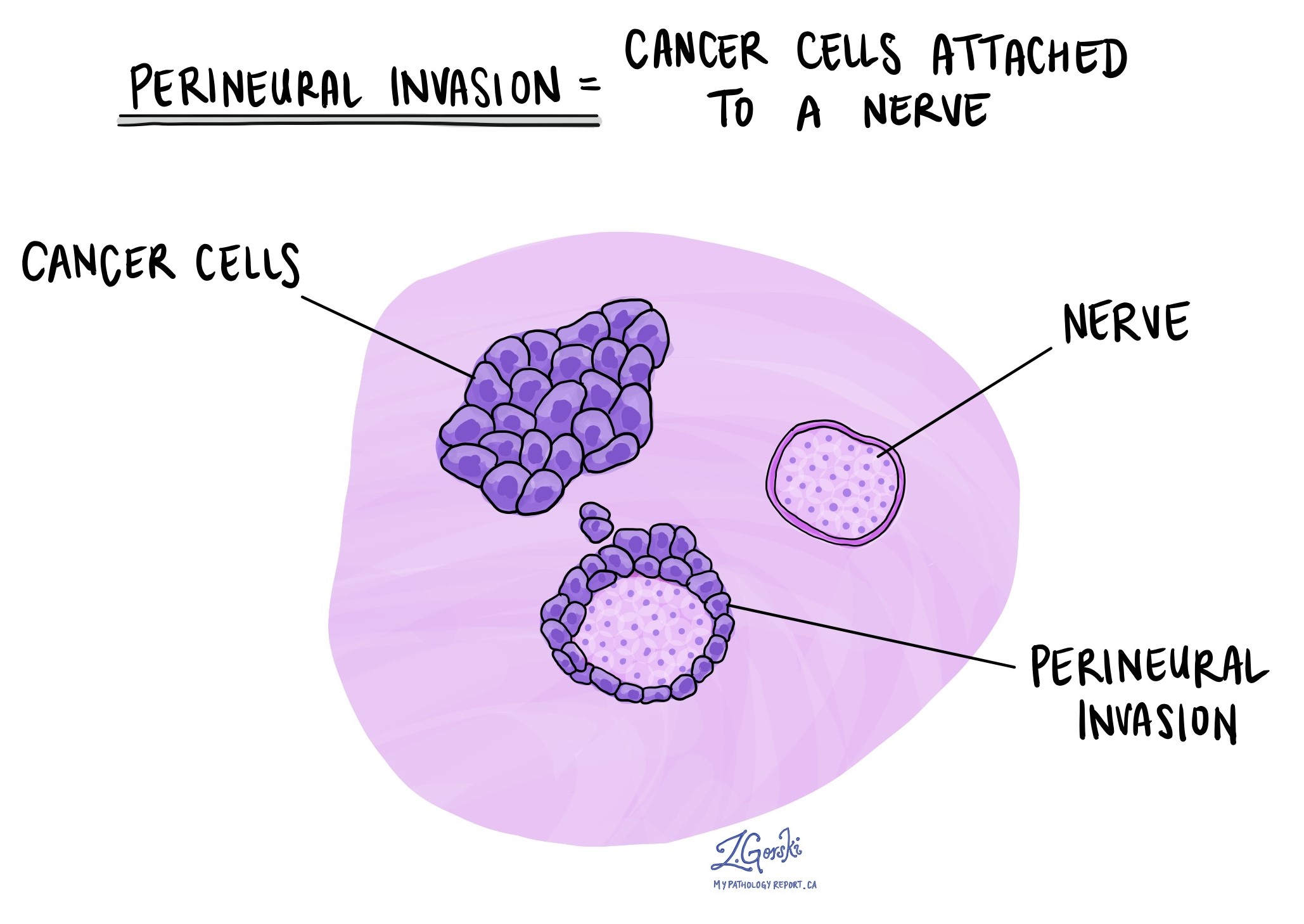
Xâm lấn mạch bạch huyết
Sự xâm lấn mạch bạch huyết xảy ra khi các tế bào ung thư xâm lấn mạch máu hoặc mạch bạch huyết. Mạch máu là những ống mỏng mang máu đi khắp cơ thể, trong khi mạch bạch huyết mang chất lỏng gọi là bạch huyết thay vì máu. Những mạch bạch huyết này kết nối với các cơ quan miễn dịch nhỏ nằm rải rác khắp cơ thể, được gọi là hạch bạch huyết.
Sự xâm lấn mạch bạch huyết rất quan trọng vì nó cho phép các tế bào ung thư lan sang các bộ phận khác của cơ thể, bao gồm các hạch bạch huyết hoặc gan, qua máu hoặc mạch bạch huyết. Ngoài ra, sự hiện diện của các tế bào ung thư bên trong tĩnh mạch lớn ngoài thành đại tràng (bên ngoài bó cơ dày) có liên quan đến nguy cơ cao là các tế bào ung thư cuối cùng sẽ được tìm thấy trong gan.

Lề
Trong bệnh lý học, rìa là phần rìa của mô được loại bỏ trong quá trình phẫu thuật khối u. Trạng thái lề trong báo cáo bệnh lý rất quan trọng vì nó cho biết liệu toàn bộ khối u đã được cắt bỏ hay còn sót lại một số. Thông tin này giúp xác định nhu cầu điều trị thêm.
Các nhà nghiên cứu bệnh học thường đánh giá tỷ lệ lợi nhuận sau một thủ tục phẫu thuật giống như cắt bỏ or sự cắt bỏ, nhằm mục đích loại bỏ toàn bộ khối u. Lợi nhuận thường không được đánh giá sau một sinh thiết, chỉ loại bỏ một phần của khối u. Số lượng lề được báo cáo và kích thước của chúng – bao nhiêu mô bình thường nằm giữa khối u và mép cắt – thay đổi tùy theo loại mô và vị trí khối u.
Các nhà nghiên cứu bệnh học kiểm tra lề để kiểm tra xem các tế bào khối u có hiện diện ở mép cắt của mô hay không. Tỷ lệ dương, nơi tìm thấy tế bào khối u, cho thấy một số bệnh ung thư có thể vẫn còn trong cơ thể. Ngược lại, biên độ âm, không có tế bào khối u ở rìa, cho thấy khối u đã được loại bỏ hoàn toàn. Một số báo cáo cũng đo khoảng cách giữa các tế bào khối u gần nhất và rìa, ngay cả khi tất cả các lề đều âm tính.

Khối u vừa chớm nở
Khối u vừa chớm nở là thuật ngữ mà các nhà nghiên cứu bệnh học sử dụng để mô tả các tế bào ung thư đơn lẻ hoặc các nhóm nhỏ tế bào ung thư nhìn thấy ở rìa khối u. Nó được cho là dấu hiệu cho thấy khối u đang trở nên ít biệt hóa hơn. Dựa trên số lượng chồi nhìn thấy dưới kính hiển vi, người ta sẽ cho điểm thấp, trung bình hoặc cao. Điểm cao có liên quan đến nguy cơ gia tăng các tế bào ung thư sẽ lan sang bộ phận khác của cơ thể.
Hiệu quả điều trị
Nếu bạn được điều trị ung thư (hóa trị hoặc xạ trị hoặc cả hai) trước khi cắt bỏ khối u, bác sĩ giải phẫu bệnh sẽ kiểm tra cẩn thận khu vực mô nơi khối u được xác định trước đó để xem liệu có tế bào ung thư nào còn sống (khả năng sống sót) hay không. Hệ thống được sử dụng phổ biến nhất mô tả hiệu quả điều trị theo thang điểm từ 0 đến 3, với 0 là không có tế bào ung thư còn sống (tất cả các tế bào ung thư đã chết) và 3 là ung thư còn sót lại trên diện rộng mà không có sự thoái triển rõ ràng của khối u (tất cả hoặc hầu hết tế bào ung thư còn sống).
Tiền gửi khối u
Tiền gửi khối u là một nhóm tế bào ung thư tách biệt với khối u chính nhưng không nằm trong hạch bạch huyết. Sự tích tụ khối u có liên quan đến nguy cơ cao hơn là các tế bào khối u sẽ lan sang một bộ phận khác của cơ thể, chẳng hạn như gan hoặc phổi, sau khi điều trị. Sự lắng đọng khối u cũng xác định giai đoạn khối u bệnh lý (pT).
Hạch bạch huyết
Các cơ quan miễn dịch nhỏ, được gọi là hạch bạch huyết, nằm khắp cơ thể. Tế bào ung thư có thể di chuyển từ khối u đến các hạch bạch huyết này thông qua các mạch bạch huyết nhỏ. Vì lý do này, các bác sĩ thường loại bỏ và kiểm tra các hạch bạch huyết bằng kính hiển vi để tìm tế bào ung thư. Quá trình này, trong đó các tế bào ung thư di chuyển từ khối u ban đầu đến một bộ phận cơ thể khác như hạch bạch huyết, được gọi là di căn.
Các tế bào ung thư đầu tiên thường di chuyển đến các hạch bạch huyết gần khối u, mặc dù các hạch bạch huyết ở xa cũng có thể bị ảnh hưởng. Do đó, bác sĩ phẫu thuật thường loại bỏ các hạch bạch huyết gần khối u nhất trước tiên. Họ có thể loại bỏ các hạch bạch huyết ở xa khối u hơn nếu chúng to ra và có sự nghi ngờ mạnh mẽ rằng chúng có chứa tế bào ung thư.
Các nhà nghiên cứu bệnh học sẽ kiểm tra bất kỳ hạch bạch huyết nào bị loại bỏ dưới kính hiển vi và kết quả sẽ được trình bày chi tiết trong báo cáo của bạn. Kết quả “dương tính” cho thấy sự hiện diện của tế bào ung thư trong hạch bạch huyết, trong khi kết quả “âm tính” có nghĩa là không tìm thấy tế bào ung thư. Nếu báo cáo tìm thấy các tế bào ung thư trong một hạch bạch huyết, nó cũng có thể chỉ định kích thước của cụm tế bào lớn nhất này, thường được gọi là “tập trung” hoặc “tiền gửi”. Sự lan rộng ra ngoài hạch xảy ra khi các tế bào khối u xâm nhập vào bao ngoài của hạch và lan sang các mô lân cận.
Kiểm tra các hạch bạch huyết là quan trọng vì hai lý do. Đầu tiên, nó giúp xác định giai đoạn hạch bệnh lý (pN). Thứ hai, việc phát hiện ra các tế bào ung thư trong một hạch bạch huyết cho thấy nguy cơ tìm thấy các tế bào ung thư ở các bộ phận khác của cơ thể sau này sẽ tăng lên. Thông tin này hướng dẫn bác sĩ quyết định xem bạn có cần điều trị bổ sung hay không, chẳng hạn như hóa trị, xạ trị hoặc liệu pháp miễn dịch.
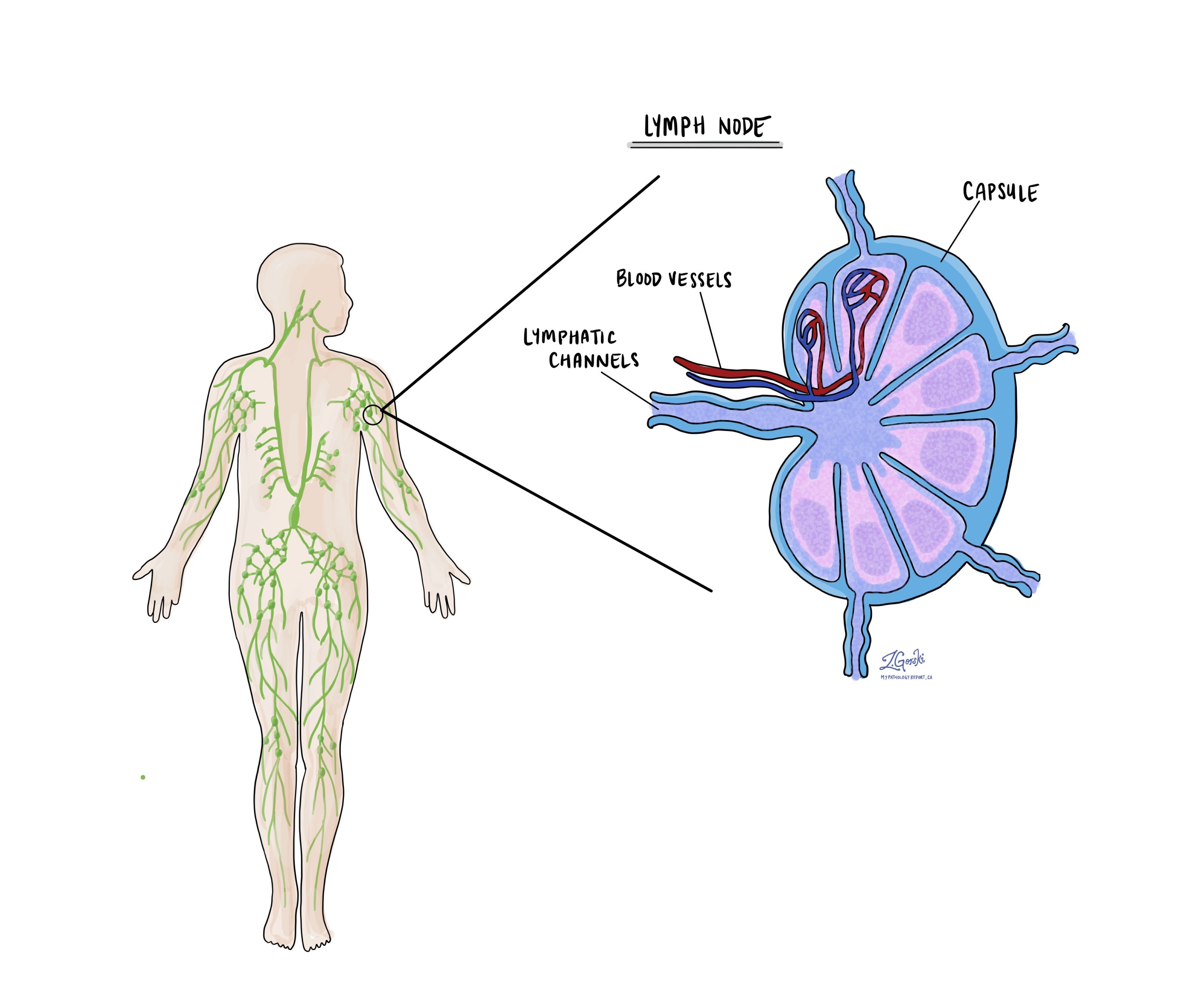
Protein sửa chữa không phù hợp
Sửa chữa không khớp (MMR) là một hệ thống bên trong tất cả các tế bào khỏe mạnh, bình thường nhằm sửa chữa các lỗi trong vật liệu di truyền (DNA) của chúng ta. Hệ thống này được tạo thành từ các loại protein khác nhau và bốn loại phổ biến nhất là MSH2, MSH6, MLH1 và PMS2.
Bốn protein sửa chữa không khớp MSH2, MSH6, MLH1 và PMS2 hoạt động theo cặp để sửa chữa DNA bị hỏng. Cụ thể, MSH2 hoạt động với MSH6 và MLH1 hoạt động với PMS2. Nếu một protein bị mất, cặp protein này không thể hoạt động bình thường và nguy cơ phát triển ung thư sẽ tăng lên.
Làm thế nào để các nhà nghiên cứu bệnh học kiểm tra các protein sửa chữa không phù hợp?
Cách phổ biến nhất để kiểm tra các protein sửa chữa không khớp là hóa mô miễn dịch. Thử nghiệm này cho phép các nhà nghiên cứu bệnh học xem liệu các tế bào khối u có tạo ra tất cả bốn loại protein sửa chữa không khớp hay không. Kết quả của thử nghiệm này thường được báo cáo như sau:
- Kết quả bình thường: Biểu hiện protein được giữ lại.
- Kết quả bất thường: Mất biểu hiện protein.
Tại sao xét nghiệm các protein sửa chữa không phù hợp lại quan trọng?
Thử nghiệm sửa chữa không phù hợp rất quan trọng vì nó có thể giúp dự đoán mức độ hiệu quả của một số phương pháp điều trị. Ví dụ, những bệnh ung thư bị mất biểu hiện protein sửa chữa không khớp có nhiều khả năng đáp ứng với các phương pháp điều trị bằng liệu pháp miễn dịch như thuốc ức chế PD-1 hoặc PD-L1. Điều này là do số lượng đột biến cao thường thấy ở các khối u thiếu hụt có thể tạo ra các kháng nguyên mới khiến khối u dễ lộ rõ hơn và dễ bị tổn thương trước hệ thống miễn dịch.
Thử nghiệm sửa chữa không khớp cũng được thực hiện để xác định những bệnh nhân có thể mắc hội chứng Lynch, còn được gọi là ung thư đại trực tràng không polyp di truyền (HNPCC). Hội chứng Lynch là một rối loạn di truyền làm tăng nguy cơ phát triển nhiều loại ung thư, bao gồm ung thư thực quản, ung thư ruột kết, ung thư nội mạc tử cung, ung thư buồng trứng và ung thư dạ dày.
Những thay đổi di truyền khác được tìm thấy trong ung thư biểu mô tuyến xâm lấn của đại tràng và trực tràng
- Đột biến gen APC (Adenomatous Polyposis Coli): Hầu như phổ biến trong các trường hợp ung thư ruột kết lẻ tẻ, đột biến gen APC thường là sự kiện sớm trong quá trình phát triển của ung thư đại trực tràng. Gen APC là gen ức chế khối u và việc nó bất hoạt sẽ dẫn đến sự phát triển tế bào bất thường.
- Đột biến KRAS và NRAS: Đột biến ở gen KRAS và NRAS, một phần của họ gen RAS, xảy ra ở khoảng 40-45% bệnh ung thư đại trực tràng. Những đột biến này dẫn đến sự phân chia và tăng trưởng tế bào không kiểm soát được. Đặc biệt, sự hiện diện của đột biến KRAS có liên quan đến khả năng kháng một số liệu pháp kháng EGFR (thụ thể yếu tố tăng trưởng biểu bì).
- Đột biến BRAF: Đột biến gen BRAF, đặc biệt là V600E, được tìm thấy ở khoảng 10% trường hợp ung thư đại trực tràng. Nó thường liên quan đến tiên lượng xấu và khả năng kháng một số phương pháp điều trị. Đột biến BRAF phổ biến hơn ở các bệnh ung thư phát triển theo con đường răng cưa.
- Đột biến PIK3CA: Đột biến trong gen PIK3CA, mã hóa cho một tiểu đơn vị phosphatidylinositol 3-kinase (PI3K), xảy ra ở khoảng 10-20% bệnh ung thư đại trực tràng. Những đột biến này có thể kích hoạt đường truyền tín hiệu AKT, thúc đẩy sự tăng sinh và sống sót của tế bào.
Các xét nghiệm được sử dụng để phát hiện những thay đổi di truyền
- Giải trình tự thế hệ tiếp theo (NGS): NGS cho phép kiểm tra đồng thời nhiều gen để phát hiện đột biến, xóa và khuếch đại. Cách tiếp cận toàn diện này có thể đánh giá tất cả các thay đổi di truyền phổ biến trong ung thư đại trực tràng, bao gồm các đột biến APC, KRAS, NRAS, BRAF và PIK3CA.
- Phản ứng chuỗi polymerase (PCR): Kỹ thuật này khuếch đại các đoạn DNA, giúp phân tích các thay đổi di truyền cụ thể, chẳng hạn như đột biến KRAS, NRAS và BRAF.
- Lai huỳnh quang tại chỗ (FISH): FISH có thể xác định các bất thường về di truyền như khuếch đại hoặc xóa trong các gen cụ thể. Nó ít được sử dụng hơn để phát hiện thường xuyên những thay đổi di truyền được đề cập nhưng có thể hữu ích trong những bối cảnh cụ thể.
Về bài viết này
Các bác sĩ viết bài này để giúp bạn đọc và hiểu báo cáo bệnh lý của mình. Liên hệ với chúng tôi nếu bạn có thắc mắc về bài viết này hoặc báo cáo bệnh lý của bạn. Để có phần giới thiệu đầy đủ về báo cáo bệnh lý của bạn, hãy đọc bài viết này.