de Jason Wasserman MD PhD FRCPC
Noiembrie 16, 2023
Carcinomul lobular invaziv este un tip de cancer mamar. Carcinomul lobular invaziv începe de obicei de la o creștere non-canceroasă a celulelor mamare anormale numite carcinom lobular in situ (LCIS). LCIS poate fi prezent luni sau ani înainte de a se transforma în carcinom lobular invaziv. În plus, pacienții cu un diagnostic anterior de LCIS au un risc mai mare de a dezvolta carcinom lobular invaziv.
Cum se pune acest diagnostic?
Diagnosticul de carcinom lobular invaziv se face de obicei după ce o mică probă de tumoră este îndepărtată printr-o procedură numită biopsie. Țesutul este apoi trimis unui patolog pentru examinare la microscop.
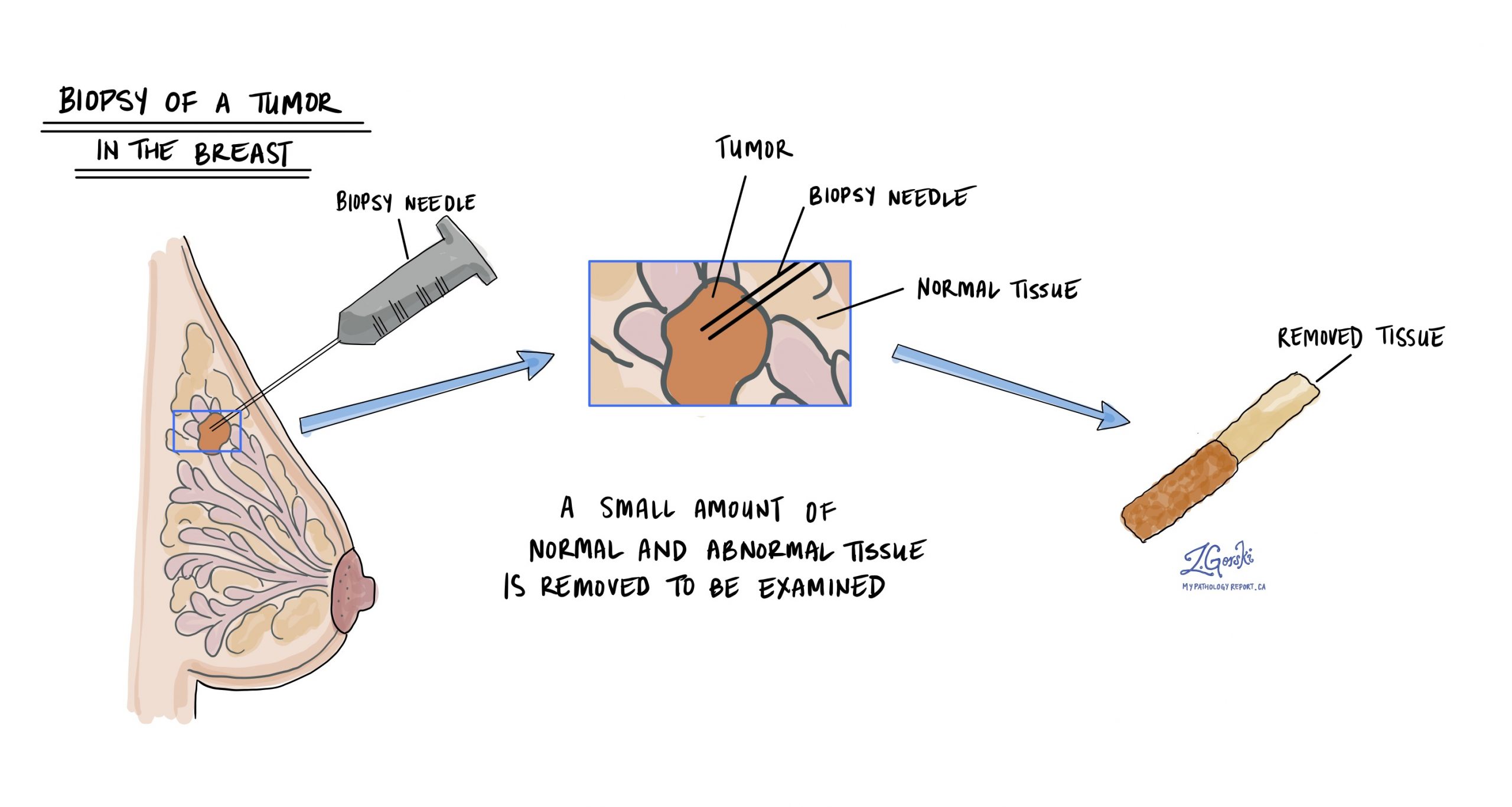
Ce înseamnă dacă tumora este descrisă ca tip clasic sau tip pleomorf?
Patologii împart carcinomul lobular invaziv în două tipuri - tipul clasic și tipul pleomorf - pe baza modului în care arată celulele canceroase atunci când sunt examinate la microscop. Tipul tumorii este important, deoarece este mai probabil ca carcinomul lobular invaziv de tip pleomorf metastazeaza (transmite catre noduli limfatici și alte părți ale corpului.
- Tip clasic – Acesta este cel mai frecvent tip de carcinom lobular invaziv. Celulele canceroase sunt mici și călătoresc prin țesut ca celule unice (nu sunt atașate de celelalte celule canceroase).
- tip pleomorf – Celulele canceroase din tipul pleomorf sunt mai mari și cu aspect mai anormal decât celulele din tipul clasic. The nucleu al celulei (partea celulei care deține cea mai mare parte a materialului genetic) este de asemenea hipercromatic (mai întunecat) și mai mare decât nucleul la tipul clasic.
Care este gradul histologic Nottingham pentru carcinomul lobular invaziv și de ce este important?
Patologii folosesc un sistem numit sistem de clasificare Nottingham pentru a împărți carcinomul lobular invaziv în trei niveluri sau grade – 1, 2 și 3. Gradul este important, deoarece tumorile de gradul 2 și de gradul 3 tind să crească mai rapid și sunt mai probabil să se răspândească la alte părți ale corpului cum ar fi noduli limfatici.
Cum determină patologii gradul Nottingham pentru carcinomul lobular invaziv?
Gradul poate fi determinat numai după ce tumora este examinată la microscop. Când examinează tumora, patologii caută următoarele trei caracteristici microscopice:
- Tubule – Un tubul este un grup de celule conectate pentru a forma o structură rotundă, asemănătoare unui inel. Tubulii arată asemănător, dar nu sunt la fel ca glande care se găsesc în mod normal în sân. Se acordă un scor de la 1 la 3 pe baza procentului de celule canceroase care formează tubuli. Tumorilor formate în mare parte din tubuli li se acordă un scor de 1, în timp ce tumorilor formate din foarte puține glande li se acordă un scor de 3. Celulele din carcinomul lobular invaziv nu formează glande și primesc întotdeauna un scor de 3 pentru această caracteristică.
- Pleomorfismul nuclear - nucleu este o parte a celulei care deține cea mai mare parte a materialului genetic al celulei (ADN). Pleomorfismul (sau pleomorf) este un cuvânt pe care patologii îl folosesc atunci când nucleul unei celule tumorale arată foarte diferit de nucleul unei alte celule tumorale. Se acordă un scor de la 1 la 3 pentru pleomorfismul nuclear. Când majoritatea celulelor canceroase sunt mici și arată foarte asemănător între ele, tumorii primește un scor de 1. Când celulele canceroase sunt foarte mari și au aspect anormal, tumorii primesc un scor de 3.
- Rata mitotică - Celulele se divid pentru a crea celule noi. Procesul de creare a unei noi celule se numește mitoză, iar o celulă care se împarte se numește a figura mitotică. Patologul dumneavoastră va număra numărul de figuri mitotice dintr-o anumită zonă (numită câmp de mare putere) și va folosi acest număr pentru a da un scor între 1 și 3. Tumorilor cu foarte puține figuri mitotice li se acordă un scor de 1, în timp ce celor cu multor figuri mitotice li se acordă un scor de 3.
Se adaugă punctajul din fiecare categorie pentru a determina nota generală, după cum urmează:
- Grad 1 (grad scăzut) - Scor de 3, 4 sau 5.
- Clasa 2 (clasa mare) – scor 6 sau 7.
- Clasa 3 (clasa mare) – scor 8 sau 9.
De ce este importantă dimensiunea tumorii?
Mărimea unei tumori mamare este importantă deoarece este utilizată pentru a determina stadiul patologic al tumorii (pT) și pentru că tumorile mai mari au mai multe șanse să metastazeze (se răspândească) la noduli limfatici și alte părți ale corpului. Mărimea tumorii poate fi determinată numai după ce întreaga tumoră a fost îndepărtată. Din acest motiv, nu va fi inclus în raportul dumneavoastră de patologie după a biopsie.
Ce sunt markerii de prognostic mamar și de ce sunt ei importanți?
Markerii de prognostic sunt proteine sau alte elemente biologice care pot fi măsurate pentru a ajuta la prezicerea modului în care o boală precum cancerul se va comporta în timp și cum va răspunde la tratament. Cei mai frecvent testați markeri de prognostic la sân sunt receptorii hormonali receptor de estrogen (ER) și receptor de progesteron (PR) și factorul de creștere HER2.
Receptorii hormonali – ER și PR
ER și PR sunt receptori hormonali care permit celulelor să răspundă la acțiunile hormonilor sexuali estrogen și progesteron. ER și PR sunt produse de celulele mamare normale și de unele cancere de sân. Cancerele care fac ER și PR sunt descrise ca fiind „sensibile la hormoni”, deoarece depind de acești hormoni pentru a crește.
Patologii efectuează adesea un test numit imunohistochimie pentru a vedea dacă celulele tumorii din carcinomul lobular invaziv produc ER și PR. Acest test este adesea efectuat pe biopsie probă. Cu toate acestea, în unele situații, poate fi efectuată numai după îndepărtarea întregii tumori.
Patologii determină scorul ER și PR măsurând procentul de celule tumorale care au proteine într-o parte a celulei numită nucleu și intensitatea petelor. Cele mai multe rapoarte oferă un interval pentru procentul de celule care arată pozitivitate nucleară, în timp ce intensitatea este descrisă ca slabă, moderată sau ridicată.
HER2
HER2 este o proteină care este produsă de celule normale, sănătoase din întregul corp. Celulele tumorale din unele tipuri de cancer produc HER2 suplimentar și acest lucru permite celulelor tumorii să crească mai repede decât celulele normale.
Două teste sunt efectuate în mod obișnuit pentru a măsura cantitatea de HER2 în carcinomul lobular invaziv. Se numește primul test imunohistochimie și permite patologului dumneavoastră să vadă proteina HER2 de pe suprafața celulei. Acest test primește un scor de la 0 la 3.
Scorul imunohistochimic HER2:
- Negativ (0 și 1) – Un scor de 0 sau 1 înseamnă că celulele tumorale nu produc proteină HER2 suplimentară.
- echivoc (2) – Un scor de 2 înseamnă că celulele pot produce proteină HER2 suplimentară și se numește un alt test hibridizarea in situ a fluorescenței (vezi mai jos) va trebui efectuată pentru a confirma rezultatele.
- Pozitiv (3) – Un scor de 3 înseamnă că celulele produc proteină HER2 suplimentară.
Al doilea test care este folosit pentru a măsura HER2 se numește hibridizare fluorescentă in situ (FISH). Acest test este de obicei efectuat numai după un scor de 2 la testul de imunohistochimie. În loc să caute HER2 în exteriorul celulei, FISH folosește o sondă care se lipește de gena HER2 în interiorul nucleului celulei. Celulele normale au 2 copii ale genei HER2 în nucleul celulei. Scopul testului HER FISH este de a identifica celulele tumorale care au mai multe copii ale genei HER2, ceea ce le permite să facă mai multe copii ale proteinei HER2.
Scorul HER2 FISH:
- Pozitiv (amplificat) – Celulele tumorale au copii suplimentare ale genei HER2. Cel mai probabil, aceste celule produc proteine HER2 suplimentare.
- Negativ (neamplificat) – Celulele tumorale nu au copii suplimentare ale genei HER2. Cel mai probabil, aceste celule nu produc proteine HER2 suplimentare.
Ce este carcinomul lobular in situ și cum este legat de carcinomul lobular invaziv?
Carcinom lobular in situ (LCIS) este non-invaziva tumoră care apare înainte de dezvoltarea carcinomului lobular invaziv. Deoarece LCIS duce la carcinom lobular invaziv, este obișnuit ca patologii să găsească LCIS și carcinom lobular invaziv în același țesut.
Ce înseamnă extensia tumorii și de ce este importantă?
Carcinomul lobular invaziv începe în interiorul sânului, dar tumora se poate răspândi în pielea de deasupra sau în mușchii peretelui toracic. Termenul de extensie tumorală este folosit atunci când celulele tumorale se găsesc fie în piele, fie în mușchii de sub sân. Extensia tumorii este importantă deoarece este asociată cu un risc mai mare ca tumora să crească înapoi după tratament (recurență locală) sau ca celulele canceroase să se deplaseze către un loc îndepărtat al corpului, cum ar fi plămânul. Extensia tumorii este, de asemenea, utilizată pentru a determina stadiul tumoral patologic (pT).
Ce este invazia limfovasculară și de ce este importantă?
Invazia limfovasculară înseamnă că celulele canceroase au fost văzute în interiorul unui vas de sânge sau vas limfatic. Vasele de sânge sunt tuburi lungi și subțiri care transportă sânge în jurul corpului. Vasele limfatice sunt similare cu vasele de sânge mici, cu excepția faptului că transportă un lichid numit limfă în loc de sânge. Vasele limfatice se conectează cu mici organe imunitare numite noduli limfatici care se găsesc în tot corpul. Invazia limfovasculară este importantă deoarece celulele canceroase pot folosi vasele de sânge sau vasele limfatice pentru a se răspândi în alte părți ale corpului, cum ar fi ganglionii limfatici sau plămânii.

Ce sunt ganglionii limfatici și de ce sunt ei importanți?
Ganglionii limfatici sunt mici organe imunitare care se găsesc în tot corpul. Celulele canceroase se pot răspândi de la o tumoare la ganglionii limfatici prin vase mici numite limfatice. Din acest motiv, ganglionii limfatici sunt în mod obișnuit îndepărtați și examinați la microscop pentru a căuta celule canceroase. Mișcarea celulelor canceroase de la tumoră la o altă parte a corpului, cum ar fi un ganglion limfatic, se numește a metastază.
Celulele canceroase se răspândesc, de obicei, mai întâi la ganglionii limfatici din apropierea tumorii, deși pot fi implicați și ganglionii limfatici departe de tumoră. Din acest motiv, primii ganglioni limfatici îndepărtați sunt de obicei aproape de tumoră. Ganglionii limfatici mai departe de tumoră sunt în mod obișnuit îndepărtați numai dacă sunt măriți și există o suspiciune clinică ridicată că ar putea exista celule canceroase în ganglionul limfatic.
Dacă au fost îndepărtați ganglioni limfatici din corpul dumneavoastră, aceștia vor fi examinați la microscop de către un patolog, iar rezultatele acestei examinări vor fi descrise în raportul dumneavoastră. Cele mai multe rapoarte vor include numărul total de ganglioni limfatici examinați, unde în organism au fost găsiți ganglionii limfatici și numărul (dacă există) care conțin celule canceroase. Dacă celulele canceroase au fost observate într-un ganglion limfatic, va fi inclusă și dimensiunea celui mai mare grup de celule canceroase (descris adesea ca „focalizare” sau „depozit”).
Examinarea ganglionilor limfatici este importantă din două motive. În primul rând, această informație este utilizată pentru a determina stadiul nodal patologic (pN). În al doilea rând, găsirea celulelor canceroase într-un ganglion limfatic crește riscul ca celulele canceroase să fie găsite în alte părți ale corpului în viitor. Ca rezultat, medicul dumneavoastră va folosi aceste informații atunci când decide dacă este necesar un tratament suplimentar, cum ar fi chimioterapie, radioterapie sau imunoterapie.
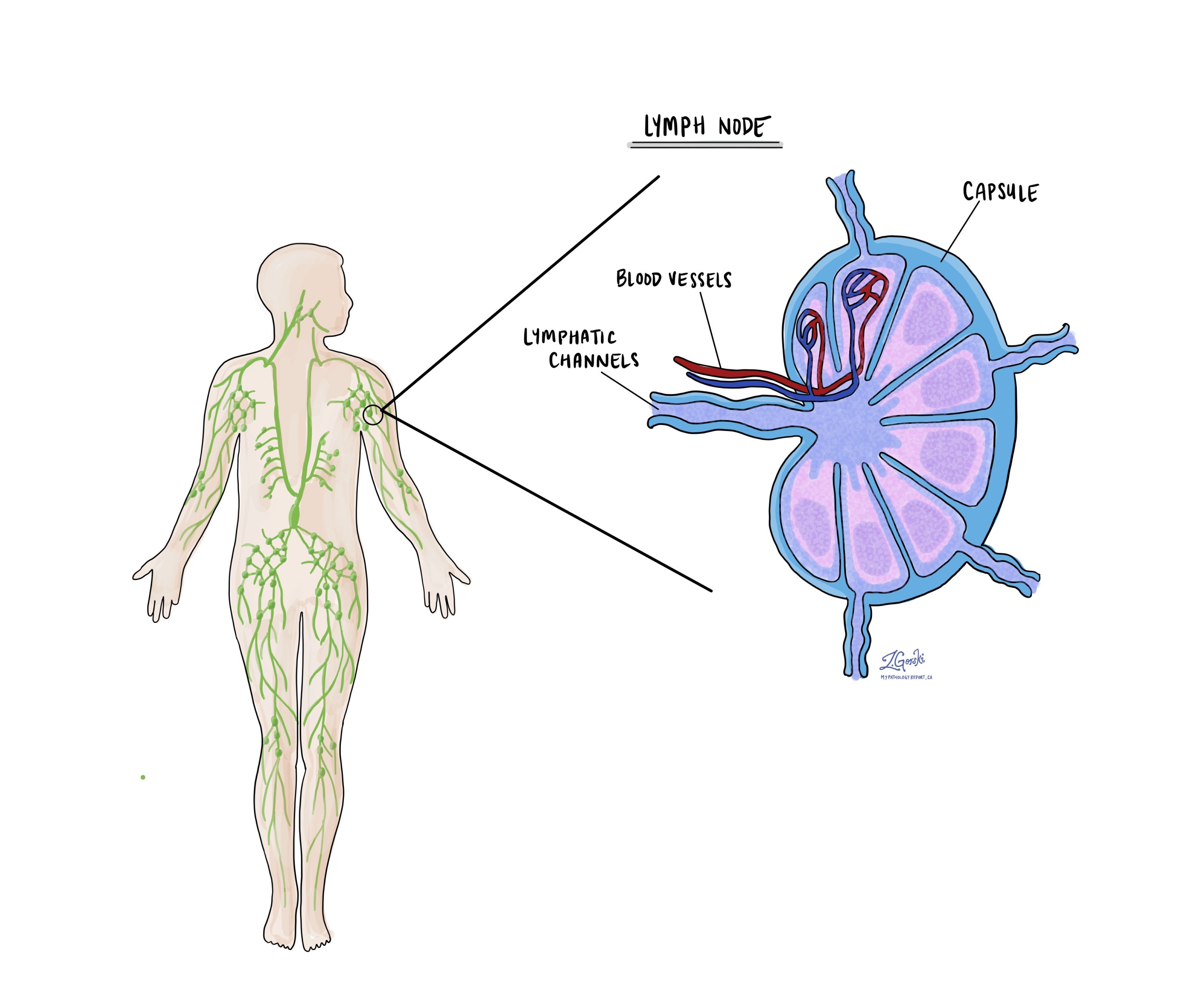
Ce înseamnă dacă un ganglion limfatic este descris ca pozitiv?
Patologii folosesc adesea termenul „pozitiv” pentru a descrie a ganglionilor limfatici care conține celule canceroase. De exemplu, un ganglion limfatic care conține celule canceroase poate fi numit „pozitiv pentru malignitate” sau „pozitiv pentru carcinom metastatic”.
Ce înseamnă dacă un ganglion limfatic este descris ca fiind negativ?
Patologii folosesc adesea termenul „negativ” pentru a descrie a ganglionilor limfatici care nu conține celule canceroase. De exemplu, un ganglion limfatic care nu conține celule canceroase poate fi numit „negativ pentru malignitate” sau „negativ pentru carcinom metastatic”.
Ce sunt celulele tumorale izolate (ITC)?
Patologii folosesc termenul „celule tumorale izolate” pentru a descrie un grup de celule tumorale care măsoară 0.2 mm sau mai puțin și se găsesc într-un ganglionilor limfatici. Ganglionii limfatici cu numai celule tumorale izolate (ITC) nu sunt considerați „pozitivi” în scopul stadiului ganglionar patologic (pN).
Ce este o micrometastaza?
O „micrometastază” este un grup de celule tumorale care măsoară de la 0.2 mm la 2 mm și se găsește într-un ganglionilor limfatici. Dacă în toți ganglionii examinați se găsesc doar micrometastaze, stadiul ganglionar patologic este pN1mi.
Ce este o macrometastază?
O „macrometastază” este un grup de celule tumorale care măsoară mai mult de 2 mm și se găsește în a ganglionilor limfatici. Macrometastazele sunt asociate cu o rautate prognoză și poate necesita tratament suplimentar.
Ce este un ganglion santinelă?
A ganglionul santinel este primul ganglion limfatic din lanțul de ganglioni limfatici care drenează lichidul din sân. Se găsește de obicei în axilă (subsuoară). Dacă cancerul este găsit în axilă, acesta va fi de obicei găsit mai întâi în ganglionul santinelă.
Ce este un ganglion limfatic axilar non-santinelă?
Un axilar non-santinelă ganglionilor limfatici este situat după ganglionul santinel în axilă (axilă). Celulele canceroase se răspândesc de obicei la acești ganglioni limfatici după ce trec prin ganglionul santinelă.
Ce înseamnă extensia extraganglionară?
Toți ganglionii limfatici sunt înconjurați de un strat subțire de țesut numit capsulă. Extensia extraganglionară înseamnă că celulele canceroase din ganglionul limfatic au spart prin capsulă și s-au răspândit în țesutul din afara ganglionului limfatic. Extensia extraganglionară este importantă deoarece crește riscul ca tumora să recrească în aceeași locație după intervenție chirurgicală. Pentru unele tipuri de cancer, extensia extraganglionară este, de asemenea, un motiv pentru a lua în considerare un tratament suplimentar, cum ar fi chimioterapia sau radioterapia.
Ce este o marjă și de ce sunt importante marjele?
În patologie, o margine este marginea unui țesut care este tăiată la îndepărtarea unei tumori din corp. Marginile descrise într-un raport de patologie sunt foarte importante pentru că vă spun dacă întreaga tumoră a fost îndepărtată sau dacă o parte din tumoră a fost lăsată în urmă. Starea marjei va determina ce tratament suplimentar (dacă există) aveți nevoie.
Cele mai multe rapoarte de patologie descriu doar marginile după o procedură chirurgicală numită extirpare or rezecţie a fost efectuat pentru îndepărtarea întregii tumori. Din acest motiv, marginile nu sunt de obicei descrise după o procedură numită a biopsie se efectuează pentru a elimina doar o parte a tumorii. Numărul de margini descrise într-un raport de patologie depinde de tipurile de țesuturi îndepărtate și de localizarea tumorii. Mărimea marginii (cantitatea de țesut normal dintre tumoare și marginea tăiată) depinde de tipul de tumoare care este îndepărtată și de localizarea tumorii.
Patologii examinează cu atenție marginile pentru a căuta celule tumorale la marginea tăiată a țesutului. Dacă celulele tumorale sunt văzute la marginea tăiată a țesutului, marginea va fi descrisă ca pozitivă. Dacă nu se observă celule tumorale la marginea tăiată a țesutului, o marjă va fi descrisă ca fiind negativă. Chiar dacă toate marginile sunt negative, unele rapoarte de patologie vor oferi, de asemenea, o măsurare a celulelor tumorale cele mai apropiate de marginea tăiată a țesutului.
O marjă pozitivă (sau foarte apropiată) este importantă, deoarece înseamnă că celulele tumorale pot fi lăsate în urmă în corpul dumneavoastră atunci când tumora a fost îndepărtată chirurgical. Din acest motiv, pacienților care au o marjă pozitivă li se poate oferi o altă intervenție chirurgicală pentru a îndepărta restul tumorii sau radioterapie în zona corpului cu marginea pozitivă. Decizia de a oferi tratament suplimentar și tipul de opțiuni de tratament oferite vor depinde de o varietate de factori, inclusiv de tipul de tumoră îndepărtată și de zona corpului implicată. De exemplu, un tratament suplimentar poate să nu fie necesar pentru a benign (non-canceroasă) tip de tumoare, dar poate fi recomandat pentru a maligne tip (canceros) de tumoră.
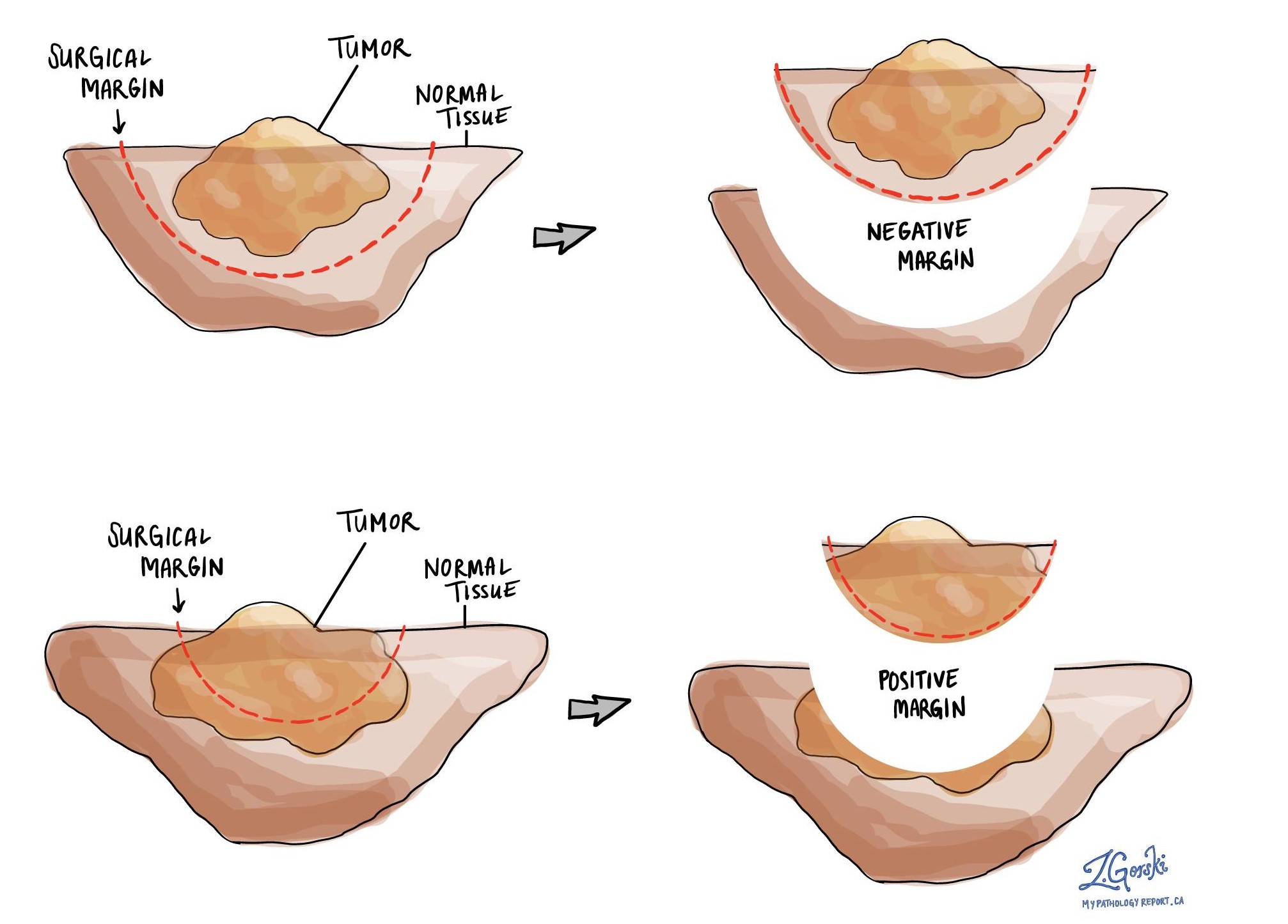
Ce înseamnă efectul tratamentului?
Dacă ați primit tratament (fie chimioterapie sau radioterapie) înainte ca tumora să fie îndepărtată, patologul dumneavoastră va examina tot țesutul trimis pentru a vedea cât de mult din tumoră este încă în viață (viabilă). Ganglionii limfatici cu celule canceroase vor fi de asemenea examinate pentru efectele tratamentului. Un efect de tratament mai mare (nu sau foarte puține celule tumorale viabile rămase) este asociat cu o mai bună supraviețuire fără boală și globală.
Despre acest articol
Acest articol a fost scris de medici pentru a vă ajuta să citiți și să înțelegeți raportul dumneavoastră de patologie. Contact dacă aveți întrebări despre acest articol sau raportul dumneavoastră de patologie. Citit acest articol pentru o introducere mai generală a părților unui raport tipic de patologie.


