par Jason Wasserman MD PhD FRCPC
Le 17 juin 2025
Le carcinome adénosquameux est un type de cancer du poumon qui contient deux types distincts de cellules cancéreuses : cellules glandulaires et cellules squameusesLes cellules glandulaires produisent normalement du mucus et d'autres substances qui contribuent à l'hydratation des voies respiratoires, tandis que les cellules squameuses tapissent généralement la surface interne des voies respiratoires. En raison de cette combinaison, le carcinome adénosquameux présente les caractéristiques de deux autres types de cancer du poumon : adénocarcinome (dérivé de cellules glandulaires) et carcinome épidermoïde (dérivée de cellules squameuses). Cette tumeur est connue pour son comportement agressif et son risque accru de propagation.
Quels sont les symptômes du carcinome adénosquameux du poumon ?
Les symptômes courants comprennent:
-
Une toux persistante qui s’aggrave avec le temps.
-
Tousser du sang.
-
Essoufflement.
-
Douleur thoracique.
Si la tumeur s'est propagée à d'autres parties du corps, des symptômes supplémentaires peuvent apparaître selon la localisation. Par exemple, si la tumeur se propage aux os, elle peut provoquer des douleurs osseuses ou les fragiliser, augmentant ainsi le risque de fracture (appelée fracture pathologique).
Quelles sont les causes du carcinome adénosquameux du poumon ?
Les causes exactes du carcinome adénosquameux du poumon ne sont pas entièrement comprises, mais plusieurs facteurs de risque connus augmentent la probabilité de développer ce cancer :
-
Fumer du tabac : Il s’agit de la cause la plus fréquente de tous les types de cancer du poumon.
-
Exposition au radon : Un gaz radioactif présent dans certaines maisons.
-
Exposition à l'amiante : Souvent lié à des professions telles que la construction, l’exploitation minière ou la construction navale.
-
Autres substances nocives : Produits chimiques et polluants industriels.
-
Facteurs génétiques: Les antécédents familiaux et les maladies héréditaires peuvent également augmenter le risque.
Comment ce diagnostic est-il établi ?
Le diagnostic du carcinome adénosquameux commence généralement par des examens d'imagerie, comme une radiographie thoracique ou un scanner, suivis du prélèvement d'un petit échantillon de tissu pulmonaire par biopsie ou ponction à l'aiguille fine (PAF). Cet échantillon est examiné au microscope par un pathologiste (médecin spécialisé dans le diagnostic des maladies par l'analyse d'échantillons de tissus).
Si la biopsie confirme qu'il s'agit d'un carcinome adénosquameux, une intervention chirurgicale peut être pratiquée pour retirer la totalité de la tumeur. Le type d'intervention dépend de la taille et de la localisation de la tumeur dans le poumon :
-
Résection en coin: Ablation de petites tumeurs situées près du bord externe du poumon.
-
Lobectomie : Ablation d'un lobe du poumon pour les tumeurs plus grosses.
-
Pneumonectomie : Ablation d'un poumon entier pour les tumeurs proches du centre ou les tumeurs de grande taille.
À quoi ressemble le carcinome adénosquameux au microscope ?
Au microscope, le carcinome adénosquameux contient un mélange de deux types de cellules cancéreuses différents :
-
Cellules glandulaires : Souvent disposées en structures glandulaires (semblables à des glandes) ou en groupes solides, ces cellules tapissent parfois les alvéoles (sacs aériens) selon un motif dit lépidique.
-
Cellules squameuses : Ils forment généralement de grands groupes et peuvent être décrits comme :
-
Kératinisation : Lorsque les cellules produisent une grande quantité de kératine (une protéine qui donne aux cellules une apparence rose au microscope).
-
Non kératinisant : Lorsque les cellules ne produisent pas beaucoup de kératine (ce qui les fait apparaître plus bleues au microscope).
-
Quels tests supplémentaires peuvent être effectués pour confirmer le diagnostic ?
Votre pathologiste peut utiliser des tests spéciaux appelés immunohistochimie (IHC) Pour confirmer le diagnostic et distinguer le carcinome adénosquameux des autres types de cancer du poumon. L'immunohistochimie permet d'identifier des protéines spécifiques produites par les cellules cancéreuses. Pour le carcinome adénosquameux, les résultats typiques sont :
-
TTF-1 : Positif dans les cellules glandulaires.
-
p40 et CK5 : Positif dans les cellules squameuses.
-
Chromogranine et synaptophysine : Généralement négatif dans les cellules glandulaires et squameuses.
Diffusion dans les espaces aériens (STAS)
La propagation par les espaces aériens (STAS) décrit un mode de croissance du cancer du poumon où les cellules cancéreuses se propagent dans les espaces aériens adjacents du poumon. La présence de STAS entraîne souvent un risque accru de récidive du cancer et indique généralement un pronostic plus sombre, en particulier pour les tumeurs à un stade précoce.
Les pathologistes examinent le tissu pulmonaire entourant la tumeur au microscope pour déterminer si les cellules cancéreuses flottent librement ou sont attachées séparément aux parois alvéolaires, loin de la masse tumorale principale.
Tumeurs multiples dans le poumon
Il est possible d'avoir plusieurs tumeurs dans le poumon. Si plusieurs tumeurs sont détectées, votre rapport anatomopathologique décrira chaque tumeur séparément.
Il existe deux raisons pour lesquelles plusieurs tumeurs peuvent apparaître :
-
Propagation à partir d'une tumeur : Probablement si toutes les tumeurs sont du même type (par exemple, si elles sont toutes des carcinomes adénosquameux). Les tumeurs plus petites sont appelées nodules si elles sont localisées du même côté du poumon, et métastases si elles sont localisées du côté opposé.
-
Tumeurs séparées : Si les tumeurs sont de types différents (par exemple, un carcinome adénosquameux et un carcinome épidermoïde), elles sont susceptibles de s'être développées séparément. Ces tumeurs sont considérées comme des cancers primitifs distincts.
Invasion pleurale
La plèvre est une fine membrane qui entoure les poumons et la paroi thoracique. Lorsque des cellules cancéreuses se propagent à la plèvre, on parle d'invasion pleurale. L'invasion pleurale est importante car elle signifie généralement :
-
Stade tumoral supérieur : Le cancer qui envahit la plèvre est considéré comme plus avancé.
-
Pronostic plus sombre : L’invasion pleurale entraîne souvent des complications, telles qu’une accumulation de liquide (épanchement pleural), qui peut provoquer un essoufflement, des douleurs thoraciques et de la toux.
Invasion lymphovasculaire
L'invasion lymphovasculaire signifie que les cellules cancéreuses ont pénétré dans les petits vaisseaux (vaisseaux sanguins ou canaux lymphatiques) du tissu pulmonaire. Ceci est important, car les cellules cancéreuses présentes dans ces vaisseaux peuvent migrer vers les ganglions lymphatiques ou d'autres parties du corps, entraînant ainsi d'autres métastases (propagation).

Les marges
En pathologie, une marge désigne le bord de tissu retiré lors d'une intervention chirurgicale visant à retirer une tumeur. Après une chirurgie pulmonaire, les pathologistes examinent soigneusement tous ces bords de tissu au microscope afin de déterminer si la tumeur a été complètement retirée.
Les marges évaluées lors des chirurgies du cancer du poumon comprennent généralement :
-
marge bronchique – C’est ici que le chirurgien coupe les voies respiratoires.
-
marge vasculaire – Il s’agit des zones où les gros vaisseaux sanguins proches de la tumeur sont sectionnés.
-
marge parenchymateuse – Cette marge comprend le bord du tissu pulmonaire autour de la tumeur.
-
marge pleurale – La plèvre est une fine membrane qui entoure le poumon, et cette marge est examinée pour déterminer si la tumeur se développe à proximité ou à travers cette membrane.
Les marges peuvent être décrites de deux manières :
-
Marge négative – Aucune cellule cancéreuse n'est visible sur les bords de l'incision. Cela indique que la tumeur a probablement été entièrement retirée, ce qui est l'objectif de l'intervention.
-
Marge positive – Des cellules cancéreuses sont visibles au bord de l'incision. Une marge positive signifie qu'il pourrait rester des cellules tumorales dans votre corps. Les patients présentant une marge positive peuvent nécessiter des traitements supplémentaires, comme une seconde intervention chirurgicale ou une radiothérapie, pour éliminer les cellules tumorales restantes et réduire le risque de récidive.
L’état des marges aide votre médecin à déterminer la nécessité d’un traitement supplémentaire et joue un rôle important dans la prédiction de la probabilité de réapparition de la tumeur.

Ganglions
Ganglions Ce sont de petits organes en forme de haricot qui jouent un rôle essentiel dans le système immunitaire. Ils sont reliés à tout le corps par de petits canaux appelés vaisseaux lymphatiques. Les cellules cancéreuses peuvent se propager d'une tumeur à travers ces vaisseaux lymphatiques jusqu'aux ganglions lymphatiques voisins, un processus appelé métastase ganglionnaire.
Les ganglions lymphatiques des poumons et du thorax sont regroupés en zones spécifiques, appelées « stations ganglionnaires ». Il existe 14 stations ganglionnaires différentes, chacune ayant une localisation spécifique :
-
Station 1: Ganglions lymphatiques cervicaux inférieurs, sus-claviculaires et de l'encoche sternale.
-
Station 2: Ganglions lymphatiques paratrachéaux supérieurs.
-
Station 3: Ganglions lymphatiques prévasculaires et rétrotrachéaux.
-
Station 4: Ganglions lymphatiques paratrachéaux inférieurs.
-
Station 5: Ganglions lymphatiques sous-aortiques (fenêtre aortopulmonaire).
-
Station 6: Ganglions lymphatiques para-aortiques (à proximité de l'aorte ascendante ou du nerf phrénique).
-
Station 7: Ganglions lymphatiques sous-carinaux (sous la carène, là où la trachée se divise en bronches).
-
Station 8: Ganglions lymphatiques para-œsophagiens (le long de l'œsophage sous la carène).
-
Station 9: Ganglions lymphatiques du ligament pulmonaire.
-
Station 10: Ganglions lymphatiques hilaires (au niveau du hile pulmonaire, où les voies respiratoires pénètrent dans le poumon).
-
Station 11: Ganglions lymphatiques interlobaires (entre les lobes pulmonaires).
-
Station 12: Ganglions lymphatiques lobaires (dans les lobes pulmonaires).
-
Station 13: Ganglions lymphatiques segmentaires (à l'intérieur des segments pulmonaires).
-
Station 14: Ganglions lymphatiques sous-segmentaires (dans des sous-segments pulmonaires plus petits).

Si des ganglions lymphatiques sont retirés lors d'une intervention chirurgicale, un pathologiste les examine attentivement au microscope pour vérifier s'ils contiennent des cellules cancéreuses. Le rapport d'anatomopathologie comprend généralement :
-
Le nombre total de ganglions lymphatiques examinés.
-
Les emplacements (stations) des ganglions lymphatiques examinés.
-
Le nombre de ganglions lymphatiques contenant des cellules cancéreuses.
-
La taille du plus grand groupe de cellules cancéreuses (souvent appelé « foyer » ou « dépôt »).
L'examen des ganglions lymphatiques fournit des informations importantes qui aident votre médecin à déterminer le stade ganglionnaire pathologique (pN) du cancer. Il permet également de prédire la probabilité de propagation des cellules cancéreuses à d'autres parties du corps, guidant ainsi les décisions concernant les traitements complémentaires tels que la chimiothérapie, la radiothérapie ou l'immunothérapie.
Biomarqueurs du carcinome adénosquameux du poumon
Les biomarqueurs sont des molécules spécifiques présentes dans les cellules tumorales. Ces molécules aident les médecins à comprendre le comportement de la tumeur et sa réponse potentielle aux différents traitements. La recherche de biomarqueurs est importante dans le cancer du poumon, car certaines tumeurs présentent des modifications génétiques qui les rendent bien réceptives aux thérapies ciblées. Ces thérapies sont des médicaments conçus spécifiquement pour attaquer les cellules cancéreuses présentant ces modifications génétiques. L'identification de ces biomarqueurs aide les médecins à choisir les options thérapeutiques les plus efficaces.
Les pathologistes recherchent des biomarqueurs à l’aide de tests de laboratoire spécialisés.
Deux tests courants incluent :
-
Séquençage de nouvelle génération (NGS) Ce test examine plusieurs gènes simultanément afin de détecter des mutations (modifications du matériel génétique des cellules tumorales). Le NGS permet d'identifier rapidement plusieurs biomarqueurs à partir d'un seul échantillon de tissu.
-
Immunohistochimie (IHC) – Ce test utilise des colorants spéciaux qui se fixent à des protéines spécifiques produites par les cellules cancéreuses. Lorsque ces protéines sont présentes, les cellules tumorales changent de couleur au microscope. L'IHC permet de confirmer la présence de certains biomarqueurs dans la tumeur.
Biomarqueurs courants testés dans le carcinome adénosquameux du poumon
Votre rapport de pathologie peut inclure des informations sur les biomarqueurs suivants. Chaque biomarqueur peut orienter votre traitement et fournir des informations importantes sur votre tumeur.
-
EGFR : Les mutations (changements) du gène EGFR sont fréquentes dans le cancer du poumon, en particulier chez les personnes n'ayant jamais fumé, les femmes et les personnes d'origine est-asiatique. Les tumeurs présentant des mutations du gène EGFR répondent souvent très bien aux thérapies ciblées appelées inhibiteurs de l'EGFR. Votre rapport décrira la tumeur comme EGFR-positive si une mutation est détectée. En l'absence de mutation, elle sera dite EGFR-négative.
-
ALK: Les modifications du gène ALK, appelées réarrangements ou fusions ALK, entraînent une croissance tumorale et sont souvent observées chez les patients jeunes ou non-fumeurs. Les tumeurs présentant des réarrangements du gène ALK répondent généralement bien aux médicaments appelés inhibiteurs d'ALK. Votre rapport indiquera que votre tumeur est ALK-positive si cette modification est présente. En son absence, votre tumeur sera ALK-négative.
-
ROS1 : Les réarrangements (fusions) de ROS1 entraînent une croissance rapide des cellules cancéreuses. Les tumeurs ROS1-positives répondent généralement bien aux traitements ciblés par inhibiteurs de ROS1. Si votre tumeur présente un réarrangement de ROS1, elle sera dite ROS1-positive. En l'absence de réarrangement, elle sera dite ROS1-négative.
-
BRAF: Certaines mutations du gène BRAF peuvent entraîner une croissance rapide des cellules tumorales. Les tumeurs présentant des mutations spécifiques du gène BRAF, notamment la mutation V600E, peuvent être traitées par des inhibiteurs de BRAF. Si une mutation du gène BRAF est détectée, votre tumeur sera dite BRAF-positive. En l'absence de mutation, elle sera dite BRAF-négative.
-
MET: Les mutations du gène MET, en particulier celles entraînant un « saut de l'exon 14 » du gène MET, entraînent une croissance tumorale accrue. Les tumeurs MET-positives répondent souvent aux thérapies ciblées appelées inhibiteurs de MET. Votre rapport anatomopathologique décrira votre tumeur comme MET-positive si cette mutation est présente. En l'absence de mutation, votre tumeur sera MET-négative.
-
RET : Les réarrangements ou fusions du gène RET entraînent une croissance tumorale incontrôlée. Les tumeurs présentant des fusions du gène RET répondent généralement très bien aux inhibiteurs de RET. Votre compte rendu indiquera que votre tumeur est RET-positive si une fusion est détectée. En l'absence de fusion, elle sera qualifiée de RET-négative.
-
NTRK1-3 : Les fusions du gène NTRK sont rares, mais peuvent fortement favoriser la croissance tumorale. Les tumeurs présentant des fusions du gène NTRK répondent généralement à des médicaments ciblés appelés inhibiteurs de TRK. Si une fusion du gène NTRK est détectée, votre tumeur sera décrite comme NTRK-positive. Dans le cas contraire, elle sera décrite comme NTRK-négative.
-
KRAS: Les mutations KRAS sont fréquentes dans les cancers du poumon, en particulier chez les fumeurs. Historiquement, les tumeurs KRAS-positives étaient difficiles à traiter, mais des médicaments récents ciblant une mutation KRAS spécifique (KRAS G12C) ont montré des résultats prometteurs. Si une mutation KRAS est présente, votre tumeur sera dite KRAS-positive. En l'absence de mutation, votre tumeur sera dite KRAS-négative.
-
ERBB2 (HER2) : Les mutations du gène ERBB2 (également appelées mutations HER2) peuvent favoriser la croissance tumorale, en particulier chez les non-fumeurs. Les tumeurs porteuses de mutations HER2 peuvent répondre aux thérapies ciblées actuellement à l'étude ou disponibles dans des centres spécialisés. Si votre tumeur présente une mutation du gène ERBB2, elle sera dite ERBB2-positive. En l'absence de mutation, elle sera dite ERBB2-négative.
-
NRAS : Les mutations du gène NRAS surviennent le plus souvent dans les tumeurs des personnes ayant fumé. Actuellement, les thérapies ciblées spécifiques aux mutations du gène NRAS sont limitées ; cependant, l'identification de cette mutation peut contribuer à comprendre le comportement tumoral. Votre tumeur sera dite NRAS-positive si une mutation est détectée, ou NRAS-négative si aucune mutation n'est présente.
-
MAP2K1 (MEK1) : Les mutations du gène MAP2K1 sont plus fréquentes chez les fumeurs et sont associées à une croissance tumorale accrue. Des traitements ciblant spécifiquement les mutations du gène MAP2K1 sont actuellement à l'étude. Votre compte rendu anatomopathologique indiquera si une mutation du gène MAP2K1 est présente (MAP2K1 positif) ou non (MAP2K1 négatif).
-
NRG1 : Les réarrangements du gène NRG1 sont rares, mais importants, car ils peuvent favoriser une croissance tumorale rapide. Les chercheurs étudient activement des traitements ciblés pour les tumeurs présentant des réarrangements du gène NRG1. Votre tumeur sera dite NRG1-positive si ce réarrangement est détecté. Dans le cas contraire, elle sera dite NRG1-négative.
Pourquoi les tests de biomarqueurs sont-ils importants pour le traitement ?
L'identification de ces biomarqueurs dans votre tumeur est essentielle, car ils aident les médecins à choisir les traitements les plus efficaces. Certains biomarqueurs correspondent à des médicaments spécifiques qui ciblent directement les cellules tumorales. Ces traitements sont souvent plus efficaces et présentent moins d'effets secondaires que la chimiothérapie traditionnelle.
Si votre tumeur ne présente pas de biomarqueurs correspondant aux traitements ciblés disponibles, votre médecin pourrait vous recommander d'autres options, comme la chimiothérapie ou l'immunothérapie. Votre équipe médicale vous aidera à comprendre les résultats de vos analyses et les meilleures options thérapeutiques disponibles pour vous.
Stadification pathologique (pTNM)
La stadification pathologique décrit l'étendue de la propagation du cancer selon le système TNM. Ce système fournit des informations importantes pour le pronostic et les décisions thérapeutiques.
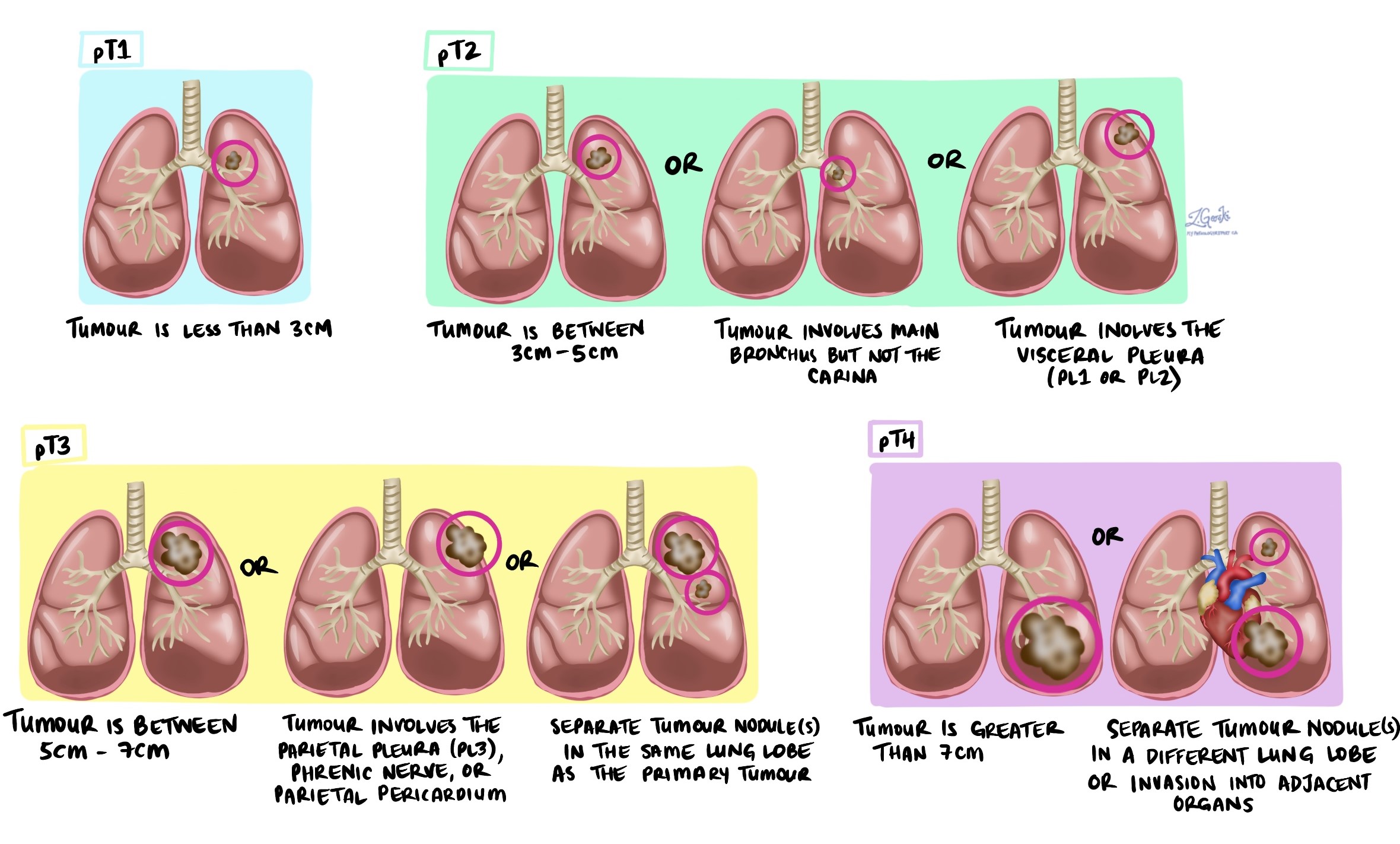
Stade tumoral (pT)
Le stade pathologique de la tumeur décrit la taille et l'étendue de la tumeur pulmonaire primitive. Il varie de 1 à 4 et permet de déterminer le pronostic et la meilleure approche thérapeutique.
-
T1: La tumeur ne dépasse pas 3 centimètres et est limitée au poumon, sans impliquer les structures voisines.
-
T2: La tumeur mesure plus de 3 centimètres mais pas plus de 5 centimètres, ou elle envahit la plèvre viscérale (enveloppe du poumon), ou elle bloque partiellement une voie aérienne (bronche), mais n'est pas proche du hile pulmonaire.
-
T3: La tumeur mesure plus de 5 centimètres mais pas plus de 7 centimètres, ou elle a directement envahi les structures voisines telles que la paroi thoracique, le péricarde (enveloppe du cœur), le diaphragme, ou présente des nodules tumoraux séparés dans le même lobe pulmonaire.
-
T4: La tumeur mesure plus de 7 centimètres, ou elle a envahi des structures vitales telles que le cœur, les principaux vaisseaux sanguins, la trachée, l’œsophage, la colonne vertébrale, ou présente des nodules tumoraux distincts dans un lobe différent du même poumon.
Stade nodal (pN)
Le stade ganglionnaire pathologique est basé sur le nombre de ganglions lymphatiques contenant des cellules cancéreuses et sur l’emplacement des ganglions lymphatiques impliqués.
-
NX : Aucun ganglion lymphatique n'a été soumis.
-
N0: Aucune cellule cancéreuse dans les ganglions lymphatiques.
-
N1: Cellules cancéreuses dans les ganglions lymphatiques proches de la tumeur (stations 10–14).
-
N2: Cellules cancéreuses dans les ganglions lymphatiques au milieu de la poitrine (stations 7 à 9).
-
N3: Cellules cancéreuses dans les ganglions lymphatiques éloignés de la tumeur ou du côté opposé de la poitrine (stations 1 à 6).
Effet du traitement
Si vous avez reçu une chimiothérapie ou une radiothérapie avant l'intervention, l'effet du traitement décrit la réponse de la tumeur. Les pathologistes mesurent la quantité de tissu tumoral viable (vivant) restant après le traitement, exprimée en pourcentage. Un pourcentage plus faible de tumeur viable indique une meilleure réponse au traitement.
Pronostic du carcinome adénosquameux du poumon
Le carcinome adénosquameux a souvent un pronostic plus sombre que les autres cancers du poumon en raison de son caractère agressif et de sa tendance à se propager précocement. Cependant, le pronostic dépend fortement du stade du diagnostic. Les tumeurs à un stade précoce ont généralement de meilleures perspectives que les tumeurs à un stade avancé.
Questions à poser à votre médecin
Si vous avez reçu un diagnostic de carcinome adénosquameux, pensez à demander :
-
Quel est le stade de ma tumeur et qu’est-ce que cela signifie ?
-
Les marges chirurgicales étaient-elles claires (négatives) ?
-
Les ganglions lymphatiques étaient-ils impliqués ?
-
Aurai-je besoin d’un traitement supplémentaire comme une chimiothérapie ou une radiothérapie ?
-
Dois-je subir des tests génétiques pour orienter le traitement ?
-
À quelle fréquence dois-je faire l’objet d’un suivi ?
-
Existe-t-il des essais cliniques disponibles pour ma maladie ?