ジェイソン・ワッサーマン医学博士(FRCPC)とマット・チェッキーニ医学博士(FRCPC)
2025 年 11 月 27 日
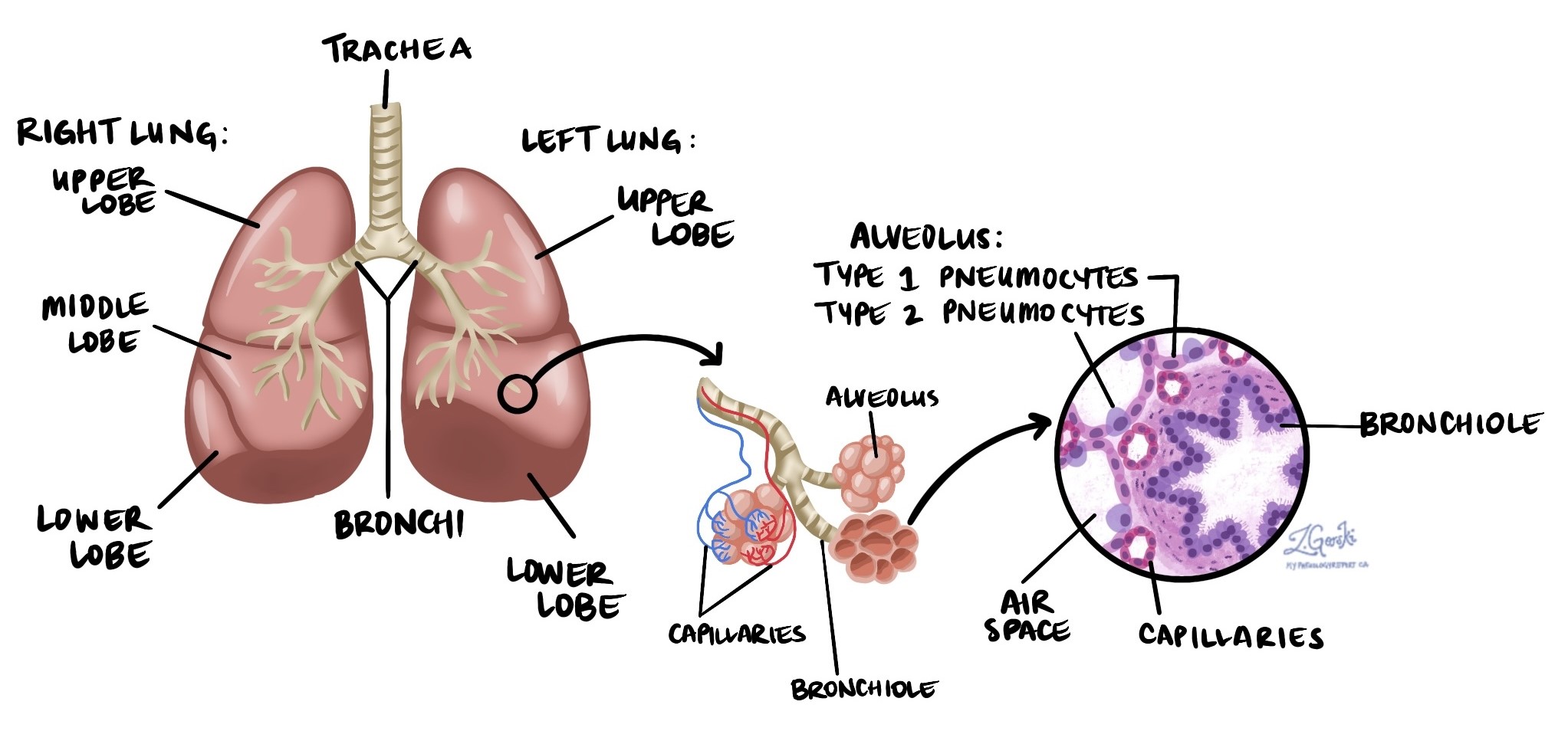
腺癌 最も一般的な肺がんの一種で、北米における肺がん症例の約40%を占めています。これは、 非小細胞肺がん (NSCLC)腺癌は、肺胞と呼ばれる肺の小さな空気の袋の内側を覆う特殊な細胞である肺胞上皮細胞から発生します。肺胞は、酸素が血流に入り、二酸化炭素が排出される場所です。
腺がんは肺の外縁付近から発生することが多いため、X 線や CT スキャンなどの画像検査で小さな結節や腫瘤が見つかると早期に発見されることがあります。
肺腺がんの原因は何ですか?
肺腺癌の主な原因は喫煙です。喫煙には紙巻きタバコ、葉巻、パイプが含まれます。しかし、喫煙経験のない人にも腺癌が発生することがあります。
その他の原因と危険因子としては次のようなものがあります:
-
ラドン被曝。
-
アスベスト、シリカ、ディーゼル排気ガスなどの職業上の暴露。
-
屋外の大気汚染。
これらの要因は肺細胞にダメージを与え、時間の経過とともに癌のリスクを高める可能性があります。
肺の腺癌の症状は何ですか?
肺腺がんの症状は様々です。特に初期段階では、症状が現れない人もいます。症状が現れた場合は、以下のような症状が現れることがあります。
-
咳が持続したり悪化したりすること。
-
喀血。
-
胸痛。
-
息切れ。
-
疲労または意図しない体重減少。
がんが体の他の部位に転移した場合、症状は転移した部位によって異なります。例えば、骨転移の場合は痛みが生じたり、病的骨折(がんによって骨組織が弱くなることで起こる骨折)を引き起こすこともあります。
肺の腺癌に関連する状態は何ですか?
肺腺癌は、次のような前癌状態から発生することがあります。
-
非典型腺腫性過形成(AAH)は、肺胞の内層細胞が異常に見えても癌ではない状態です。
-
上皮内腺癌(AIS) 肺胞の内面に限定され、3cm未満の非浸潤癌です。
AIS は、腫瘍が 3 cm を超えて成長した場合、または癌細胞が肺胞内壁の下の支持組織に侵入した場合に、浸潤性腺癌に進行する可能性があります。
この診断はどのように行われますか?
腺癌の診断は、画像検査で肺に疑わしい領域が見つかったときに始まります。診断を確定するために、 生検 小さな組織サンプルを採取するために行われます。生検は、針生検、気管支鏡検査、気管支内超音波検査(EBUS)、または穿刺吸引細胞診(FNA)によって行われます。採取された組織サンプルは、組織を研究して病気を診断することを専門とする医師である病理医によって顕微鏡で検査されます。
がんと診断された場合、腫瘍を切除するための手術が推奨されることがあります。手術の種類は腫瘍の大きさと位置によって異なります。外表面に近い小さな腫瘍は楔状切除で切除できますが、大きな腫瘍や中心部にある腫瘍は肺葉切除、さらには肺全摘出が必要になる場合があります。
摘出後、病理医は腫瘍全体を検査します。重要な特徴として、以下の点が挙げられます。
-
成長のパターン(組織学的タイプ)。
-
がんが周囲の肺組織に広がっているかどうか。
-
気腔を通して拡散するかどうか(STAS)が存在します。
-
腫瘍細胞が血管やリンパ管に侵入しているかどうか。
-
腫瘍が胸膜にまで成長しているかどうか。
-
手術マージンが明確であるかどうか。
-
リンパ節に癌細胞が含まれているかどうか。
免疫組織化学(IHC)
免疫組織化学 細胞内の特定のタンパク質を検出するために、色素に結合した抗体を用いる特殊な検査です。これらのタンパク質は「マーカー」として機能し、病理医ががんの種類を特定し、発生部位を特定するのに役立ちます。
肺腺癌では、典型的には次のような結果が見られます。
-
TTF-1: 陽性。
-
p40: 陰性。
-
CK5: 陰性。
-
クロモグラニン:陰性。
-
シナプトフィジン:陰性。
この染色パターンは診断を裏付け、扁平上皮癌や神経内分泌腫瘍などの他の種類の肺癌を除外するのに役立ちます。
腺癌の組織学的型
肺腺癌は、癌細胞の増殖様式に基づいて組織学的にいくつかの型に分類されます。腫瘍は、1つまたは複数の型を示すことがあります。
鱗状型
癌細胞は肺胞の内面に沿って増殖します。腫瘍が完全に鱗状で、大きさが3cm未満の場合、AISに分類されます。
腺房型
腫瘍細胞は丸い腺のような構造を形成します。
ソリッドタイプ
腫瘍細胞は隙間のほとんどない密集したシート状に増殖します。このタイプはより悪性度が高いです。
乳頭型
腫瘍細胞は乳頭と呼ばれる指のような突起を形成します。
微小乳頭型
腫瘍細胞は房状の小さな塊を形成します。これは非常に悪性度の高いパターンです。
腫瘍のグレード
肺腺癌の場合、腫瘍のグレードは、顕微鏡下での癌の進行度を表します。グレードは、以下の2つの顕微鏡的特徴に基づいています。
-
主な組織学的パターン。
-
腫瘍のどこにも見られない最悪の(最も攻撃的な)パターン。
鱗状増殖が主体で、充実性または微小乳頭状の特徴が最小限に抑えられた腫瘍は高分化型であり、増殖速度が遅く、予後も良好です。腺房性または乳頭状増殖を呈し、少量の悪性度パターンを示す腫瘍は中分化型です。充実性または微小乳頭状増殖を多量に含む腫瘍は低分化型であり、悪性度が高く、増殖速度が速く、転移しやすいことを意味します。
腫瘍のグレードは、特に早期段階の病気においては、予後を予測する最も重要な指標の 1 つです。
空域を介した拡散 (STAS)
STASとは、がん細胞が主腫瘍の縁を越えて肺の気腔内に浮遊している状態を指します。これらの細胞は原発巣から分離しており、肺の細い気道を通って移動することができます。
STASの存在は、特に楔状切除などの小手術後に再発リスクが上昇することと関連しています。そのため、STASは病理報告書に記載され、治療方針の決定に役立ちます。
多発性腫瘍
肺に複数の腫瘍が見つかることもあります。このような場合、それぞれの腫瘍を個別に検査します。複数の腫瘍が、特に顕微鏡下で同一に見える場合、単一の原発腫瘍からの転移である場合もあります。原発腫瘍と同じ肺に小さな二次腫瘍が現れた場合、それらはしばしば結節と呼ばれます。これは小さく丸い病変で、肺内での転移を示している可能性があります。
場合によっては、腫瘍が独立して形成された可能性があり、特に組織学的パターンや特徴が異なる場合はその可能性が高くなります。例えば、一方の腫瘍は腺癌で、もう一方の腫瘍は扁平上皮癌である可能性があります。腫瘍が別々に発生した場合、それらは転移性疾患ではなく、別々の原発性癌とみなされます。この2つの可能性を区別することは、病期分類、治療、予後に影響を与えるため重要です。
胸膜浸潤
胸膜は2層からなる薄い膜です。
-
臓側胸膜は肺の表面を覆っています。
-
胸腔の内側を覆う壁側胸膜。
胸膜浸潤とは、がん細胞がこれらの層のいずれか、または両方に増殖していることを意味します。臓側胸膜のみに浸潤している腫瘍は、肺組織自体に限局している腫瘍よりも局所的に進行しているとみなされます。胸壁に接する外層である壁側胸膜に浸潤している腫瘍は、がんが肺を越えて胸腔内壁に達しているため、さらに進行しているとみなされます。胸膜浸潤はTステージを上昇させ、転移および再発のリスクを高めます。
リンパ管浸潤
リンパ血管浸潤(LVI)は、がん細胞が腫瘍内または腫瘍近傍の血管またはリンパ管に侵入することで発生します。これらの血管は、がんがリンパ節、骨、肝臓、脳など、体の他の部位に転移する経路として機能します。リンパ血管浸潤がある場合、転移のリスクが高く、追加の治療が推奨される場合があります。
マージン
切除断端とは、手術中に切除された組織の端のことです。病理医はすべての切除断端を検査し、腫瘍が完全に切除されたかどうかを判断します。切除断端陰性は、切除断端に癌細胞が認められないことを意味します。切除断端陽性は、切除断端に癌細胞が存在し、癌が残存している可能性が懸念されることを意味します。切除断端の状態は、医師が更なる手術や放射線治療が必要かどうかを判断する際に役立ちます。

リンパ節
リンパ節 リンパ液は小さな免疫器官であり、リンパ液を濾過します。肺腺癌は、肺や胸部中央のリンパ節に転移することがよくあります。手術では、特定の解剖学的領域(リンパ節ステーションと呼ばれる)からリンパ節を摘出し、検査することがあります。
病理報告書には、検査されたリンパ節の数、位置、そして癌の有無が記載されます。これらの情報はリンパ節転移の進行度を判定するのに役立ち、治療法の選択において重要な役割を果たします。

病理学的病期(pTNM)
肺腺癌はTNMシステムを使用してステージ分けされます。
-
T ステージは腫瘍の大きさと、近くの組織への浸潤の有無を表します。
-
N ステージは、リンパ節に癌が含まれているかどうかを示します。
-
M ステージは、がんが脳、骨、肝臓などの遠隔臓器に転移しているかどうかを示します。
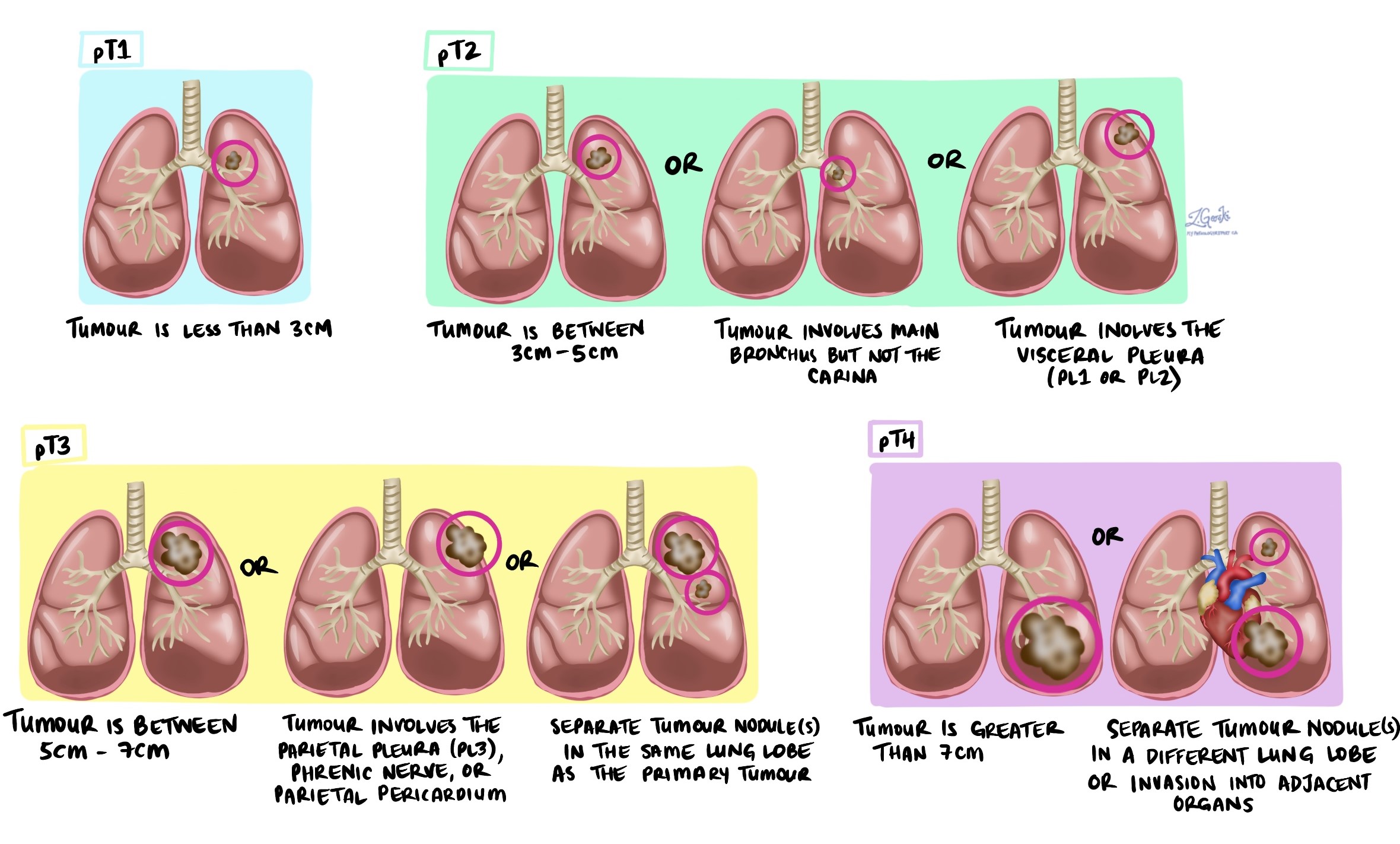
腫瘍の病期(pT)
-
T1: 腫瘍の大きさは3cm以下。
-
T2: 腫瘍は3cmより大きいが5cm以下、または臓側胸膜または中心気道に浸潤している。
-
T3: 腫瘍は 5 cm より大きいが 7 cm 以下、または近くの組織にまで広がっています。
-
T4: 腫瘍が 7 cm より大きいか、心臓や食道などの近くの臓器に浸潤しています。
ノーダルステージ(pN)
-
NX: リンパ節は検査されませんでした。
-
N0: リンパ節に癌細胞はありません。
-
N1: 肺内または気道付近のリンパ節に癌細胞が存在する(ステーション10~14)。
-
N2: 気道近くの胸部中央のリンパ節に癌細胞がある(ステーション7~9)。
-
N3: 胸部の反対側または首の下部のリンパ節に癌細胞が存在する(ステーション 1 ~ 6)。
ステージが進むにつれて転移や再発のリスクが高くなり、より集中的な治療が必要になることがよくあります。
肺腺癌のバイオマーカー
バイオマーカーとは、がん細胞における測定可能な変化であり、多くの場合、特定の遺伝子やタンパク質が関与しています。これらの変化は、医師が腫瘍の挙動を理解し、最適な治療法を決定するのに役立ちます。肺腺がんにおいては、多くの腫瘍が遺伝子変異を有しており、がんの増殖を助ける異常なシグナルを遮断する治療法で標的とすることができるため、バイオマーカーは特に重要です。バイオマーカー検査は現在、診断の標準的な方法となっており、多くの治療方針の決定を導きます。
肺腺癌ではどのような種類のバイオマーカーが検査されますか?
肺腺がんのバイオマーカー検査のほとんどは、腫瘍DNAに見られる遺伝子変異と遺伝子再編成に焦点を当てています。これらの変化は、PCR(DNAの小さな断片を増幅する検査)、次世代シーケンシング(NGS:一度に多くの遺伝子を調べる検査)、FISH(蛍光プローブを用いて遺伝子再編成を検出する検査)といった特殊な検査技術を用いて検出されます。これらの検査は生検組織、つまり手術で切除された腫瘍に対して行われ、どの治療法が最も効果的かを判断する上で重要な役割を果たします。
EGFR
EGFRは、細胞の増殖を制御する受容体をコードする遺伝子です。EGFRに特定の変異が生じると、受容体が過剰に活性化し、腫瘍の増殖を促進します。EGFR変異は、喫煙経験のない人、女性、そして東アジア系の人々に多く見られます。これらの変異は重要です。なぜなら、EGFR遺伝子変異を有する腫瘍は、異常な増殖シグナルを阻害し、腫瘍を縮小させたり、進行を遅らせたりするEGFR標的療法に非常によく反応することが多いからです。
病理学者は、PCR または次世代シーケンシングを使用して腫瘍の DNA を調べ、特定の遺伝子変化を検出することで、EGFR 変異を検査します。
病理レポートでは、変異が検出された場合は腫瘍が EGFR 陽性と記載され、変異が見つからない場合は EGFR 陰性と記載されます。
ALK
ALKは、他の遺伝子と融合して異常な融合タンパク質を形成し、腫瘍の増殖を促進する遺伝子です。このようなALK融合は、若年患者や喫煙経験のない人に多く見られます。ALK再構成が重要なのは、この変異を有する腫瘍は、異常な融合タンパク質を阻害するALK標的療法に非常によく反応することが多いためです。
ALK 検査は、腫瘍細胞内の ALK タンパク質をハイライトする免疫組織化学、ALK 遺伝子の再編成を検出する FISH、または ALK 遺伝子を直接分析する次世代シーケンシングを使用して実行されます。
腫瘍は、再構成が存在する場合は ALK 陽性、再構成が見つからない場合は ALK 陰性として説明されます。
ROS1
ROS1は、再構成を受け、腫瘍の増殖を刺激する融合タンパク質を形成する遺伝子です。EGFR遺伝子変異やALK遺伝子変異ほど一般的ではありませんが、ROS1融合は、異常なタンパク質を阻害し、がんの制御を助けるROS1標的療法に非常によく反応するため、重要です。
ROS1 テストは、免疫組織化学、FISH、または次世代シーケンシングによって実行して、ROS1 遺伝子融合を検出できます。
融合が見つかった場合、腫瘍は ROS1 陽性と判定され、融合が見つからない場合、腫瘍は ROS1 陰性と判定されます。
ブラフ
BRAFは細胞増殖の制御に関与する遺伝子です。BRAF V600E変異などの特定の変異は、腫瘍細胞の増殖を加速させる可能性があります。これらの変異は、BRAF遺伝子に変異のある腫瘍が、異常なシグナル伝達経路を阻害するBRAF標的療法に反応する可能性があるため、重要です。
検査は、PCR または次世代シーケンシングを使用して腫瘍 DNA を分析し、特定の BRAF 変異を特定することによって行われます。
変異が存在する場合、腫瘍は BRAF 陽性と判定され、変異が検出されない場合は BRAF 陰性と判定されます。
MET
METは正常な細胞増殖を制御する遺伝子です。METエクソン14スキッピングという特定の異常は、METタンパク質の活性化を通常よりも長く持続させ、腫瘍細胞の増殖を抑制されない状態にします。METエクソン14スキッピングを有する腫瘍は、METを標的とした治療に反応することが多いため、このバイオマーカーは重要です。
MET テストは通常、次世代シーケンシングを使用して実行され、MET エクソン 14 スキッピングまたはその他の MET 変異を検出します。
MET 変異が検出された場合、腫瘍は MET 陽性と分類され、変異が見つからない場合、MET 陰性と分類されます。
RET
RET遺伝子は、他の遺伝子と融合して異常なタンパク質を作り出し、腫瘍の増殖を促進します。RET融合遺伝子が重要なのは、この変異を持つ腫瘍は、RETを標的とした治療に非常によく反応することが多いためです。
RET 融合は、次世代シーケンシングまたは FISH を使用して識別されます。どちらも異常な再配列を検出できます。
融合が存在する場合、腫瘍は RET 陽性と説明され、融合が存在しない場合は RET 陰性と説明されます。
NTRK(NTRK1、NTRK2、NTRK3)
NTRK遺伝子は他の遺伝子と融合し、腫瘍の増殖を強く促進する異常なTRK融合タンパク質を形成することがあります。稀ではありますが、これらの融合は重要です。なぜなら、NTRK遺伝子に変異を持つ癌は、TRKを標的とした治療に対して劇的で長期的な反応を示すことが多いからです。
NTRK 検査には、異常な TRK タンパク質発現をスクリーニングするための免疫組織化学検査、続いて遺伝子融合の存在を確認するための FISH または次世代シーケンシングが含まれる場合があります。
融合が見つかった場合、腫瘍は NTRK 陽性と判定され、融合が検出されない場合は NTRK 陰性と判定されます。
クラス
KRASは細胞の成長と分裂を制御する遺伝子です。KRAS変異は肺腺癌において最も一般的なバイオマーカーの一つであり、特に喫煙歴のある患者において顕著です。これらの変異は、腫瘍の挙動を予測するのに役立つこと、そして特定のKRAS変異であるKRAS G12Cは新しいKRAS標的薬で治療できることから重要です。
KRAS 変異は、腫瘍 DNA を分析する PCR または次世代シーケンシングによって検出されます。
変異が特定された場合、腫瘍は KRAS 陽性と判定され、変異が見つからない場合、KRAS 陰性と判定されます。
ERBB2(HER2)
ERBB2(別名HER2)は、変異を起こして異常なシグナル伝達と腫瘍の増殖を引き起こす可能性のある遺伝子です。HER2変異は、標的療法や現在進行中の臨床試験においてHER2変異を持つ腫瘍を標的としているため、重要です。
HER2 検査は、腫瘍の DNA 内の ERBB2 変異を検出するために次世代シーケンシングを使用して実行されます。
変異が検出された場合は腫瘍は ERBB2 陽性と判定され、変異が検出されない場合は ERBB2 陰性と判定されます。
NRAS
NRASはKRASに類似した遺伝子で、細胞増殖経路に関与しています。NRAS変異は喫煙歴のある人に多く見られます。NRASを標的とした特異的な治療法はまだ確立されていませんが、NRAS変異を特定することで、医師は腫瘍の挙動を理解し、臨床試験の選択肢を検討することができます。
NRAS 検査は、腫瘍の DNA の変異を調べるために次世代シーケンシングを使用して実行されます。
変異が検出された場合は腫瘍は NRAS 陽性と判定され、変異が見つからない場合は NRAS 陰性と判定されます。
MAP2K1(MEK1)
MAP2K1(別名MEK1)は、細胞増殖を制御するシグナル伝達経路に関与する遺伝子です。MAP2K1の変異は、この経路を標的とした標的療法が研究されており、治療選択肢となる可能性があるため、重要です。
MAP2K1 検査は、腫瘍 DNA の変異を検出するために次世代シーケンシングを使用して実行されます。
変異が特定された場合、腫瘍は MAP2K1 陽性と判定され、変異が見つからない場合、腫瘍は MAP2K1 陰性と判定されます。
NRG1
NRG1は、腫瘍の増殖を促進する再構成または融合を形成する可能性のある遺伝子です。NRG1再構成は稀ではありますが、現在研究中の新たなNRG1標的治療に感受性を示す可能性があるため、重要です。
NRG1 テストは、次世代シーケンシングを使用して腫瘍 DNA を調べ、遺伝子再構成の証拠を探します。
再構成が検出された場合は腫瘍は NRG1 陽性と判定され、再構成が見つからない場合は NRG1 陰性と判定されます。
PD-L1
PD-L1は、一部の癌細胞の表面に存在するタンパク質です。免疫細胞と相互作用することで、腫瘍は免疫系による攻撃を回避し、破壊を免れます。PD-L1が重要なのは、PD-L1の発現が高い腫瘍は免疫療法に反応する可能性が高くなるためです。免疫療法とは、免疫系が癌細胞を認識して攻撃するのを助ける治療法です。PD-1阻害剤またはPD-L1阻害剤と呼ばれる免疫療法薬は、現在、多くの肺腺癌患者、特に腫瘍のPD-L1レベルが高い患者にとって標準的な治療となっています。
病理医は免疫組織化学を用いてPD-L1の検査を行います。これは、色素に結合した抗体を用いてPD-L1タンパク質に結合させ、顕微鏡下で可視化する検査法です。この検査では、表面にPD-L1を発現している腫瘍細胞の数と、その発現強度を測定します。この検査は通常、治療開始前に生検サンプルを用いて行われます。
PD-L1検査の結果は、PD-L1染色を示す腫瘍細胞の割合を表すパーセンテージで報告されます。これは腫瘍割合スコア(TPS)と呼ばれます。
-
TPS が 1% 未満の場合、PD-L1 陰性または非常に低いとみなされます。
-
TPS が 1 ~ 49% の場合、表現度は低から中程度とみなされます。
-
TPS が 50% 以上の場合、高発現とみなされます。
一部のレポートでは、使用される検査方法に応じて、免疫細胞のスコアが含まれたり、Combined Positive Score (CPS) が使用されたりする場合があります。
診断後
診断が確定した後、医師は病理報告書、画像検査、そしてあなたの全般的な健康状態を検討し、個別の治療計画を作成します。治療には、手術、化学療法、免疫療法、分子標的療法、放射線療法、またはこれらの組み合わせが含まれる場合があります。
腫瘍の分子生物学的検査を受けることは重要です。多くの肺腺がんは、EGFR、ALK、ROS1、KRAS、RETなどの遺伝子変異を有しており、これらは非常に効果的な治療法で標的とすることができます。分子生物学的検査は、現在、早期段階であっても肺がん治療の標準的かつ不可欠な要素となっています。
医療チームは、転移の有無を確認するための追加画像検査、肺活量を評価する肺機能検査、咳や息切れなどの症状の対処法についても話し合うことがあります。治療後のフォローアップは、再発や新たな肺結節の発生をモニタリングするために重要です。
医師に尋ねるべき質問
-
私のがんの進行度はどの段階ですか。また、それは治療計画にどのような影響を与えるのでしょうか。
-
私の腫瘍に胸膜浸潤、リンパ血管浸潤、またはSTASが見つかりましたか?
-
手術マージンはきれいでしたか?
-
がんはリンパ節に転移しましたか?
-
EGFR、ALK、KRAS、またはその他のバイオマーカーの分子検査は必要ですか?
-
どのような治療法をお勧めしますか、またその目標は何ですか?
-
さらなる治療のために腫瘍内科医、放射線腫瘍医、または外科医に診てもらうべきでしょうか?
-
治療後にはどのようなフォローアップスケジュールをお勧めしますか?