door Jason Wasserman MD PhD FRCPC en Zuzanna Gorski MD
30 december 2023
Plaveiselcelcarcinoom (SCC) is de meest voorkomende vorm van kanker in het strottenhoofd. Het ontstaat vaak vanuit een precancereuze aandoening, de zogenaamde precancereuze aandoening keratiniserende squameuze dysplasie. Het treft meestal volwassenen ouder dan 40 jaar.
Dit artikel zal u helpen uw diagnose en pathologierapport voor plaveiselcelcarcinoom van het strottenhoofd te begrijpen.
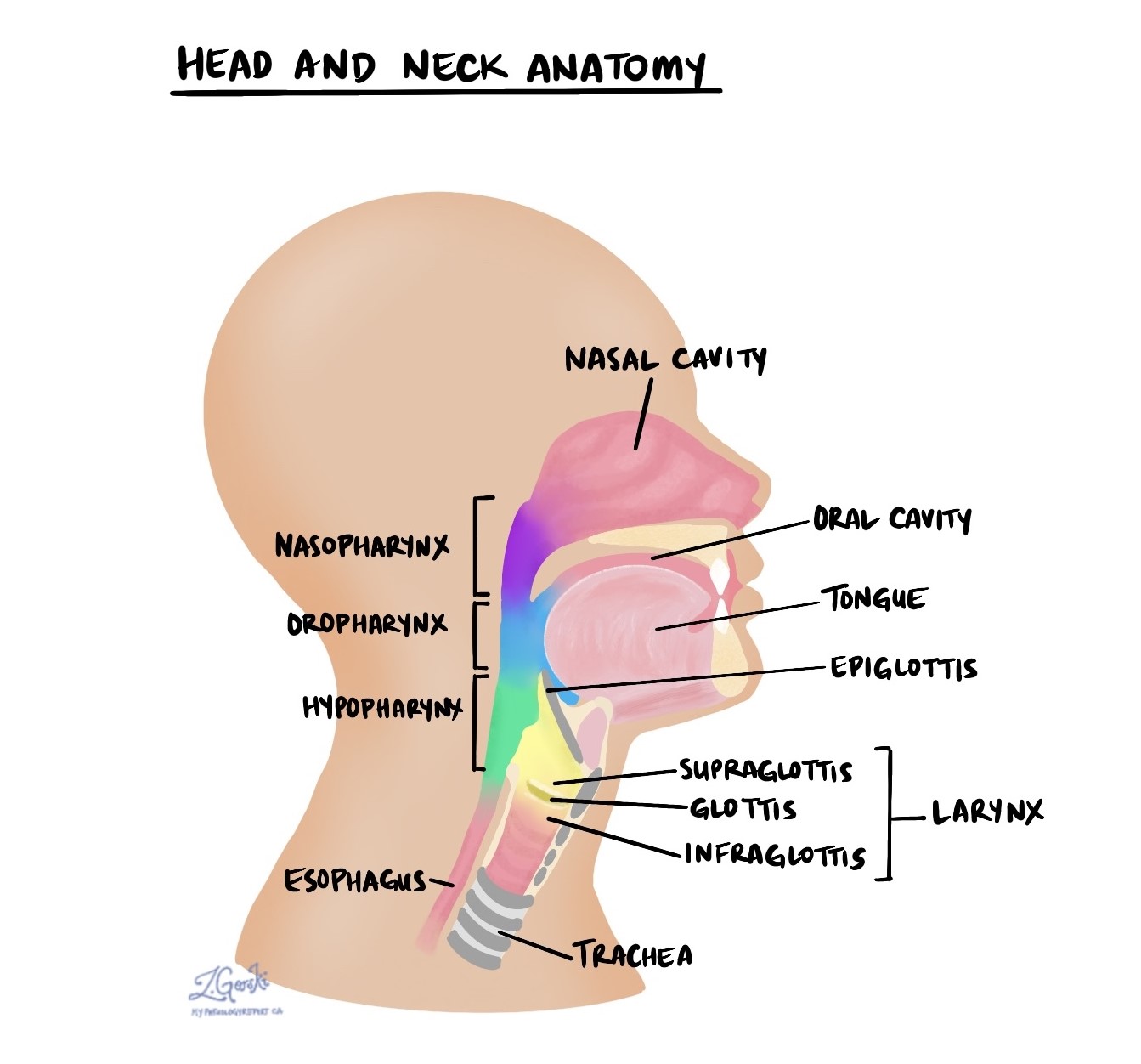
Het strottenhoofd
Het strottenhoofd is een structuur die zich in de bovenste nek bevindt, net boven de luchtpijp. De functies omvatten het beschermen van de luchtwegen en het produceren van geluid. Het is verdeeld in drie delen: de supraglottis, glottis en subglottis. De glottis, die de stembanden omvat, is de meest voorkomende locatie voor plaveiselcelcarcinoom. Naarmate de tumor groeit, kan deze zich echter naar andere delen van het strottenhoofd verspreiden. Dit wordt transglottische extensie genoemd.
Wat veroorzaakt plaveiselcelcarcinoom van het strottenhoofd?
De meest voorkomende oorzaak van plaveiselcelcarcinoom in het strottenhoofd is roken. Andere oorzaken zijn onder meer overmatig alcoholgebruik, onderdrukking van het immuunsysteem en eerdere bestraling van de nek.
Wat zijn de symptomen van plaveiselcelcarcinoom?
Symptomen van plaveiselcelcarcinoom van het strottenhoofd zijn ademhalingsproblemen, heesheid of stemveranderingen en slikproblemen.
Plaveiselcelcarcinoom van het strottenhoofd
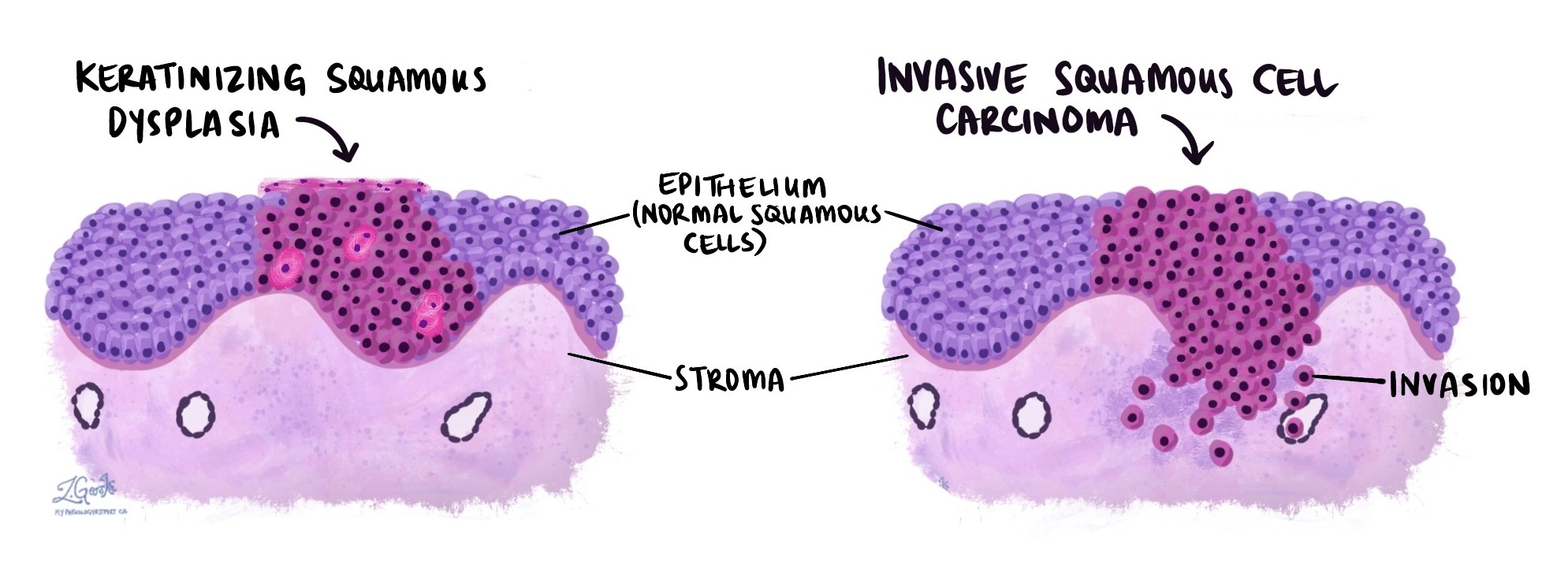
Plaveiselcelcarcinoom begint vanaf plaveiselcellen normaal te vinden in de epitheel, een dunne laag weefsel die het binnenoppervlak van het strottenhoofd bedekt. Het ontwikkelt zich gewoonlijk vanuit een precancereuze aandoening die wordt genoemd keratiniserende squameuze dysplasie (ook wel genoemd hooggradige dysplasie). Bij keratiniserende plaveiseldysplasie bevinden de abnormale plaveiselcellen zich volledig in de huid epitheel. Na verloop van tijd breken de abnormale cellen uit het epitheel en verspreiden zich naar het onderliggende epitheel stroma. Dit proces wordt genoemd invasie en het signaleert de overgang van dysplasie naar invasief plaveiselcelcarcinoom.
Uw pathologierapport voor plaveiselcelcarcinoom van het strottenhoofd
De informatie in uw pathologierapport voor plaveiselcelcarcinoom van het strottenhoofd speelt een belangrijke rol in uw medische zorg. Naast de diagnose zullen de meeste rapporten de tumorgraad (goed, gedifferentieerd, matig gedifferentieerd of slecht gedifferentieerd) vermelden, samen met informatie over de tumorgrootte, de delen van het strottenhoofd die bij de tumor betrokken zijn, de aan- of afwezigheid van perineurale invasie en lymfovasculaire invasieen de beoordeling van marges. Eventueel lymfeklieren tegelijk met de tumor zijn verwijderd, worden ze ook onderzocht op tumorcellen. Deze elementen worden in de onderstaande paragrafen gedetailleerder beschreven.

Tumorgraad
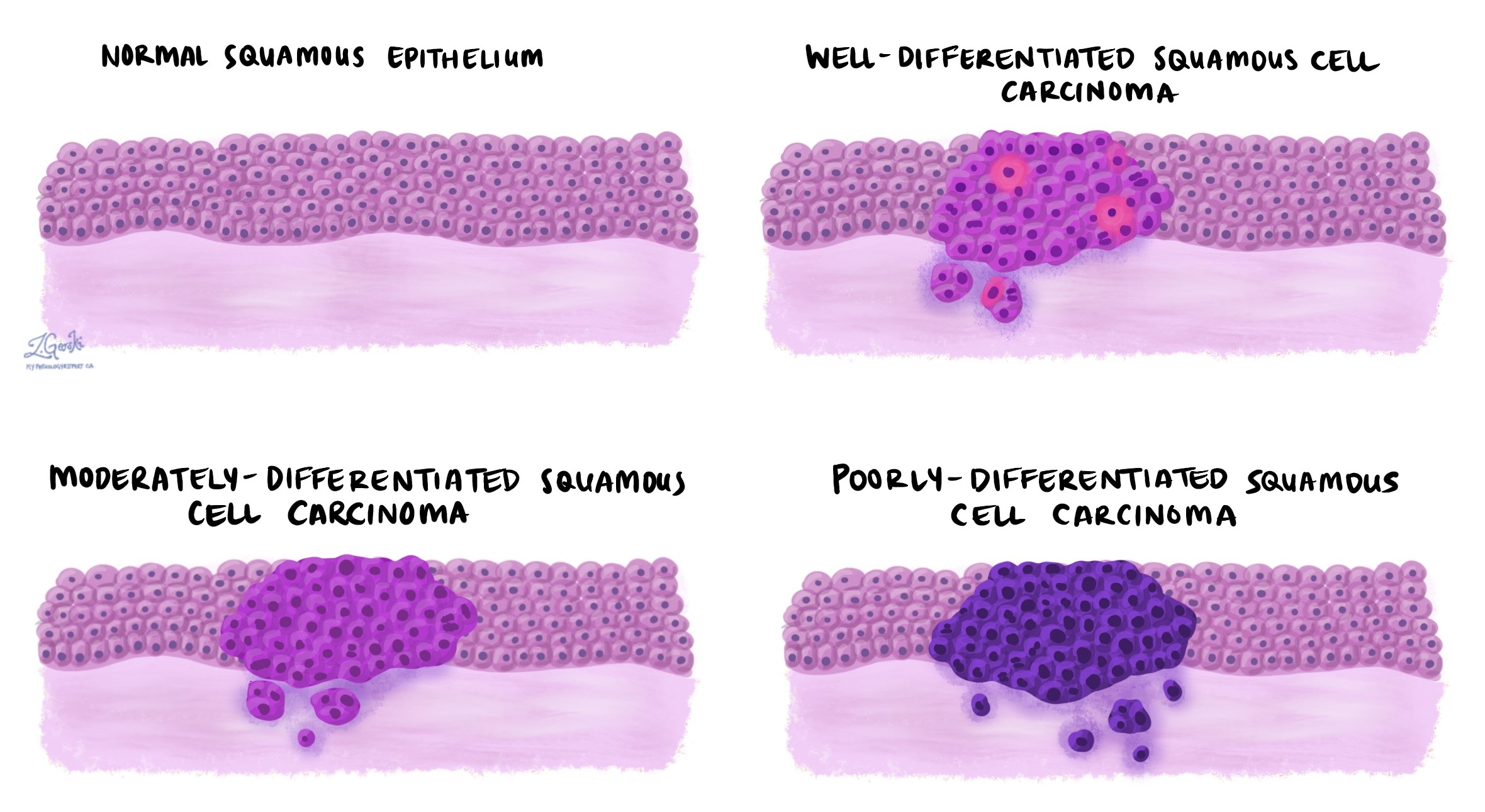
Plaveiselcelcarcinoom van het strottenhoofd is onderverdeeld in drie graden: goed gedifferentieerd, matig gedifferentieerd en slecht gedifferentieerd. Het cijfer is gebaseerd op de mate waarin de tumorcellen op de tumor lijken plaveiselcellen wordt normaal gesproken aangetroffen in het epitheel aan de binnenkant van het strottenhoofd en kan alleen worden vastgesteld nadat de tumor onder de microscoop is onderzocht.
De graad is belangrijk omdat tumoren van een hogere graad (met name slecht gedifferentieerde tumoren) zich agressiever gedragen en na de behandeling waarschijnlijk opnieuw zullen groeien. uitzaaien (verspreid) naar lymfeklieren of andere delen van het lichaam.
Invasief plaveiselcelcarcinoom van het strottenhoofd wordt als volgt geclassificeerd:
- Goed gedifferentieerd – Goed gedifferentieerd plaveiselcelcarcinoom bestaat uit tumorcellen die er bijna hetzelfde uitzien als normale plaveiselcellen.
- Matig gedifferentieerd – Matig gedifferentieerd plaveiselcelcarcinoom bestaat uit tumorcellen die er anders uitzien dan normale plaveiselcellen, maar die nog steeds als plaveiselcellen kunnen worden herkend.
- Slecht gedifferentieerd – Slecht gedifferentieerd plaveiselcelcarcinoom bestaat uit tumorcellen die weinig op normale plaveiselcellen lijken. Deze cellen kunnen er zo abnormaal uitzien dat uw patholoog mogelijk een aanvullende test moet bestellen, zoals: immunohistochemie om de diagnose te bevestigen.
Invasie
Plaveiselcelcarcinoom begint in de epitheel, een dunne laag weefsel aan de binnenkant van het strottenhoofd. Naarmate de tumor groeit, kan deze zich echter verspreiden naar andere delen van het strottenhoofd en nabijgelegen organen, zoals het ringkraakbeen, de schildklier, de voorste zachte weefsels (de weefsels aan de voorkant van de nek, net onder de huid), spieren en botten. Nadat de tumor is verwijderd, wordt al het omliggende weefsel onderzocht op tumorcellen. De resultaten van dit onderzoek worden gebruikt om het pathologische tumorstadium (pT) te bepalen. Tumoren die zich beperken tot het strottenhoofd hebben de neiging zich minder agressief te gedragen, terwijl tumoren die zich verspreiden naar nabijgelegen organen en weefsels dit eerder zullen doen. uitzaaien naar lymfeklieren en na de operatie weer aangroeien.
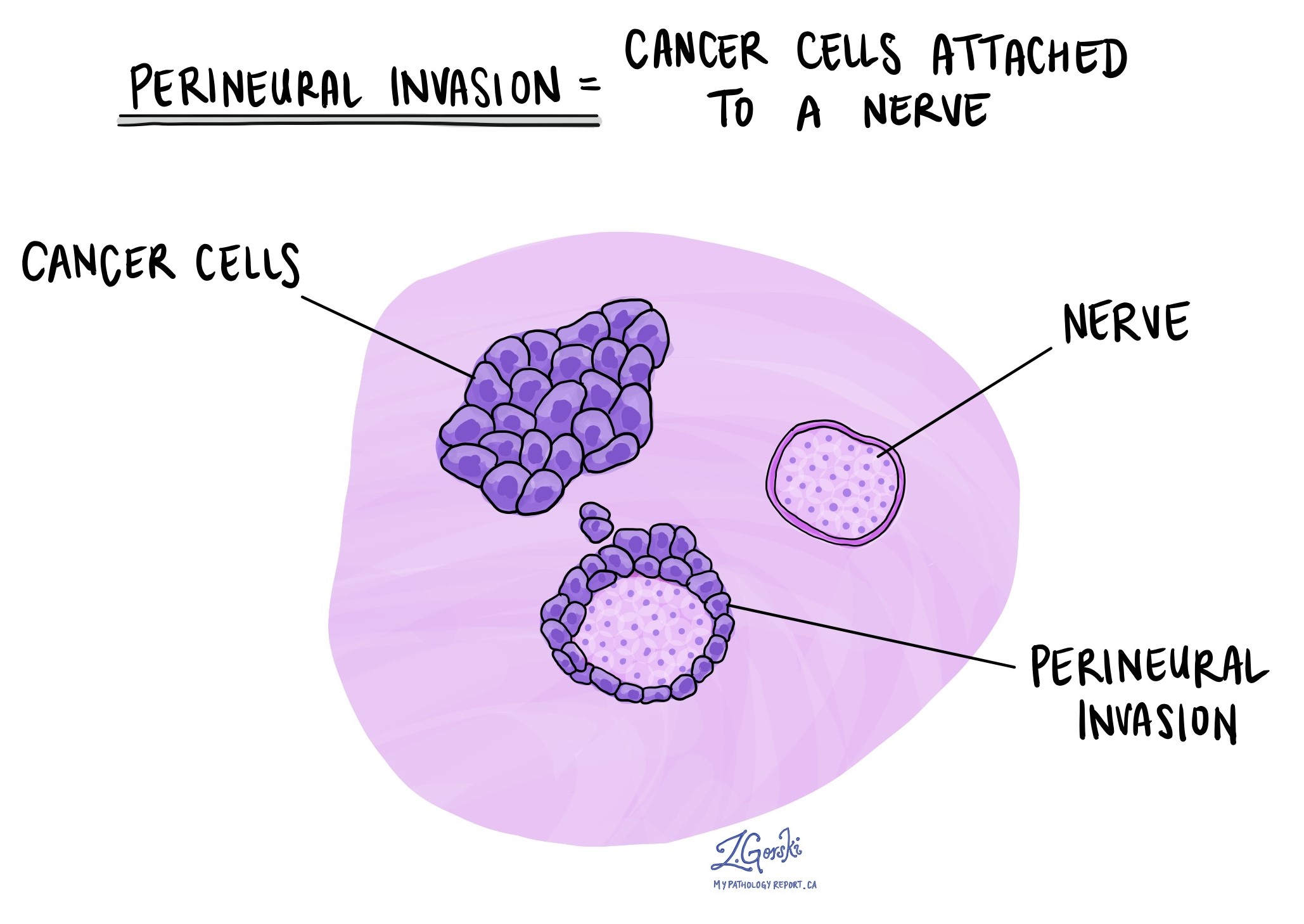
Perineurale invasie
Pathologen gebruiken de term ‘perineurale invasie’ om een situatie te beschrijven waarin kankercellen zich hechten aan een zenuw of deze binnendringen. ‘Intraneurale invasie’ is een verwante term die specifiek verwijst naar kankercellen die in een zenuw worden aangetroffen. Zenuwen, die op lange draden lijken, bestaan uit groepen cellen die bekend staan als neuronen. Deze zenuwen, die door het hele lichaam aanwezig zijn, verzenden informatie zoals temperatuur, druk en pijn tussen het lichaam en de hersenen. De aanwezigheid van perineurale invasie is belangrijk omdat kankercellen hierdoor langs de zenuw naar nabijgelegen organen en weefsels kunnen reizen, waardoor het risico toeneemt dat de tumor na de operatie terugkeert.
Lymfovasculaire invasie
Lymfovasculaire invasie vindt plaats wanneer kankercellen een bloedvat of lymfekanaal binnendringen. Bloedvaten, dunne buisjes die bloed door het lichaam transporteren, staan in contrast met lymfekanalen, die in plaats van bloed een vloeistof transporteren die lymfe wordt genoemd. Deze lymfatische kanalen zijn verbonden met kleine immuunorganen die bekend staan als lymfeklieren, verspreid over het hele lichaam. Lymfovasculaire invasie is belangrijk omdat kankercellen zich hierdoor via het bloed of de lymfevaten kunnen verspreiden naar andere lichaamsdelen, waaronder de lymfeklieren of de longen.

Marges
In de pathologie verwijst een marge naar de rand van het weefsel dat tijdens een tumoroperatie wordt verwijderd. De margestatus in een pathologierapport is belangrijk omdat deze aangeeft of de gehele tumor is verwijderd of dat er een deel is achtergebleven. Deze informatie helpt bij het bepalen van de noodzaak voor verdere behandeling.
Pathologen beoordelen doorgaans de marges na een chirurgische ingreep zoals een uitsnijding or resectie, gericht op het verwijderen van de gehele tumor. Marges worden meestal niet geëvalueerd na een biopsie, waarbij slechts een deel van de tumor wordt verwijderd. Het aantal gerapporteerde marges en hun grootte – hoeveel normaal weefsel zich tussen de tumor en de snijrand bevindt – variëren afhankelijk van het weefseltype en de tumorlocatie.
Pathologen onderzoeken de marges om te controleren of er tumorcellen aanwezig zijn aan de snijrand van het weefsel. Een positieve marge, waar tumorcellen worden gevonden, suggereert dat er mogelijk kanker in het lichaam achterblijft. Daarentegen suggereert een negatieve marge, zonder tumorcellen aan de rand, dat de tumor volledig was verwijderd. Sommige rapporten meten ook de afstand tussen de dichtstbijzijnde tumorcellen en de marge, zelfs als alle marges negatief zijn.

Lymfeklieren
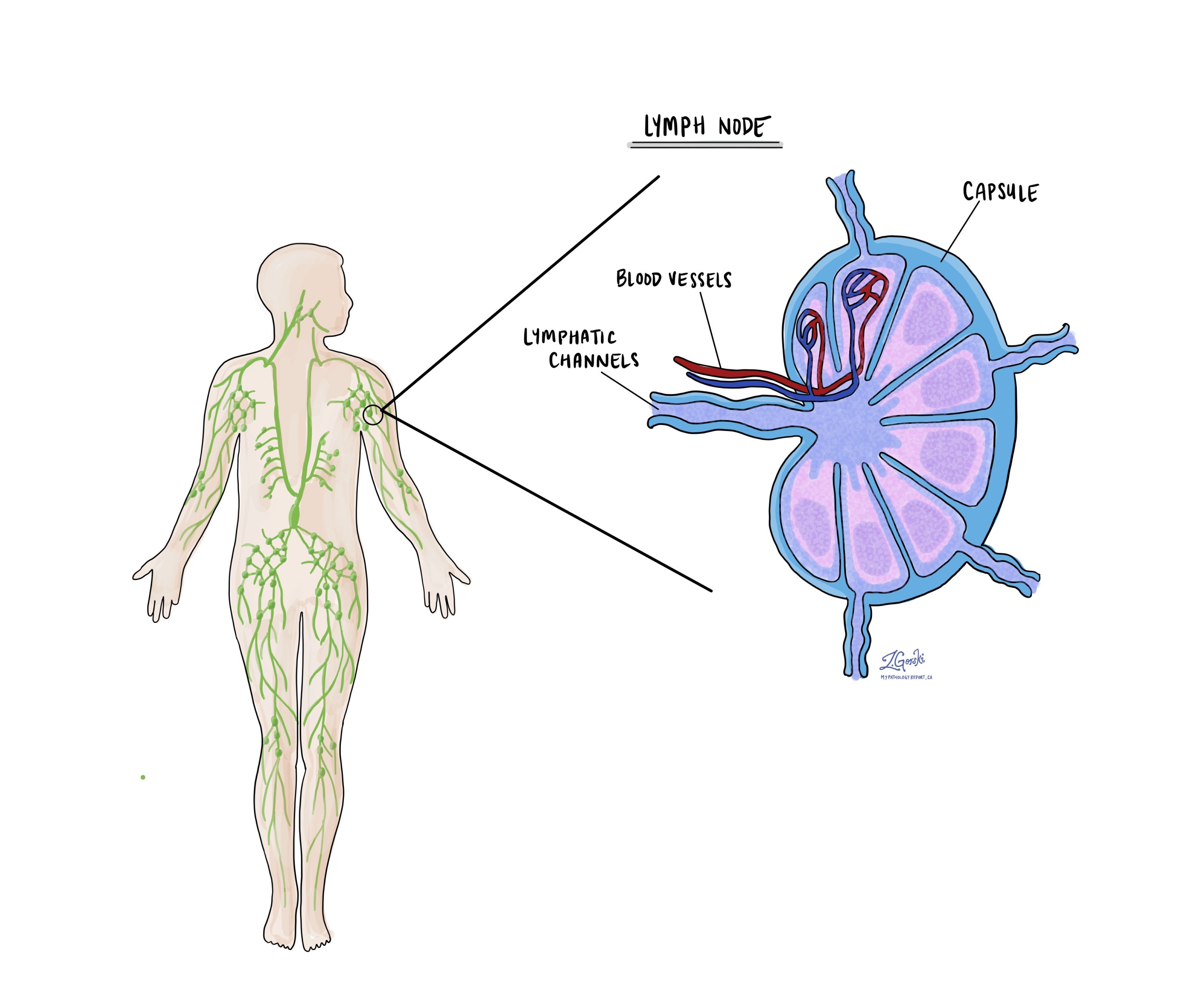
Lymfeklieren zijn kleine immuunorganen die door het hele lichaam worden aangetroffen. Kankercellen kunnen zich via kleine lymfevaten van een tumor naar de lymfeklieren verspreiden. Om deze reden worden lymfeklieren gewoonlijk verwijderd en onder een microscoop onderzocht om te zoeken naar kankercellen. De beweging van kankercellen van de tumor naar een ander deel van het lichaam, zoals een lymfeklier, wordt a genoemd uitzaaiing.
Kankercellen verspreiden zich meestal eerst naar lymfeklieren dicht bij de tumor, hoewel lymfeklieren ver weg van de tumor ook betrokken kunnen zijn. Om deze reden bevinden de eerste verwijderde lymfeklieren zich meestal dicht bij de tumor. Lymfeklieren verder weg van de tumor worden meestal alleen verwijderd als ze vergroot zijn en er een groot klinisch vermoeden bestaat dat er kankercellen in de lymfeklier zitten.
Een nekdissectie is een chirurgische ingreep die wordt uitgevoerd om te verwijderen lymfeklieren uit de nek. De verwijderde lymfeklieren komen meestal uit verschillende delen van de nek en elk gebied wordt een niveau genoemd. De niveaus in de nek omvatten 1, 2, 3, 4 en 5. Uw pathologierapport zal vaak beschrijven hoeveel lymfeklieren er zijn gezien in elk niveau dat voor onderzoek is verzonden. Lymfeklieren aan dezelfde kant van de tumor worden ipsilateraal genoemd, terwijl die aan de andere kant van de tumor contralateraal worden genoemd.
Indien er lymfeklieren uit uw lichaam zijn verwijderd, worden deze door een patholoog onder de microscoop onderzocht. De uitslag van dit onderzoek wordt in uw rapport beschreven. ‘Positief’ betekent dat er kankercellen in de lymfeklier zijn gevonden. ‘Negatief’ betekent dat er geen kankercellen zijn gevonden. Als er kankercellen in een lymfeklier worden aangetroffen, kan de grootte van de grootste groep kankercellen (vaak omschreven als ‘focus’ of ‘afzetting’) ook in uw melding worden opgenomen. Extranodale extensie betekent dat de tumorcellen het kapsel aan de buitenkant van de lymfeklier hebben doorbroken en zich hebben verspreid naar het omliggende weefsel.
Het onderzoek van lymfeklieren is om twee redenen belangrijk. Eerst wordt deze informatie gebruikt om het pathologische nodale stadium (pN) te bepalen. Ten tweede verhoogt het vinden van kankercellen in een lymfeklier het risico dat kankercellen in de toekomst in andere delen van het lichaam worden gevonden. Als gevolg hiervan zal uw arts deze informatie gebruiken bij de beslissing of aanvullende behandeling zoals chemotherapie, bestralingstherapie of immunotherapie nodig is.
Pathologisch stadium
Het pathologische stadium van plaveiselcelcarcinoom van het strottenhoofd is gebaseerd op het TNM-stadiëringssysteem, een internationaal erkend systeem gecreëerd door de Amerikaans Gemengd Comité voor Kanker. Dit systeem gebruikt informatie over de primaire tumor (T), lymfeklieren (N), en verre metastatische ziekte (M) om het volledige pathologische stadium (pTNM) te bepalen. Uw patholoog onderzoekt het ingeleverde weefsel en geeft elk onderdeel een nummer. Over het algemeen betekent een hoger aantal een meer gevorderde ziekte en een slechtere prognose.
Tumorstadium (pT)
Er zijn drie verschillende tumorstadiëringssystemen voor plaveiselcelcarcinoom van het strottenhoofd. Welk systeem wordt gekozen, hangt af van waar in het strottenhoofd de tumor is begonnen.
Supraglottische tumoren
- T1 – De tumor is niet verder uitgezaaid dan de supraglottis en de stembanden bewegen normaal.
- T2– De tumor heeft zich voorbij de supraglottis verspreid naar een ander deel van het strottenhoofd of naar het weefsel net buiten het strottenhoofd.
- T3 – De stembanden bewegen niet meer normaal of de tumor is uitgezaaid naar weefsels verder weg van het strottenhoofd.
- T4 - De tumor is uitgezaaid naar de spieren van de tong, spieren aan de voorkant van de nek, de wervelkolom en de borst, of is door het kraakbeen gegaan dat voor de schildklier zit.
Glottische tumoren
- T1 – De tumor heeft alleen betrekking op de stembanden.
- T2- De tumor heeft zich buiten de glottis verspreid om de supraglottis of subglottis te betrekken of de stembanden bewegen niet meer normaal.
- T3 – De stembanden bewegen niet meer normaal of de tumor is uitgezaaid naar het weefsel net buiten het strottenhoofd.
- T4 - De tumor is uitgezaaid naar de spieren van de tong, spieren aan de voorkant van de nek, de wervelkolom en de borst, of is door het kraakbeen gegaan dat voor de schildklier zit.
Subglottische tumoren
- T1 – De tumor heeft alleen betrekking op de subglottis.
- T2 – De tumor is uitgezaaid naar de stembanden.
- T3 – De stembanden bewegen niet meer normaal of de tumor is uitgezaaid naar het weefsel net buiten het strottenhoofd.
- T4 - De tumor is uitgezaaid naar de spieren van de tong, spieren aan de voorkant van de nek, de wervelkolom en de borst, of is door het kraakbeen gegaan dat voor de schildklier zit.
Nodale fase (pN)
Plaveiselcelcarcinoom van het strottenhoofd krijgt een knoopstadium tussen 0 en 3 op basis van het onderzoek van alle lymfeklieren ontvangen. Zowel N2 als N3 zijn verder onderverdeeld in subfasen (bijvoorbeeld N2a, N2b, etc).
De volgende vier kenmerken worden gebruikt om de nodale fase te bepalen:
- Het aantal lymfeklieren dat kankercellen bevat.
- De grootte van de grootste tumorafzetting.
- Extranodale extensie.
- Of de lymfeklieren met kankercellen zich aan dezelfde of aan de andere kant van de nek bevinden als de hoofdtumor.
Met behulp van deze functies zal uw patholoog als volgt een knoopstadium bieden:
- NX – Er zijn geen lymfeklieren opgestuurd voor pathologisch onderzoek.
- N0 - In de onderzochte lymfeklieren worden geen kankercellen gezien.
- N1 – Kankercellen worden slechts in één lymfeklier gevonden. De lymfeklier met kankercellen bevindt zich aan dezelfde kant als de tumor (ipsilateraal), de tumorafzetting is 3 cm of minder groot en extranodale extensie wordt niet gezien.
- N2a – Er zijn twee mogelijke opties voor ziekte in het N2a-stadium:
- Kankercellen worden slechts in één lymfeklier gevonden. De lymfeklier met kankercellen bevindt zich aan dezelfde kant van de tumor (ipsilateraal), de tumorafzetting meet 3 cm of minder, en extranodale extensie wordt gezien.
- Kankercellen worden slechts in één lymfeklier gevonden. De lymfeklier met kankercellen bevindt zich aan dezelfde kant van de tumor (ipsilateraal), de tumorafzetting meet meer dan 3 cm maar niet meer dan 6 cm, en extranodale extensie wordt niet gezien.
- N2b – Kankercellen komen voor in meer dan één lymfeklier. Alle lymfeklieren met kankercellen bevinden zich aan dezelfde kant als de tumor (ipsilateraal), geen van de tumorafzettingen is groter dan 6 cm en extranodale extensie wordt niet gezien.
- N2c – Kankercellen worden aangetroffen in een of meer lymfeklieren. Ten minste één van de lymfeklieren met kankercellen bevindt zich op de andere kant als de tumor (contralateraal), geen van de tumorafzettingen is groter dan 6 cm en extranodale extensie wordt niet gezien.
- N3a – Kankercellen worden aangetroffen in ten minste één lymfeklier aan dezelfde (ipsilaterale) of tegenoverliggende zijde van de tumor (contralateraal). De grootste tumorafzetting is: meer dan 6 cm groot en extranodale extensie wordt niet gezien.
- N3b – Er zijn drie mogelijke opties voor ziekte in het N3b-stadium:
- Kankercellen worden alleen gevonden in één lymfeklier. De lymfeklier met kankercellen zit aan dezelfde kant van de tumor (ipsilateraal), de tumorafzetting meet meer dan 3 cm en extranodale extensie wordt gezien.
- Kankercellen worden gevonden in meer dan één lymfeklier en extranodale extensie wordt gezien in ten minste één lymfeklier.
- Kankercellen worden slechts in één lymfeklier gevonden. De lymfeklier met kankercellen bevindt zich aan de andere kant van de tumor en extranodale extensie wordt gezien.