Catherine Forse MD FRCPC a Jason Wasserman MD PhD FRCPC
Apríla 23, 2024
Adenokarcinóm (tiež známy ako invazívny adenokarcinóm) je typ rakoviny pažeráka. Ide o najbežnejší typ rakoviny pažeráka vo vyspelých krajinách a vyskytuje sa častejšie u mužov ako u žien. Tento typ rakoviny zvyčajne začína v časti pažeráka nazývanej gastroezofageálne spojenie.
Tento článok vám pomôže prečítať a pochopiť vašu patologickú správu o adenokarcinóme pažeráka.
Pažerák
Ezofág je dutá svalová trubica, ktorá spája hrdlo (hltan) so žalúdkom. Jeho primárnou funkciou je transport potravy a tekutín z úst do žalúdka na trávenie. Pri prehĺtaní sa steny pažeráka sťahujú koordinovane – tento pohyb, nazývaný peristaltika, tlačí potravu smerom nadol. Pažerák má tiež zvierače na oboch koncoch; tieto svalové chlopne sa otvárajú, aby umožnili potrave a tekutinám prejsť do žalúdka a zatvárajú sa, aby sa zabránilo spätnému toku obsahu žalúdka späť do pažeráka a úst.
Aké sú príznaky adenokarcinómu v pažeráku?
Najčastejšími príznakmi adenokarcinómu pažeráka sú ťažkosti s prehĺtaním (najmä pevných potravín), bolesť na hrudníku, zhoršenie kyslého refluxu a strata hmotnosti.
Čo spôsobuje adenokarcinóm pažeráka?
Adenokarcinóm pažeráka najčastejšie vzniká zo stavu tzv Barrettov pažerák čo je spôsobené dlhodobým spätným tokom žalúdočných kyselín do pažeráka (kyslá refluxná choroba). Z tohto dôvodu sa adenokarcinóm v pažeráku často vyvíja po mnohých rokoch refluxu kyseliny.
Keď je vnútro pažeráka dlhodobo vystavené žalúdočnej kyseline, tzv dlaždicové bunky ktoré bežne pokrývajú vnútro pažeráka sú nahradené žľazové bunky ktoré sú podobné bunkám nachádzajúcim sa vo vnútri tenkého čreva. Tieto bunky črevného typu sú odolnejšie voči poraneniu silnými kyselinami vznikajúcimi v žalúdku. Premena skvamóznych buniek na bunky črevného typu sa nazýva črevná metaplázia.
Lekári používajú termín Barrettov pažerák na opis črevnej metaplázie v pažeráku. Je pomenovaná po doktorovi Normanovi R. Barrettovi, chirurgovi, ktorý cvičil v Londýne v Anglicku v 1950. rokoch minulého storočia. Ľudia, ktorí majú Barrettov pažerák po mnoho rokov, môžu vyvinúť typ abnormálneho rastu nazývaného dysplázia, ktorý je spojený so zvýšeným rizikom vzniku adenokarcinómu.
Čo hľadať vo svojej patologickej správe pre invazívny adenokarcinóm pažeráka:
Histologický stupeň
Patológovia používajú termín diferencovaný na rozdelenie adenokarcinómu pažeráka do troch stupňov – dobre diferencovaný, stredne diferencovaný a slabo diferencovaný. Stupeň je založený na percentách nádoru tvoriacich okrúhle štruktúry tzv žaluďov. Nádor, ktorý netvorí žiadne žľazy, sa nazýva nediferencovaný. Stupeň je dôležitý, pretože zle diferencované a nediferencované nádory sa správajú agresívnejšie a je pravdepodobnejšie, že sa rozšíria do iných častí tela, ako napr. lymfatické uzliny.
Adenokarcinóm pažeráka sa klasifikuje takto:
- Dobre diferencovaný adenokarcinóm: Viac ako 95 % nádoru tvoria žľazy. Patológovia tiež popisujú tieto nádory ako 1. stupeň.
- Stredne diferencovaný adenokarcinóm: 50 až 95 % nádoru tvoria žľazy. Patológovia tiež popisujú tieto nádory ako 2. stupeň.
- Zle diferencovaný adenokarcinóm: Menej ako 50 % nádoru tvoria žľazy. Patológovia tiež popisujú tieto nádory ako 3. stupeň.

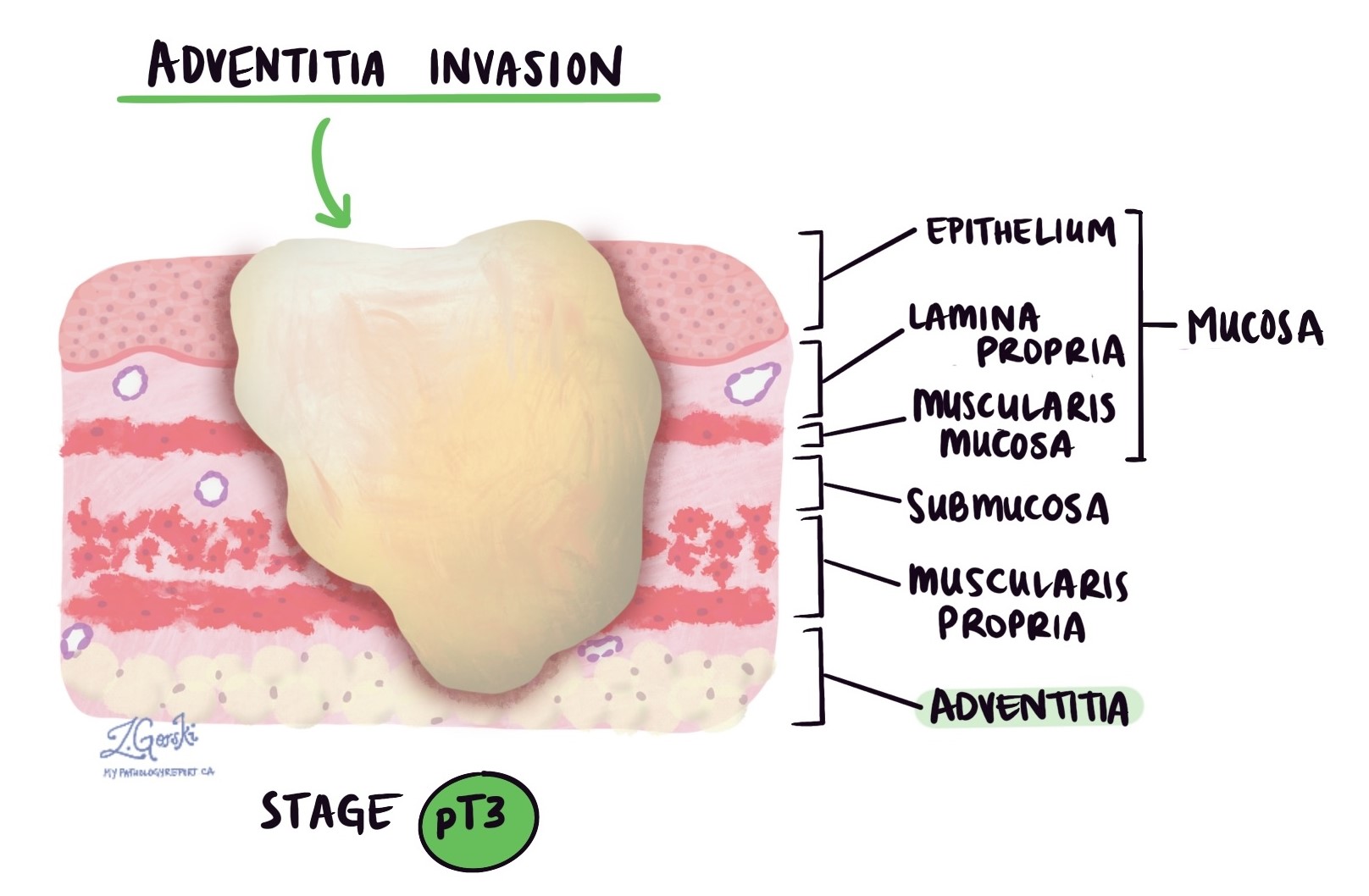
Hĺbka invázie a patologické štádium nádoru (pT)
Adenokarcinóm začína v tenkej vrstve tkaniva vo vnútri pažeráka nazývanej sliznica. Keď je nádor umiestnený úplne v sliznici, je to tzv intramukozálne. Pacienti s intramukóznym adenokarcinómom pažeráka majú celkovo lepšie prognóza pretože nádorové bunky sa menej pravdepodobne šíria do iných častí tela, ako napr lymfatické uzliny.
V patológii, invázie opisuje šírenie rakovinových buniek do orgánov alebo tkanív obklopujúcich miesto, kde nádor začal. Ako nádor v pažeráku rastie, rakovinové bunky sa môžu šíriť do vrstiev tkaniva pod sliznicou. V tomto bode sa ochorenie označuje ako invazívny adenokarcinóm.
Pri skúmaní nádoru pod mikroskopom váš patológ uvidí, ako ďaleko sa rakovinové bunky rozšírili zo sliznice do spodných vrstiev tkaniva. Toto sa nazýva hĺbka alebo úroveň invázie a je to dôležité, pretože nádory, ktoré prenikajú hlbšie, sa s väčšou pravdepodobnosťou rozšíria do iných častí tela, ako napr. lymfatické uzliny, pečeň alebo pľúca. Úroveň invázie sa tiež používa na určenie patologického štádia nádoru (pT). Obrázky nižšie ukazujú vzťah medzi hĺbkou invázie a patologickým štádiom nádoru.



HER2
HER2 je typ proteínu, ktorý funguje ako receptor a funguje ako spínač, ktorý riadi rast a delenie buniek. V niektorých nádorových bunkách sa tvorí nadbytok HER2, čo vedie k oveľa rýchlejšiemu rastu a deleniu ako u normálnych buniek.
Približne jeden z piatich prípadov adenokarcinómu pažeráka zahŕňa nadprodukciu HER2. Špecifické liečby sa zameriavajú na nádory, ktoré produkujú extra HER2. Váš patológ preto môže odporučiť testovanie nádoru na prebytok HER2, aby sa určil najlepší liečebný prístup.
Najbežnejšou metódou na detekciu HER2 pri adenokarcinóme je test nazývaný imunohistochémia. Výsledky tohto testu sa zvyčajne uvádzajú nasledujúcim spôsobom:
- Negatívne (0 alebo 1) – Nádorové bunky neprodukujú extra HER2.
- Nejednoznačné (2) – Nádorové bunky môžu produkovať extra HER2. V tomto prípade vám patológovia zvyčajne vykonajú laboratórne vyšetrenie tzv fluorescenčná in situ hybridizácia (FISH) aby sa zistilo, či nádorové bunky majú viac génových kópií HER2. To môže pomôcť určiť, či nádor exprimuje viac proteínu HER2.
- Pozitívne (3) – Nádorové bunky určite produkujú extra množstvá HER2.
Mismatch repair proteíny
Mismatch repair (MMR) je systém vo všetkých normálnych, zdravých bunkách, ktorý opravuje chyby v našom genetickom materiáli (DNA). Systém obsahuje rôzne proteíny a štyri najbežnejšie sú MSH2, MSH6, MLH1 a PMS2.
Štyri chybné opravné proteíny MSH2, MSH6, MLH1 a PMS2 pracujú v pároch na opravu poškodenej DNA. Konkrétne MSH2 spolupracuje s MSH6 a MLH1 pracuje s PMS2. Ak dôjde k strate jedného proteínu, pár nemôže normálne fungovať a zvyšuje sa riziko vzniku rakoviny.
Najbežnejším spôsobom testovania proteínov na opravu nesúladu je imunohistochémia. Tento test umožňuje patológom zistiť, či nádorové bunky produkujú všetky štyri chybné opravné proteíny. Výsledky tohto testu sa zvyčajne uvádzajú takto:
- Normálny výsledok: Zachovaná expresia proteínu.
- Abnormálny výsledok: Strata expresie bielkovín.
Testovanie opravy nesúladu je dôležité, pretože môže pomôcť predpovedať, ako dobre môžu niektoré liečby fungovať. Napríklad rakoviny so stratou expresie chybného opravného proteínu budú s väčšou pravdepodobnosťou reagovať na imunoterapeutické liečby, ako sú inhibítory PD-1 alebo PD-L1. Je to preto, že vysoký počet mutácií, ktoré sa často nachádzajú v nedostatočných nádoroch, môže produkovať nové antigény, vďaka ktorým je nádor viditeľnejší a zraniteľnejší voči imunitnému systému.
Testovanie opravy nesúladu sa vykonáva aj na identifikáciu pacientov, ktorí môžu mať Lynchov syndróm, známy aj ako dedičný nepolypózny kolorektálny karcinóm (HNPCC). Lynchov syndróm je genetická porucha, ktorá zvyšuje riziko vzniku rôznych typov rakoviny, vrátane rakoviny pažeráka, rakoviny hrubého čreva, rakoviny endometria, rakoviny vaječníkov a rakoviny žalúdka.
PD-L1
PD-L1 (Programmed Death-Ligand 1) je proteín nachádzajúci sa na povrchu normálnych, zdravých buniek a niektorých rakovinových buniek. Nazýva sa to proteín kontrolného bodu imunity, pretože spomaľuje aktivitu imunitných buniek nazývaných T bunky. Tieto bunky normálne detegujú abnormálne bunky, ako sú rakovinové bunky, a odstraňujú ich z tela. Rakovinové bunky, ktoré exprimujú tento proteín, unikajú útoku T buniek aktiváciou proteínu na T bunke nazývaného PD-1.
Lekári testujú tento proteín, aby pomohli určiť, ktorí pacienti môžu mať prospech z liečby, ktorá sa zameriava na dráhu PD-1/PD-L1, ako sú inhibítory kontrolných bodov imunity. Na testovanie expresie PD-L1 patológovia zvyčajne vykonávajú test tzv imunohistochémia na vzorke nádorového tkaniva. V tomto teste sa špecifická protilátka proti PD-L1 aplikuje na tkanivový rez a potom sa deteguje pomocou sekundárnej protilátky pripojenej k farbivu.
Úroveň expresie proteínu sa potom spočíta a vyhodnotí na základe intenzity a percenta pozitívnych buniek. V prípade rakoviny pažeráka sa výsledok uvádza ako kombinované pozitívne skóre (CPS), pričom skóre > 1 sa považuje za pozitívne.
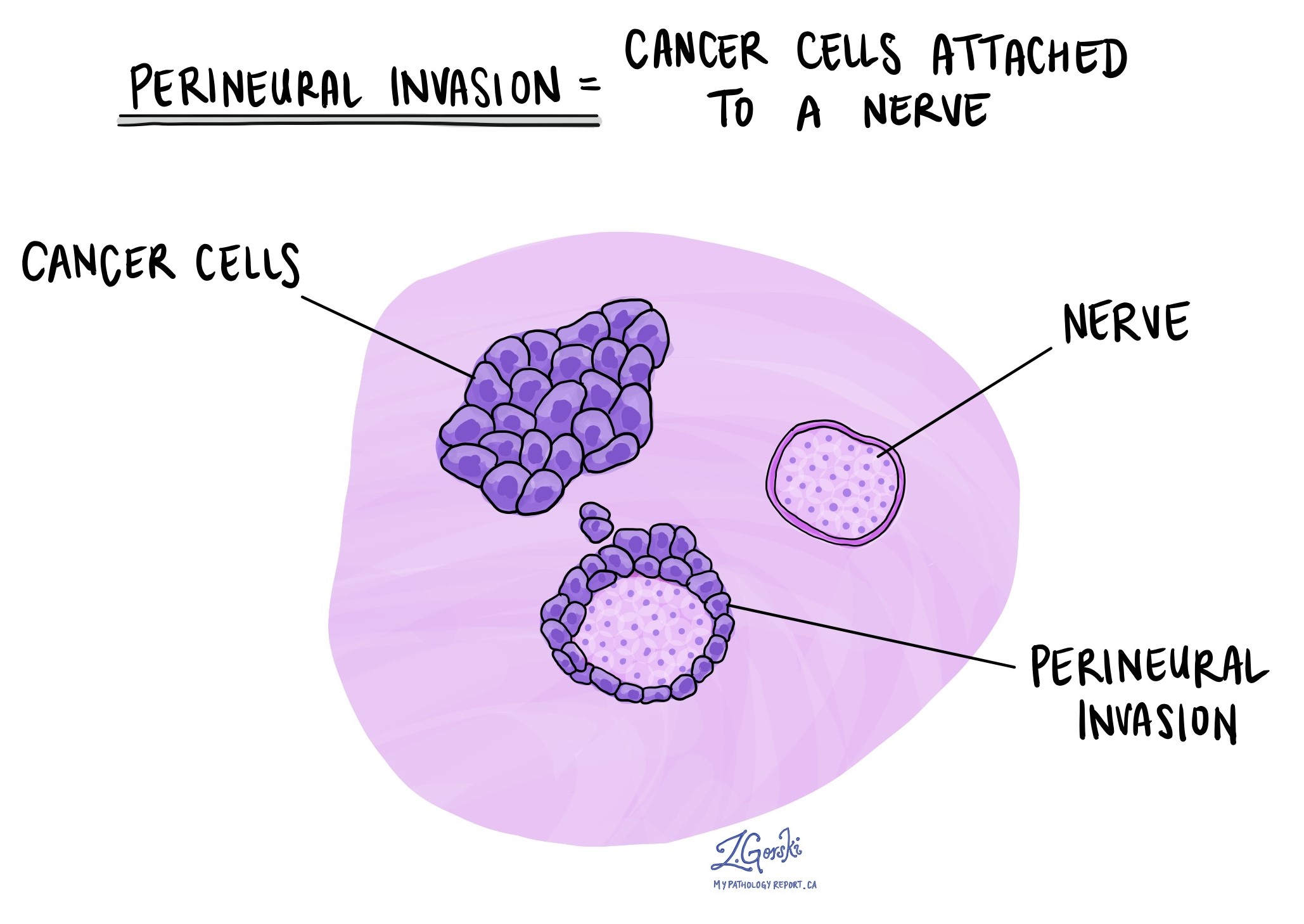
Perineurálna invázia
Patológovia používajú termín „perineurálna invázia“ na opis situácie, keď sa rakovinové bunky prichytia k nervu alebo napadnú nerv. „Intraneurálna invázia“ je príbuzný výraz, ktorý sa špecificky vzťahuje na rakovinové bunky nachádzajúce sa vo vnútri nervu. Nervy, pripomínajúce dlhé drôty, pozostávajú zo skupín buniek známych ako neuróny. Tieto nervy, prítomné v celom tele, prenášajú medzi telom a mozgom informácie, ako je teplota, tlak a bolesť. Prítomnosť perineurálnej invázie je dôležitá, pretože umožňuje rakovinovým bunkám cestovať pozdĺž nervu do blízkych orgánov a tkanív, čím sa zvyšuje riziko recidívy nádoru po operácii.
Lymfovaskulárna invázia
Lymfovaskulárna invázia nastáva, keď rakovinové bunky napadnú krvnú cievu alebo lymfatickú cievu. Krvné cievy sú tenké trubice, ktoré prenášajú krv po celom tele, zatiaľ čo lymfatické cievy nesú tekutinu nazývanú lymfa namiesto krvi. Tieto lymfatické cievy sa spájajú s malými imunitnými orgánmi roztrúsenými po celom tele, tzv lymfatické uzliny. Lymfovaskulárna invázia je dôležitá, pretože umožňuje rakovinovým bunkám šíriť sa do iných častí tela, vrátane lymfatických uzlín alebo pečene, cez krv alebo lymfatické cievy.

Okraje
V patológii je okraj okrajom tkaniva odstráneného počas operácie nádoru. Stav okraja v správe o patológii je dôležitý, pretože naznačuje, či bol odstránený celý nádor alebo či nejaký zostal. Tieto informácie pomáhajú určiť potrebu ďalšej liečby.
Patológovia zvyčajne hodnotia okraje po chirurgickom zákroku, ako je napr vyrezanie or resekcia, ktorá odstráni celý nádor. Okraje sa zvyčajne nevyhodnocujú po a biopsia, ktorý odstráni len časť nádoru.
pre endoskopické resekcie tam, kde bola odstránená iba malá časť vnútornej strany pažeráka, okraje budú zahŕňať:
- Okraj sliznice – Toto je tkanivo, ktoré lemuje vnútorný povrch pažeráka. Iný názov pre tento okraj je laterálny okraj.
- Hlboký okraj - Toto tkanivo sa nachádza vo vnútri steny pažeráka. Nachádza sa pod nádorom.
pre vzorky z ezofagektómie ak bol odstránený celý segment pažeráka, okraje budú zahŕňať:
- Proximálny okraj - Tento okraj sa nachádza v blízkosti hornej časti pažeráka, bližšie k ústam.
- Distálny okraj - Tento okraj sa nachádza v blízkosti spodnej časti pažeráka. Distálny okraj môže byť v pažeráku alebo žalúdku.
- Radiálny okraj – Toto je tkanivo okolo vonkajšej strany pažeráka.
Patológovia skúmajú okraje, aby skontrolovali, či sú na reze tkaniva prítomné nádorové bunky. Pozitívny okraj, kde sa nachádzajú nádorové bunky, naznačuje, že určitá rakovina môže zostať v tele. Naopak, negatívny okraj bez nádorových buniek na okraji naznačuje, že nádor bol úplne odstránený. Niektoré správy tiež merajú vzdialenosť medzi najbližšími nádorovými bunkami a okrajom, aj keď sú všetky okraje negatívne.

Lymfatické uzliny
Malé imunitné orgány, tzv lymfatické uzliny, sa nachádzajú v celom tele. Rakovinové bunky môžu cestovať z nádoru do týchto lymfatických uzlín cez drobné lymfatické cievy. Z tohto dôvodu lekári často odstraňujú a mikroskopicky skúmajú lymfatické uzliny, aby hľadali rakovinové bunky. Tento proces, pri ktorom sa rakovinové bunky presúvajú z pôvodného nádoru do inej časti tela, ako je lymfatická uzlina, sa nazýva metastáza.
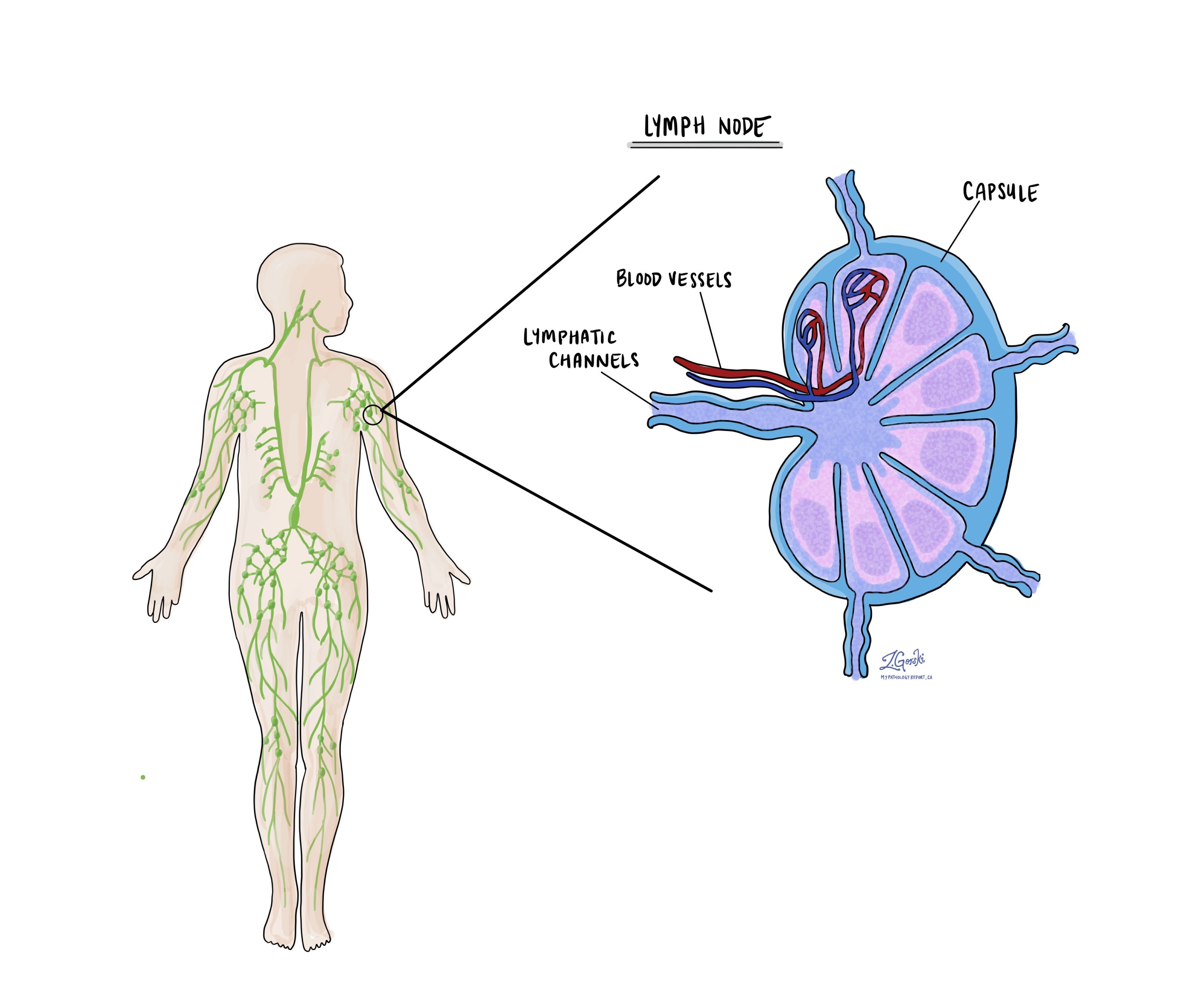
Rakovinové bunky zvyčajne najskôr migrujú do lymfatických uzlín v blízkosti nádoru, hoci môžu byť postihnuté aj vzdialené lymfatické uzliny. V dôsledku toho chirurgovia zvyčajne najskôr odstraňujú lymfatické uzliny najbližšie k nádoru. Môžu odstrániť lymfatické uzliny ďalej od nádoru, ak sú zväčšené a existuje silné podozrenie, že obsahujú rakovinové bunky.
Patológovia preskúmajú všetky odstránené lymfatické uzliny pod mikroskopom a zistenia budú podrobne uvedené vo vašej správe. „Pozitívny“ výsledok znamená prítomnosť rakovinových buniek v lymfatických uzlinách, zatiaľ čo „negatívny“ výsledok znamená, že neboli nájdené žiadne rakovinové bunky. Ak správa nájde rakovinové bunky v lymfatických uzlinách, môže tiež špecifikovať veľkosť najväčšieho zhluku týchto buniek, ktorý sa často označuje ako „focus“ alebo „depozit“. Extranodálne predĺženie nastáva, keď nádorové bunky prenikajú do vonkajšieho puzdra lymfatických uzlín a šíria sa do susedného tkaniva.
Vyšetrenie lymfatických uzlín je dôležité z dvoch dôvodov. Po prvé, pomáha určiť patologické uzlové štádium (pN). Po druhé, objavenie rakovinových buniek v lymfatických uzlinách naznačuje zvýšené riziko neskoršieho nájdenia rakovinových buniek v iných častiach tela. Tieto informácie vedú vášho lekára pri rozhodovaní, či potrebujete ďalšie liečby, ako je chemoterapia, rádioterapia alebo imunoterapia.
Patologické nodálne štádium (pN) pre adenokarcinóm pažeráka:
- N0 – V žiadnej z vyšetrovaných lymfatických uzlín nie sú viditeľné žiadne nádorové bunky.
- N1 - Nádorové bunky sú viditeľné v jednej alebo dvoch lymfatických uzlinách.
- N2 - Nádorové bunky sú viditeľné v troch až šiestich lymfatických uzlinách.
- N3 – Nádorové bunky sa vyskytujú vo viac ako šiestich lymfatických uzlinách.
- NX – Patológovi neboli odoslané žiadne lymfatické uzliny na vyšetrenie.
Účinok liečby
Ak ste podstúpili liečbu rakoviny (buď chemoterapiu alebo radiačnú terapiu alebo oboje) pred odstránením nádoru, váš patológ starostlivo vyšetrí oblasť tkaniva, kde bol predtým identifikovaný nádor, aby zistil, či sú nejaké rakovinové bunky stále živé (životaschopné). Najčastejšie používaný systém popisuje účinok liečby na stupnici od 0 do 3, pričom 0 znamená žiadne životaschopné rakovinové bunky (všetky rakovinové bunky sú mŕtve) a 3 predstavuje rozsiahlu reziduálnu rakovinu bez zjavnej regresie nádoru (všetky alebo väčšina rakovinové bunky sú živé).
O tomto článku
Lekári napísali tento článok, aby vám pomohol prečítať a pochopiť vašu správu o patológii. Kontaktujte nás s akýmikoľvek otázkami týkajúcimi sa tohto článku alebo vašej patologickej správy. Čítať tento článok pre všeobecnejší úvod do častí typickej správy o patológii.


