जेसन वासरमैन एमडी पीएचडी एफआरसीपीसी द्वारा
फ़रवरी 6, 2026
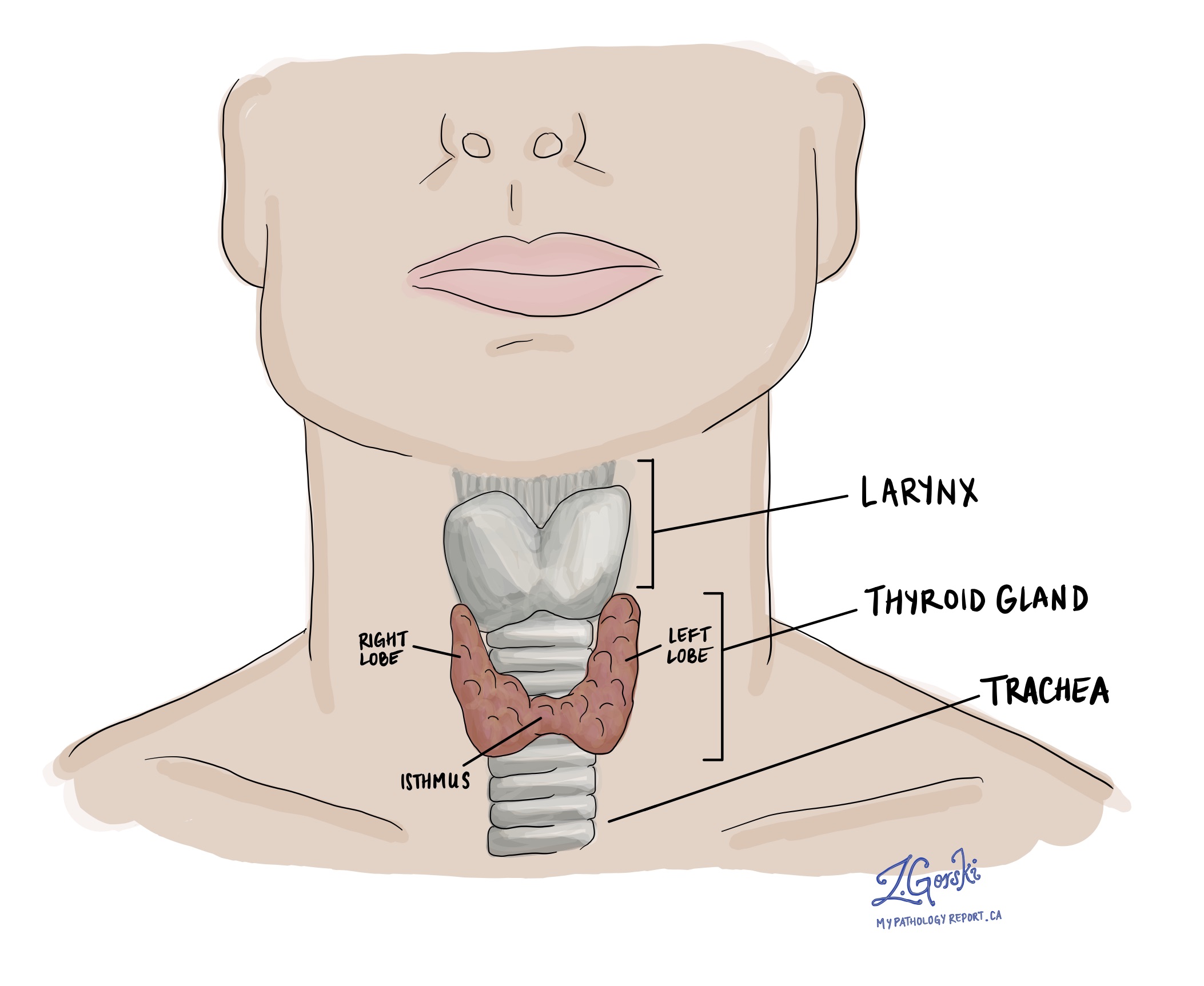
कूपिक थायरॉयड कार्सिनोमा यह एक प्रकार का थायरॉइड कैंसर है जो फॉलिक्युलर कोशिकाओं से शुरू होता है, ये कोशिकाएं थायरॉइड ग्रंथि में थायरॉइड हार्मोन का उत्पादन करती हैं। थायरॉइड गर्दन के सामने स्थित एक छोटी, तितली के आकार की ग्रंथि है जो शरीर द्वारा ऊर्जा के उपयोग को नियंत्रित करने में मदद करती है।
इस कैंसर को अच्छी तरह से विभेदित माना जाता है, जिसका अर्थ है कि ट्यूमर कोशिकाएं सूक्ष्मदर्शी से देखने पर भी सामान्य थायरॉइड कोशिकाओं जैसी दिखती हैं। फॉलिक्युलर थायरॉइड कार्सिनोमा को कैंसर क्यों कहा जाता है, जबकि इसे सामान्य थायरॉइड कैंसर नहीं माना जाता? सौम्य ट्यूमर, है आक्रमणआक्रमण का अर्थ है कि ट्यूमर कोशिकाएं ट्यूमर कैप्सूल (ट्यूमर के चारों ओर ऊतक की पतली परत) से होकर बढ़ गई हैं और/या आसपास की रक्त वाहिकाओं में प्रवेश कर गई हैं।
यह लेख बताता है कि फॉलिक्युलर थायरॉइड कार्सिनोमा का निदान, वर्गीकरण और मूल्यांकन कैसे किया जाता है, और इसमें कौन-कौन सी विशेषताएं पाई जाती हैं। पैथोलॉजिस्ट किन बातों का पता लगाना है, और ये निष्कर्ष रोग के पूर्वानुमान और उपचार से कैसे संबंधित हैं।
फॉलिक्युलर थायरॉइड कार्सिनोमा कितना आम है?
फॉलिक्युलर थायरॉइड कार्सिनोमा थायरॉइड कैंसर के लगभग 5-15% मामलों के लिए जिम्मेदार है। यह अन्य कैंसरों की तुलना में कम आम है। पैपिलरी थायरॉयड कार्सिनोमा और यह बच्चों की तुलना में वयस्कों में अधिक बार होता है। दुनिया के उन हिस्सों में इसकी दर अधिक है जहां आहार में आयोडीन का सेवन कम होता है।
फॉलिक्युलर थायरॉइड कार्सिनोमा के लक्षण क्या हैं?
कई लोगों को सबसे पहले गर्दन में एक दर्द रहित गांठ का पता चलता है, जो आमतौर पर थायरॉइड ग्रंथि के क्षेत्र में होती है। कुछ ट्यूमर इमेजिंग या नियमित शारीरिक परीक्षण के दौरान संयोगवश पाए जाते हैं।
बड़े ट्यूमर आसपास की संरचनाओं पर दबाव से संबंधित लक्षण पैदा कर सकते हैं, जैसे निगलने में कठिनाई, आवाज में भारीपन या गर्दन में जकड़न महसूस होना। अधिकांश रोगियों में थायरॉइड हार्मोन का स्तर सामान्य होता है, इसलिए थायरॉइड की अतिसक्रियता या अल्पसक्रियता के लक्षण असामान्य हैं।
कुछ मामलों में, कैंसर फेफड़े या हड्डियों जैसे दूरस्थ अंगों तक फैल चुका होता है। ऐसी स्थिति में, लक्षण उसी स्थान से उत्पन्न हो सकते हैं जहां कैंसर फैला है, जैसे हड्डियों में दर्द या सांस लेने में तकलीफ।
फॉलिक्युलर थायरॉइड कार्सिनोमा का क्या कारण है?
इसका सटीक कारण हमेशा ज्ञात नहीं होता है। कई कारक जोखिम को बढ़ा सकते हैं, जिनमें आयोडीन की कमी, विकिरण के संपर्क में आना (विशेषकर बचपन में), और वंशानुगत ट्यूमर सिंड्रोम जैसे कि PTEN हैमार्टोमा ट्यूमर सिंड्रोम (काउडन सिंड्रोम), DICER1 सिंड्रोम, वर्नर सिंड्रोम और कार्नी कॉम्प्लेक्स शामिल हैं।
अधिकांश मामले छिटपुट होते हैं, जिसका अर्थ है कि वे संयोगवश होते हैं और वंशानुगत नहीं होते हैं।
फॉलिक्युलर थायरॉइड कार्सिनोमा का निदान कैसे किया जाता है?
फॉलिक्युलर थायरॉइड कार्सिनोमा के निदान के लिए कई चरणों की आवश्यकता होती है क्योंकि इस ट्यूमर का निश्चित निदान केवल इमेजिंग या नीडल बायोप्सी के आधार पर नहीं किया जा सकता है।
निदान प्रक्रिया में आमतौर पर इमेजिंग अध्ययन शामिल होते हैं। फाइन-नीडल एस्पिरेशन (एफएनए) बायोप्सीइसमें ट्यूमर को शल्य चिकित्सा द्वारा निकालना और सूक्ष्मदर्शी से सावधानीपूर्वक जांच करना शामिल है। अंतिम निदान लगभग हमेशा सर्जरी के बाद ही किया जाता है, जब ट्यूमर कैप्सूल और आसपास की रक्त वाहिकाओं की पूरी तरह से जांच की जा सकती है।
इमेजिंग
अल्ट्रासाउंड आमतौर पर पहला इमेजिंग परीक्षण होता है। फॉलिक्युलर थायरॉइड कार्सिनोमा अक्सर एक ठोस, स्पष्ट थायरॉइड नोड्यूल के रूप में दिखाई देता है, कभी-कभी ट्यूमर कैप्सूल के कारण इसके चारों ओर एक घेरा भी दिखाई देता है। इमेजिंग द्वारा फॉलिक्युलर थायरॉइड कार्सिनोमा और सौम्य फॉलिक्युलर एडेनोमा के बीच सटीक अंतर करना संभव नहीं है।
फाइन-सुई एस्पिरेशन (FNA)
एफएनए से यह पता चल सकता है कि ट्यूमर फॉलिक्युलर कोशिकाओं से बना है, लेकिन इससे यह निर्धारित नहीं किया जा सकता कि ट्यूमर सौम्य है या घातक। ऐसा इसलिए है क्योंकि छोटे बायोप्सी नमूनों पर आक्रमण का आकलन नहीं किया जा सकता है। परिणामस्वरूप, एफएनए रिपोर्ट में अक्सर ऐसे शब्दों का प्रयोग किया जाता है जैसे कि कूपिक रसौली or कूपिक रसौली के लिए संदिग्धऔर निदान की पुष्टि के लिए सर्जरी आवश्यक है।
सूक्ष्म विशेषताएं
सूक्ष्मदर्शी से देखने पर, फॉलिक्युलर थायरॉइड कार्सिनोमा फॉलिक्युलर कोशिकाओं से बना होता है जो फॉलिकल्स (गोल स्थान जो सामान्यतः थायरॉइड हार्मोन संग्रहित करते हैं) में व्यवस्थित होती हैं या ठोस या ट्रेबेक्युलर वृद्धि पैटर्न में पाई जाती हैं। ट्यूमर कोशिकाएं सौम्य ट्यूमर की कोशिकाओं के समान होती हैं। कूपिक ग्रंथ्यर्बुदलेकिन मुख्य अंतर उनकी आक्रामक प्रकृति है।
कैप्सुलर इनवेज़न का अर्थ है कि ट्यूमर कोशिकाएं ट्यूमर कैप्सूल को पूरी तरह से भेदकर विकसित हो गई हैं। वैस्कुलर इनवेज़न का अर्थ है कि ट्यूमर कोशिकाएं रक्त वाहिकाओं के अंदर पाई जाती हैं, अक्सर वाहिका की दीवार से जुड़ी होती हैं या रक्त के थक्के के साथ मिश्रित होती हैं। फॉलिक्युलर थायरॉइड कार्सिनोमा के निदान के लिए कैप्सुलर या वैस्कुलर इनवेज़न के कम से कम एक केंद्र की पहचान करना आवश्यक है।
इम्युनोहिस्टोकैमिस्ट्री
इम्युनोहिस्टोकैमिस्ट्री यह एक प्रयोगशाला परीक्षण है जिसमें ट्यूमर कोशिकाओं में विशिष्ट प्रोटीन का पता लगाने के लिए एंटीबॉडी का उपयोग किया जाता है। फॉलिक्युलर थायरॉइड कार्सिनोमा में, ट्यूमर कोशिकाएं आमतौर पर थायरोग्लोबुलिन, टीटीएफ-1 और पीएएक्स8 व्यक्त करती हैं, जो इस बात की पुष्टि करता है कि ट्यूमर थायरॉइड फॉलिक्युलर कोशिकाओं से शुरू हुआ था।
ये परीक्षण ट्यूमर के मूल स्थान की पुष्टि करने और अन्य प्रकार के कैंसर को खारिज करने में सहायक होते हैं। हालांकि, इम्यूनोहिस्टोकेमिस्ट्री फॉलिक्युलर थायरॉइड कार्सिनोमा और फॉलिक्युलर एडेनोमा के बीच सटीक अंतर नहीं कर सकती। निदान अभी भी माइक्रोस्कोप के नीचे आक्रमण की पहचान पर निर्भर करता है।
ट्यूमर का वर्गीकरण (उपप्रकार)
फॉलिक्युलर थायरॉइड कार्सिनोमा को आसपास की संरचनाओं में ट्यूमर के फैलाव के आधार पर उपप्रकारों में विभाजित किया जाता है। यह वर्गीकरण महत्वपूर्ण है क्योंकि यह रोग के पूर्वानुमान और अनुवर्ती उपचार को बहुत प्रभावित करता है।
मिनिमली इनवेसिव फॉलिक्युलर थायरॉयड कार्सिनोमा
न्यूनतम आक्रमणकारी ट्यूमर केवल कैप्सूल तक ही सीमित रहते हैं, यानी ट्यूमर कोशिकाएं कैप्सूल से होकर तो बढ़ जाती हैं लेकिन रक्त वाहिकाओं में प्रवेश नहीं करतीं। ये ट्यूमर आमतौर पर अच्छी तरह से नियंत्रित होते हैं और धीमी गति से बढ़ते हैं। पूरी तरह से निकाले जाने पर रोग का पूर्वानुमान उत्कृष्ट होता है और अक्सर अतिरिक्त उपचार की आवश्यकता नहीं होती है।
एनकैप्सुलेटेड एंजियोइनवेसिव फॉलिक्युलर थायरॉयड कार्सिनोमा
इन ट्यूमरों के चारों ओर एक कैप्सूल होता है, लेकिन इनमें रक्त वाहिकाओं का फैलाव दिखाई देता है, जिसका अर्थ है कि ट्यूमर कोशिकाएं रक्त वाहिकाओं के अंदर पाई जाती हैं। रक्त वाहिकाएं राजमार्गों की तरह काम करती हैं, जो ट्यूमर कोशिकाओं को दूर के अंगों तक ले जाती हैं।
रोगविज्ञानी संवहनी आक्रमण को आगे निम्नलिखित भागों में विभाजित करते हैं:
-
सीमित संवहनी आक्रमण: ट्यूमर कोशिकाएं 4 से कम रक्त वाहिकाओं में पाई जाती हैं।
-
व्यापक रक्त वाहिका आक्रमण: ट्यूमर कोशिकाएं 4 या अधिक रक्त वाहिकाओं में पाई जाती हैं।
सीमित रक्त वाहिका आक्रमण वाले ट्यूमर का पूर्वानुमान अच्छा से मध्यम होता है, जबकि व्यापक रक्त वाहिका आक्रमण वाले ट्यूमर में दूरस्थ प्रसार का जोखिम अधिक होता है और इसके लिए अधिक गहन निगरानी की आवश्यकता होती है।
व्यापक रूप से आक्रामक कूपिक थायरॉयड कार्सिनोमा
व्यापक रूप से फैलने वाले ट्यूमर थायरॉइड के आसपास के ऊतकों या निकटवर्ती नरम ऊतकों में व्यापक घुसपैठ दिखाते हैं। इन ट्यूमर में हमेशा पूर्ण कैप्सूल नहीं होता है, जिससे घुसपैठ अधिक स्पष्ट हो जाती है। व्यापक रूप से फैलने वाले ट्यूमर अक्सर कई रक्त वाहिकाओं को प्रभावित करते हैं और इनमें पुनरावृत्ति और दूरस्थ मेटास्टेसिस का जोखिम सबसे अधिक होता है।
लसीकापर्व
लसीकापर्व थायरॉइड छोटी प्रतिरक्षात्मक अंग हैं जो लसीका द्रव को छानती हैं। कैंसर कोशिकाएं थायरॉइड से आसपास की लसीका ग्रंथियों तक लसीका वाहिकाओं के माध्यम से फैल सकती हैं।
फॉलिक्युलर थायरॉइड कार्सिनोमा, पैपिलरी थायरॉइड कार्सिनोमा की तुलना में लिम्फ नोड्स में कम फैलता है, लेकिन फिर भी ऐसा हो सकता है। सर्जरी के दौरान निकाले गए किसी भी लिम्फ नोड की माइक्रोस्कोप से जांच की जाती है और ट्यूमर कोशिकाओं की उपस्थिति या अनुपस्थिति की रिपोर्ट दी जाती है।
लिम्फ नोड्स में ट्यूमर कोशिकाओं की उपस्थिति कैंसर के चरण को बढ़ा सकती है और अतिरिक्त उपचार और अनुवर्ती कार्रवाई के लिए सिफारिशों को प्रभावित कर सकती है।
हाशिये
A हाशिया सर्जरी के दौरान ऊतक का जो किनारा हटाया जाता है, उसे मार्जिन कहते हैं। पैथोलॉजिस्ट यह निर्धारित करने के लिए मार्जिन की जांच करते हैं कि ऊतक के कटे हुए किनारे पर ट्यूमर कोशिकाएं मौजूद हैं या नहीं।
नेगेटिव मार्जिन का मतलब है कि किनारे पर कोई ट्यूमर कोशिकाएं नहीं दिख रही हैं, जिससे पता चलता है कि ट्यूमर पूरी तरह से हटा दिया गया है। पॉजिटिव मार्जिन का मतलब है कि किनारे पर ट्यूमर कोशिकाएं मौजूद हैं, जिससे संकेत मिलता है कि शरीर में कुछ ट्यूमर शेष रह सकता है। मार्जिन की स्थिति आगे के उपचार और निगरानी के बारे में निर्णय लेने में सहायक होती है।
पैथोलॉजिकल स्टेज (पीटीएनएम)
फॉलिक्युलर थायरॉइड कार्सिनोमा का पैथोलॉजिकल स्टेज टीएनएम स्टेजिंग सिस्टम पर आधारित है, जिसमें प्राथमिक ट्यूमर (टी), लिम्फ नोड्स (एन) और दूरस्थ मेटास्टेसिस (एम) को ध्यान में रखा जाता है। सामान्य तौर पर, उच्च स्टेज अधिक उन्नत बीमारी और खराब पूर्वानुमान का संकेत देता है।
ट्यूमर चरण (पीटी)
ट्यूमर की अवस्था का निर्धारण ट्यूमर के आकार और इस बात पर आधारित होता है कि क्या ट्यूमर कोशिकाएं थायरॉइड ग्रंथि से बाहर तक फैली हुई हैं:
-
T1: ट्यूमर ≤ 2 सेमी, थायरॉइड तक सीमित।
-
T2: ट्यूमर > 2 सेमी लेकिन ≤ 4 सेमी, थायरॉइड तक सीमित।
-
T3: ट्यूमर > 4 सेमी या आस-पास की गर्दन की मांसपेशियों में न्यूनतम विस्तार।
-
T4: ट्यूमर श्वासनली, स्वरयंत्र या अन्नप्रणाली जैसी प्रमुख संरचनाओं तक फैल जाता है।
नोडल चरण (पीएन)
-
N0: लिम्फ नोड्स में कोई ट्यूमर कोशिकाएं नहीं पाई गईं।
-
N1: लिम्फ नोड्स में पाए जाने वाले ट्यूमर कोशिकाएं।
-
एनएक्स: जांच के लिए कोई लसीका ग्रंथियां प्रस्तुत नहीं की गईं।
थायरॉइड कैंसर के लिए बायोमार्कर
बायोमार्कर ट्यूमर के ऊतकों पर किए जाने वाले परीक्षण होते हैं, जिनका उद्देश्य जीन या प्रोटीन में होने वाले परिवर्तनों का पता लगाना होता है। ये परिवर्तन कैंसर के विकास और उसके संभावित व्यवहार को समझने में सहायक होते हैं। थायरॉइड कैंसर में, बायोमार्कर परीक्षण का उपयोग निदान में सहायता करने, पुनरावृत्ति के जोखिम का अनुमान लगाने और लक्षित उपचारों से लाभान्वित होने वाले रोगियों की पहचान करने के लिए किया जाता है। हर थायरॉइड कैंसर के लिए बायोमार्कर परीक्षण आवश्यक नहीं होता है, और जिन विशिष्ट जीनों का परीक्षण किया जाता है वे ट्यूमर के प्रकार और नैदानिक स्थिति पर निर्भर करते हैं।
बीआरएफ
BRAF जीन कोशिकाओं को विभाजन का समय बताने वाले संकेत भेजकर सामान्य कोशिका वृद्धि को नियंत्रित करने में मदद करता है। थायरॉइड कैंसर में, BRAF V600E नामक एक विशिष्ट परिवर्तन वृद्धि संकेत को स्थायी रूप से सक्रिय कर देता है, जिससे ट्यूमर कोशिकाएं तब भी बढ़ने और जीवित रहने लगती हैं जब उन्हें नहीं होना चाहिए। यह उत्परिवर्तन सबसे अधिक पैपिलरी थायरॉइड कार्सिनोमा में देखा जाता है और कुछ रोगियों में पुनरावृत्ति के उच्च जोखिम से जुड़ा होता है, विशेष रूप से जब यह अन्य उच्च जोखिम वाले लक्षणों के साथ पाया जाता है। BRAF उत्परिवर्तन वाले ट्यूमर BRAF अवरोधक नामक लक्षित दवाओं के प्रति प्रतिक्रिया कर सकते हैं, कभी-कभी MEK अवरोधकों के साथ मिलाकर, विशेष रूप से उन्नत या रेडियोधर्मी आयोडीन-प्रतिरोधी रोग में।
आरएएस (एनआरएएस, एचआरएएस, केआरएएस)
RAS जीन परिवार सामान्य थायरॉइड कोशिकाओं के भीतर वृद्धि संकेतों को प्रसारित करने में महत्वपूर्ण भूमिका निभाता है। जब किसी RAS जीन में उत्परिवर्तन होता है, तो इसके द्वारा एन्कोड किए गए संकेत अतिसक्रिय हो जाते हैं, जिससे कोशिका वृद्धि और जीवित रहने को बढ़ावा मिलता है। RAS उत्परिवर्तन फॉलिक्युलर पैटर्न वाले थायरॉइड ट्यूमर में आम हैं, जिनमें फॉलिक्युलर थायरॉइड कार्सिनोमा, ऑन्कोसाइटिक कार्सिनोमा और NIFTP शामिल हैं। हालांकि RAS उत्परिवर्तन कैंसर के लिए विशिष्ट नहीं हैं और सौम्य ट्यूमर में भी देखे जा सकते हैं, इनकी उपस्थिति ट्यूमर के विकास को समझने में सहायक होती है और ट्यूमर की निगरानी की बारीकी से जांच को प्रभावित कर सकती है। वर्तमान में, थायरॉइड कैंसर के लिए कोई मानक RAS-लक्षित उपचार उपलब्ध नहीं हैं, लेकिन ये ट्यूमर कुछ प्रणालीगत उपचारों के प्रति अलग-अलग प्रतिक्रिया दे सकते हैं।
TERT प्रमोटर
TERT प्रमोटर टेलोमेरेज़ गतिविधि को नियंत्रित करता है, जो एक प्रोटीन है जो कोशिकाओं को बार-बार विभाजन के दौरान अपने गुणसूत्रों को बनाए रखने में मदद करता है। सामान्य कोशिकाओं में, टेलोमेरेज़ गतिविधि को सख्ती से नियंत्रित किया जाता है, लेकिन TERT प्रमोटर में उत्परिवर्तन ट्यूमर कोशिकाओं को अनिश्चित काल तक विभाजित होने की अनुमति देते हैं। थायरॉइड कैंसर में, TERT प्रमोटर उत्परिवर्तन अधिक आक्रामक व्यवहार, पुनरावृत्ति के उच्च जोखिम और खराब पूर्वानुमान से जुड़े होते हैं, विशेष रूप से जब BRAF या RAS उत्परिवर्तन के साथ संयुक्त होते हैं। हालांकि TERT को लक्षित करने वाली कोई विशिष्ट चिकित्सा नहीं है, इस उत्परिवर्तन की उपस्थिति अक्सर उपचार की तीव्रता और अनुवर्ती योजना को प्रभावित करती है।
रेत
आरईटी जीन एक रिसेप्टर उत्पन्न करता है जो कोशिका वृद्धि और विकास में शामिल होता है। थायरॉइड कैंसर में, आरईटी दो अलग-अलग तरीकों से कैंसर में योगदान कर सकता है: जीन पुनर्व्यवस्था (जो अक्सर पैपिलरी थायरॉइड कार्सिनोमा में होता है) या बिंदु उत्परिवर्तन (जो मेडुलरी थायरॉइड कार्सिनोमा की विशेषता है)। ये परिवर्तन निरंतर वृद्धि संकेत उत्पन्न करते हैं। आरईटी में परिवर्तन महत्वपूर्ण हैं क्योंकि अत्यधिक प्रभावी आरईटी-लक्षित उपचार उपलब्ध हैं और इनका उपयोग उन्नत या मेटास्टैटिक रोग में किया जा सकता है, अक्सर पारंपरिक कीमोथेरेपी की तुलना में कम दुष्प्रभावों के साथ।
एनटीआरके (एनटीआरके1, एनटीआरके3)
एनटीआरके जीन सामान्यतः तंत्रिका कोशिकाओं के विकास और संचार में सहायता करते हैं। कुछ थायरॉइड कैंसर में, एनटीआरके जीन असामान्य रूप से अन्य जीनों के साथ जुड़ जाते हैं, जिससे एक ऐसा प्रोटीन बनता है जो लगातार ट्यूमर के विकास को बढ़ावा देता है। हालांकि यह दुर्लभ है, लेकिन एनटीआरके संलयन की पहचान करना अत्यंत महत्वपूर्ण है क्योंकि इस परिवर्तन वाले ट्यूमर अक्सर टीआरके अवरोधक उपचारों के प्रति नाटकीय रूप से प्रतिक्रिया करते हैं, जो उन्नत अवस्था में भी अत्यधिक प्रभावी होते हैं।
पीपीएआरजी (PAX8::PPARG पुनर्व्यवस्था)
PPARG जीन कोशिका चयापचय और विभेदन को नियंत्रित करता है। कुछ फॉलिक्युलर थायरॉइड कार्सिनोमा में, PPARG असामान्य रूप से एक अन्य जीन, PAX8 के साथ जुड़ जाता है, जिससे एक ऐसा संलयन बनता है जो सामान्य वृद्धि नियंत्रण को बाधित करता है। इस पुनर्व्यवस्था वाले ट्यूमर अक्सर अच्छी तरह से विभेदित होते हैं और कम आक्रामक व्यवहार कर सकते हैं, हालांकि अपवाद भी मौजूद हैं। वर्तमान में PPARG पुनर्व्यवस्था के लिए कोई मानक लक्षित उपचार उपलब्ध नहीं हैं, लेकिन यह परिणाम ट्यूमर के प्रकार और अपेक्षित व्यवहार को स्पष्ट करने में सहायक है।
PIK3CA और AKT1
PIK3CA और AKT1 जीन एक ऐसे मार्ग का हिस्सा हैं जो कोशिका वृद्धि, चयापचय और जीवन रक्षा को नियंत्रित करता है। इन जीनों में उत्परिवर्तन ट्यूमर कोशिकाओं को सामान्य वृद्धि नियंत्रणों के प्रति अधिक प्रतिरोधी बना सकते हैं। थायरॉइड कैंसर में, ये उत्परिवर्तन अक्सर उन्नत, कम विभेदित या उच्च श्रेणी के ट्यूमर में देखे जाते हैं। इनकी उपस्थिति उच्च जोखिम वाले कैंसर का संकेत दे सकती है और कुछ मामलों में, PI3K/AKT/mTOR मार्ग को प्रभावित करने वाली लक्षित चिकित्साओं के लिए पात्रता का संकेत दे सकती है, जो आमतौर पर नैदानिक परीक्षणों या उन्नत अवस्थाओं में की जाती हैं।
TP53
टीपी53 जीन को अक्सर "जीनोम का रक्षक" कहा जाता है क्योंकि यह क्षतिग्रस्त कोशिकाओं को विभाजित होने से रोकने में मदद करता है। टीपी53 में उत्परिवर्तन होने पर, यह सुरक्षात्मक तंत्र निष्क्रिय हो जाता है, जिससे आनुवंशिक क्षति वाली कोशिकाएं जीवित रह सकती हैं और गुणा कर सकती हैं। टीपी53 उत्परिवर्तन अच्छी तरह से विभेदित थायरॉइड कैंसर में असामान्य हैं, लेकिन खराब रूप से विभेदित और एनाप्लास्टिक थायरॉइड कार्सिनोमा में अक्सर देखे जाते हैं। टीपी53 उत्परिवर्तन की पहचान होने पर, यह अधिक आक्रामक ट्यूमर का संकेत देता है और उपचार संबंधी निर्णयों और रोग का पूर्वानुमान प्रभावित कर सकता है, हालांकि वर्तमान में टीपी53 को लक्षित करने वाली कोई प्रत्यक्ष चिकित्सा उपलब्ध नहीं है।
सीटीएनएनबी1 (बीटा-कैटेनिन)
CTNNB1 जीन β-कैटेनिन नामक प्रोटीन का उत्पादन करता है, जो कोशिका आसंजन और वृद्धि संकेतन में शामिल होता है। इस मार्ग की असामान्य सक्रियता अनियंत्रित कोशिका वृद्धि का कारण बन सकती है। सामान्य रूप से विभेदित थायरॉइड कैंसर में CTNNB1 उत्परिवर्तन दुर्लभ होते हैं, लेकिन उच्च श्रेणी या कम विभेदित ट्यूमर में अधिक पाए जाते हैं। इनकी उपस्थिति आक्रामक रोग के निदान का समर्थन करती है और मानक उपचारों के प्रति प्रतिरोध को समझाने में सहायक होती है।
ALK
ALK जीन सामान्यतः प्रारंभिक कोशिका विकास में भूमिका निभाता है। दुर्लभ थायरॉइड कैंसर में, ALK असामान्य रूप से किसी अन्य जीन के साथ जुड़ जाता है, जिससे निरंतर वृद्धि संकेत मिलते रहते हैं। हालांकि यह असामान्य है, फिर भी ALK पुनर्व्यवस्था की पहचान करना महत्वपूर्ण है क्योंकि ALK-लक्षित उपचार उन्नत अवस्था वाले रोगियों में प्रभावी हो सकते हैं।
रोग का निदान
फॉलिक्युलर थायरॉइड कार्सिनोमा का पूर्वानुमान मुख्य रूप से आक्रमण की सीमा पर निर्भर करता है। कम आक्रमण वाले ट्यूमर का परिणाम उत्कृष्ट होता है। सीमित रक्त वाहिका आक्रमण वाले ट्यूमर में जोखिम थोड़ा अधिक होता है, लेकिन उचित उपचार से उनमें भी अच्छे परिणाम मिलते हैं। व्यापक रूप से आक्रमण करने वाले ट्यूमर और व्यापक रक्त वाहिका आक्रमण वाले ट्यूमर में पुनरावृत्ति और दूरस्थ प्रसार का जोखिम अधिक होता है।
दूरस्थ मेटास्टेसिस की उपस्थिति और कुछ आणविक परिवर्तन, जैसे कि टीआरईटी प्रमोटर उत्परिवर्तन, खराब परिणामों से जुड़े होते हैं।
अपने डॉक्टर से पूछने के लिए प्रश्न
-
मुझे फॉलिक्युलर थायरॉइड कार्सिनोमा का कौन सा उपप्रकार है?
-
क्या कैप्सूल या रक्त वाहिका में आक्रमण मौजूद था?
-
रक्त वाहिकाओं में संक्रमण कितना व्यापक था?
-
क्या कोई लिम्फ नोड्स शामिल थे?
-
क्या मुझे रेडियोधर्मी आयोडीन थेरेपी की आवश्यकता होगी?
-
मुझे इस बीमारी के दोबारा होने का दीर्घकालिक जोखिम कितना है?
-
मुझे कितनी बार अनुवर्ती परीक्षण या इमेजिंग की आवश्यकता होगी?


