بواسطة جايسون واسرمان دكتوراه في الطب دكتوراه FRCPC
17 يونيو، 2025
سرطان الغدة الحرشفية هو نوع من سرطان الرئة يحتوي على نوعين مختلفين من الخلايا السرطانية: الخلايا الغدية و الخلايا الحرشفيةتنتج الخلايا الغدية عادةً مخاطًا ومواد أخرى تساعد في الحفاظ على رطوبة المجاري الهوائية، بينما تبطن الخلايا الحرشفية عادةً السطح الداخلي للمجاري الهوائية. ونتيجةً لهذا المزيج، يُظهر سرطان الغدد الحرشفية سمات نوعين آخرين من سرطان الرئة: غدية (مشتقة من الخلايا الغدية) و سرطان الخلايا الحرشفية (مشتق من الخلايا الحرشفية). يُعرف هذا الورم بسلوكه العدواني واحتمالية انتشاره العالية.
ما هي أعراض سرطان الغدة الحرشفية في الرئة؟
تشمل الأعراض الشائعة ما يلي:
-
سعال مستمر يزداد سوءًا مع مرور الوقت.
-
سعال الدم.
-
ضيق في التنفس.
-
ألم في الصدر.
إذا انتشر الورم إلى أجزاء أخرى من الجسم، فقد تظهر أعراض إضافية حسب موقع الورم. على سبيل المثال، إذا انتشر الورم إلى العظام، فقد يُسبب ألمًا في العظام أو يُضعفها، مما يزيد من خطر الكسر (يُسمى كسرًا مرضيًا).
ما الذي يسبب سرطان الغدة الحرشفية في الرئة؟
الأسباب الدقيقة لسرطان الغدة الحرشفية في الرئة غير مفهومة تمامًا، ولكن هناك العديد من عوامل الخطر المعروفة التي تزيد من احتمالية الإصابة بهذا السرطان:
-
تدخين التبغ: وهذا هو السبب الأكثر شيوعا لجميع أنواع سرطان الرئة.
-
التعرض للرادون: غاز مشع موجود في بعض المنازل.
-
التعرض للأسبستوس: غالبًا ما ترتبط بمهن مثل البناء أو التعدين أو بناء السفن.
-
المواد الضارة الأخرى: المواد الكيميائية والملوثات الصناعية.
-
عوامل وراثية: قد يزيد التاريخ العائلي والحالات الوراثية أيضًا من خطر الإصابة.
كيف يتم هذا التشخيص؟
يبدأ تشخيص سرطان الغدد الحرشفية عادةً بفحوصات التصوير، مثل تصوير الصدر بالأشعة السينية أو التصوير المقطعي المحوسب، يليه استئصال عينة صغيرة من أنسجة الرئة عبر خزعة أو شفط بالإبرة الدقيقة (FNA). يُفحص عينة الأنسجة تحت المجهر بواسطة أخصائي علم الأمراض (وهو طبيب متخصص في تشخيص الأمراض من خلال فحص عينات الأنسجة).
إذا أكدت الخزعة أن الورم سرطان غدي حرشفي، فقد تُجرى جراحة لإزالة الورم بأكمله. يعتمد نوع الجراحة على حجم الورم وموقعه في الرئة.
-
إسفين بتر: إزالة الأورام الصغيرة بالقرب من الحافة الخارجية للرئة.
-
استئصال الفص: إزالة فص من الرئة في حالة وجود أورام أكبر حجمًا.
-
استئصال الرئة: إزالة الرئة بأكملها في حالة وجود أورام قريبة من المركز أو أورام كبيرة.
كيف يبدو سرطان الغدة الحرشفية تحت المجهر؟
تحت المجهر، يحتوي سرطان الغدة الحرشفية على مزيج من نوعين مختلفين من خلايا السرطان:
-
الخلايا الغدية: غالبًا ما تُرتَّب في هياكل غدية (تشبه الغدد) أو في مجموعات صلبة. تُبطِّن هذه الخلايا أحيانًا الحويصلات الهوائية (الأكياس الهوائية) بنمط يُسمَّى "الليبيدي".
-
الخلايا الحرشفية: عادة ما تشكل مجموعات كبيرة، ويمكن وصفها على النحو التالي:
-
الكيراتين: عندما تنتج الخلايا كمية كبيرة من الكيراتين (بروتين يجعل الخلايا تبدو باللون الوردي تحت المجهر).
-
غير الكيراتين: عندما لا تنتج الخلايا الكثير من الكيراتين (مما يجعلها تبدو أكثر زرقة تحت المجهر).
-
ما الاختبارات الإضافية التي يمكن إجراؤها لتأكيد التشخيص؟
قد يستخدم أخصائي علم الأمراض اختبارات خاصة تسمى الكيمياء المناعية (IHC) للمساعدة في تأكيد التشخيص وتمييز سرطان الغدة الحرشفية عن أنواع سرطان الرئة الأخرى. تساعد الكيمياء المناعية على تحديد بروتينات محددة تنتجها الخلايا السرطانية. بالنسبة لسرطان الغدة الحرشفية، تشمل النتائج النموذجية ما يلي:
-
تي تي إف-1: إيجابي في الخلايا الغدية.
-
p40 و CK5: إيجابية في الخلايا الحرشفية.
-
الكروموجرانين والسينابتوفيزين: عادة ما تكون سلبية في كل من الخلايا الغدية والحرشفية.
الانتشار عبر المجالات الجوية (STAS)
يصف انتشار الخلايا السرطانية عبر الفراغات الهوائية (STAS) نمطًا من نمو سرطان الرئة، حيث تنتشر الخلايا السرطانية في الفراغات الهوائية المجاورة داخل الرئة. غالبًا ما يعني وجود انتشار الخلايا السرطانية عبر الفراغات الهوائية ارتفاع خطر عودة السرطان (الانتكاس)، ويشير عمومًا إلى تشخيص أسوأ، خاصةً في الأورام في مراحلها المبكرة.
يقوم أخصائيو علم الأمراض بفحص أنسجة الرئة المحيطة بالورم تحت المجهر لتحديد ما إذا كانت الخلايا السرطانية تطفو بحرية أو متصلة بشكل منفصل بجدران الحويصلات الهوائية، بعيدًا عن كتلة الورم الرئيسية.
أورام متعددة في الرئة
من الممكن وجود أكثر من ورم في الرئة. عند اكتشاف أورام متعددة، سيصف تقريرك المرضي كل ورم على حدة.
هناك سببان لظهور الأورام المتعددة:
-
انتشار من ورم واحد: من المرجح أن تكون جميع الأورام من نفس النوع (مثل أن تكون جميعها سرطانات غدية حرشفية). تُسمى الأورام الأصغر عُقيدات إذا وُجدت على نفس جانب الرئة، وتُسمى نقائل إذا وُجدت على الرئة المقابلة.
-
الأورام المنفصلة: إذا كانت الأورام من أنواع مختلفة (على سبيل المثال، سرطان غدي حرشفي وسرطان خلايا حرشفية)، فمن المرجح أن تكون قد تطورت بشكل منفصل. تُعتبر هذه الأورام سرطانات أولية منفصلة.
الغزو الجنبي
غشاء الجنب هو غشاء رقيق يحيط بالرئتين وداخل جدار الصدر. عندما تنتشر الخلايا السرطانية إلى غشاء الجنب، يُشار إلى ذلك بالغزو الجنبي. يُعد الغزو الجنبي مهمًا لأنه يعني عادةً:
-
مرحلة الورم العليا: ويعتبر السرطان الذي يغزو غشاء الجنب أكثر تقدما.
-
تشخيص أسوأ: غالبًا ما يؤدي الغزو الجنبي إلى مضاعفات، مثل تراكم السوائل (الانصباب الجنبي)، مما قد يسبب ضيق التنفس وألم الصدر والسعال.
غزو الأوعية الدموية اللمفاوية
الغزو اللمفاوي يعني دخول الخلايا السرطانية إلى الأوعية الدموية أو القنوات اللمفاوية الصغيرة داخل أنسجة الرئة. هذا مهم لأن الخلايا السرطانية في هذه الأوعية قد تنتقل إلى العقد اللمفاوية أو أجزاء بعيدة من الجسم، مما يؤدي إلى مزيد من النقائل (الانتشار).

هوامش
في علم الأمراض، يُشير مصطلح "الهامش" إلى حافة الأنسجة المُزالة أثناء الجراحة لإزالة الورم. بعد جراحة الرئة، يفحص أخصائيو علم الأمراض جميع حواف هذه الأنسجة بعناية تحت المجهر لتحديد ما إذا كان الورم قد أُزيل بالكامل.
تشمل الهوامش التي يتم تقييمها في جراحات سرطان الرئة عادةً ما يلي:
-
الحافة القصبية - وهنا يقوم الجراح بقطع مجرى الهواء.
-
الهامش الوعائي - هذه هي المناطق التي يتم فيها قطع الأوعية الدموية الكبيرة بالقرب من الورم.
-
الهامش الحشوي - تشمل هذه الحافة حافة أنسجة الرئة المحيطة بالورم.
-
الحافة الجنبية - الغشاء الجنبي هو عبارة عن بطانة رقيقة تحيط بالرئة، ويتم فحص هذه الحافة لتحديد ما إذا كان الورم ينمو بالقرب من هذه البطانة أو من خلالها.
يمكن وصف الهوامش بطريقتين:
-
هامش سلبي لا تظهر أي خلايا سرطانية عند أي حافة قطع. هذا يشير إلى احتمال استئصال الورم بالكامل، وهو هدف الجراحة.
-
هامش إيجابي تظهر الخلايا السرطانية عند حافة النسيج المقطوع. يشير وجود هامش إيجابي إلى احتمال وجود خلايا ورمية متبقية في الجسم. قد يحتاج المرضى ذوو الهامش الإيجابي إلى علاجات إضافية، مثل جراحة ثانية أو علاج إشعاعي، لإزالة أي خلايا ورمية متبقية وتقليل خطر تكرار المرض.
تساعد حالة الهوامش طبيبك على تحديد الحاجة إلى علاج إضافي وتلعب دورًا مهمًا في التنبؤ باحتمالية نمو الورم مرة أخرى.

العقد الليمفاوية
العقد الليمفاوية هي أعضاء صغيرة تشبه حبة الفاصولياء، وتلعب دورًا أساسيًا في الجهاز المناعي. تتصل هذه الأعضاء في جميع أنحاء الجسم بقنوات صغيرة تُسمى الأوعية اللمفاوية. يمكن أن تنتشر الخلايا السرطانية من الورم عبر هذه الأوعية اللمفاوية إلى العقد اللمفاوية المجاورة، وهي عملية تُسمى نقائل العقد اللمفاوية.
تُصنَّف الغدد الليمفاوية في الرئتين والصدر في مناطق محددة، تُعرف باسم محطات الغدد الليمفاوية. هناك 14 محطة مختلفة للعقد الليمفاوية، لكل منها موقع محدد:
-
المحطة 1: الغدد الليمفاوية العنقية السفلية، وفوق الترقوة، والقصية.
-
المحطة 2: الغدد الليمفاوية في القصبة الهوائية العلوية.
-
المحطة 3: العقد الليمفاوية قبل الأوعية الدموية وخلف القصبة الهوائية.
-
المحطة 4: الغدد الليمفاوية المحيطة بالقصبة الهوائية السفلية.
-
المحطة 5: العقد الليمفاوية تحت الأبهر (نافذة الأبهر الرئوي).
-
المحطة 6: العقد الليمفاوية المجاورة للأبهر (بالقرب من الأبهر الصاعد أو العصب الحجابي).
-
المحطة 7: العقد الليمفاوية تحت القصبة الهوائية (تحت القصبة الهوائية، حيث ينقسم القصبة الهوائية إلى شعب هوائية).
-
المحطة 8: العقد الليمفاوية المحيطة بالمريء (بجانب المريء أسفل الجفن).
-
المحطة 9: العقد الليمفاوية في الرباط الرئوي.
-
المحطة 10: العقد الليمفاوية الهيلارية (في هيلوم الرئة، حيث تدخل الممرات الهوائية إلى الرئة).
-
المحطة 11: العقد الليمفاوية بين فصوص الرئة.
-
المحطة 12: العقد الليمفاوية الفصية (داخل فصوص الرئة).
-
المحطة 13: العقد الليمفاوية القطعية (داخل قطاعات الرئة).
-
المحطة 14: العقد الليمفاوية تحت القطعية (ضمن أجزاء الرئة الأصغر).

إذا أُزيلت العقد الليمفاوية أثناء الجراحة، يقوم أخصائي علم الأمراض بفحصها بعناية تحت المجهر للتحقق من احتوائها على خلايا سرطانية. يتضمن تقرير علم الأمراض عادةً ما يلي:
-
العدد الإجمالي للغدد الليمفاوية التي تم فحصها.
-
مواقع (محطات) الغدد الليمفاوية التي تم فحصها.
-
عدد الغدد الليمفاوية التي تحتوي على خلايا سرطانية.
-
حجم أكبر مجموعة من الخلايا السرطانية (غالبًا ما يطلق عليها "البؤرة" أو "الرواسب").
يوفر فحص العقد الليمفاوية معلومات مهمة تساعد طبيبك على تحديد المرحلة المرضية للسرطان (pN). كما يساعد على التنبؤ باحتمالية انتشار الخلايا السرطانية إلى أجزاء أخرى من الجسم، مما يُرشدك في اتخاذ القرارات بشأن العلاجات الإضافية مثل العلاج الكيميائي، والعلاج الإشعاعي، والعلاج المناعي.
المؤشرات الحيوية لسرطان الغدة الحرشفية في الرئة
المؤشرات الحيوية هي جزيئات محددة موجودة داخل خلايا الورم. تساعد هذه الجزيئات الأطباء على فهم سلوك الورم وكيفية استجابته للعلاجات المختلفة. يُعدّ اختبار المؤشرات الحيوية أمرًا بالغ الأهمية في سرطان الرئة، لأن بعض الأورام تحتوي على تغيرات أو تغييرات جينية تجعلها تستجيب بشكل جيد للعلاجات الموجهة. العلاجات الموجهة هي أدوية مصممة خصيصًا لمهاجمة الخلايا السرطانية التي تحتوي على هذه التغيرات الجينية. يساعد تحديد هذه المؤشرات الحيوية الأطباء على اختيار خيارات العلاج الأكثر فعالية.
يبحث علماء الأمراض عن المؤشرات الحيوية باستخدام اختبارات معملية متخصصة.
هناك اختباران شائعان:
-
تسلسل الجيل التالي (NGS) يفحص هذا الاختبار عدة جينات في آنٍ واحد لاكتشاف الطفرات (التغيرات في المادة الوراثية لخلايا الورم). ويمكن لتقنية الجيل التالي من الجينوم تحديد عدة مؤشرات حيوية بسرعة من عينة نسيجية واحدة.
-
الكيمياء الهيستولوجية المناعية (IHC) يستخدم هذا الاختبار أصباغًا خاصة تلتصق ببروتينات محددة تنتجها الخلايا السرطانية. عند وجود هذه البروتينات، يتغير لون خلايا الورم تحت المجهر. يساعد اختبار IHC على تأكيد وجود بعض المؤشرات الحيوية في الورم.
المؤشرات الحيوية الشائعة التي تم اختبارها في سرطان الغدة الحرشفية في الرئة
قد يتضمن تقريرك المرضي معلومات حول المؤشرات الحيوية التالية. يمكن لكل مؤشر حيوي أن يساعد في توجيه علاجك ويوفر معلومات مهمة حول ورمك.
-
عامل نمو البشرة: الطفرات (التغيرات) في جين عامل نمو البشرة (EGFR) شائعة في سرطان الرئة، وخاصةً لدى غير المدخنين، والنساء، والمنحدرين من أصول شرق آسيوية. غالبًا ما تستجيب الأورام التي تحتوي على طفرات في جين عامل نمو البشرة (EGFR) بشكل جيد للعلاجات الموجهة التي تُسمى مثبطات عامل نمو البشرة (EGFR). سيصف تقريرك الورم بأنه إيجابي لعامل نمو البشرة (EGFR) في حال وجود طفرة. أما في حال عدم وجود طفرة، فسيتم اعتباره سلبيًا لعامل نمو البشرة (EGFR).
-
ألك: تؤدي التغيرات في جين ALK، المعروفة باسم إعادة ترتيب أو اندماج جين ALK، إلى نمو الورم، وغالبًا ما تُلاحظ لدى المرضى الأصغر سنًا أو غير المدخنين. عادةً ما تستجيب الأورام التي تُعاني من إعادة ترتيب جين ALK بشكل جيد للأدوية التي تُسمى مثبطات ALK. سيشير تقريرك إلى أن ورمك إيجابي لـ ALK إذا كان هذا التغيير موجودًا. إذا لم يكن موجودًا، فسيكون ورمك سلبيًا لـ ALK.
-
ROS1: تُسبب إعادة ترتيب (اندماج) ROS1 نمو الخلايا السرطانية بسرعة. عادةً ما تستجيب الأورام الإيجابية لـ ROS1 بشكل جيد للعلاجات المُثبطة لـ ROS1 المُستهدفة. إذا كان الورم مُصابًا بإعادة ترتيب ROS1، فسيتم وصفه بأنه إيجابي لـ ROS1. إذا لم يتم العثور على أي إعادة ترتيب، فسيتم وصفه بأنه سلبي لـ ROS1.
-
براف: يمكن أن تُسبب بعض الطفرات في جين BRAF نموًا سريعًا للخلايا السرطانية. يمكن علاج الأورام التي تحتوي على طفرات BRAF محددة، وخاصةً طفرة V600E، بمثبطات BRAF. في حال وجود طفرة BRAF، يُوصف الورم بأنه إيجابي لـ BRAF. أما في حال عدم وجود طفرة، فيُوصف بأنه سلبي لـ BRAF.
-
التقى: تُسبب الطفرات في جين MET، وخاصةً الطفرات التي تُؤدي إلى "تخطي إكسون MET 14"، زيادةً في نمو الورم. غالبًا ما تستجيب الأورام الإيجابية لـ MET للعلاجات المُستهدفة المعروفة باسم مُثبطات MET. سيُصف تقريرك المرضي الورم بأنه إيجابي لـ MET في حال وجود هذه الطفرة. إذا لم يتم العثور على أي طفرة، فسيكون الورم سلبيًا لـ MET.
-
ريت: تؤدي إعادة ترتيب أو اندماجات RET إلى نمو ورمي غير منضبط. عادةً ما تستجيب الأورام التي تعاني من اندماجات RET بشكل جيد جدًا لمثبطات RET. سيُشير تقريرك إلى أن ورمك إيجابي لـ RET في حال وجود اندماج. إذا لم يُعثر على اندماج، فسيتم وصفه بأنه سلبي لـ RET.
-
NTRK1-3: اندماج جينات NTRK نادر، ولكنه قد يُعزز نمو الورم بشدة. عادةً ما تستجيب الأورام المُصابة باندماجات NTRK للأدوية المُستهدفة المعروفة باسم مُثبطات TRK. في حال اكتشاف اندماج NTRK، يُوصف الورم بأنه إيجابي لـ NTRK. وإلا، فيُوصف بأنه سلبي لـ NTRK.
-
كراس: طفرات KRAS شائعة في سرطانات الرئة، وخاصةً بين المدخنين. تاريخيًا، كان علاج الأورام الإيجابية لـ KRAS صعبًا، لكن الأدوية الحديثة التي تستهدف طفرة KRAS محددة (KRAS G12C) أظهرت نتائج واعدة. في حال وجود طفرة KRAS، يُوصف الورم بأنه إيجابي لـ KRAS. أما إذا لم تُكتشف أي طفرة، فيُوصف الورم بأنه سلبي لـ KRAS.
-
ERBB2 (HER2): يمكن لطفرات ERBB2 (المعروفة أيضًا بطفرات HER2) أن تُحفّز نمو الورم، خاصةً لدى غير المدخنين. قد تستجيب الأورام التي تحتوي على طفرات HER2 للعلاجات المُوجّهة التي لا تزال قيد البحث أو المُتاحة في المراكز المُتخصصة. إذا كان الورم يحتوي على طفرة ERBB2، فسيتم وصفه بأنه إيجابي لـ ERBB2. إذا لم يتم العثور على أي طفرة، فسيكون سلبيًا لـ ERBB2.
-
هيئة تنظيم الاتصالات الوطنية: تحدث الطفرات في جين NRAS بشكل شائع في أورام المدخنين. حاليًا، العلاجات الموجهة لطفرات NRAS محدودة؛ ومع ذلك، فإن تحديد هذه الطفرة لا يزال يساعد في فهم سلوك الورم. سيُوصف الورم بأنه إيجابي لـ NRAS إذا وُجدت طفرة، أو سلبي لـ NRAS إذا لم تكن هناك طفرة.
-
MAP2K1 (MEK1): طفرات MAP2K1 أكثر شيوعًا بين المدخنين، وترتبط بزيادة نمو الورم. حاليًا، لا تزال العلاجات التي تستهدف طفرات MAP2K1 قيد الدراسة. سيوضح تقريرك المرضي ما إذا كانت طفرة MAP2K1 موجودة (موجبة لـ MAP2K1) أم لا (سالبة لـ MAP2K1).
-
NRG1: تُعد إعادة ترتيب جين NRG1 نادرة، لكنها مهمة، إذ يُمكن أن تُعزز نمو الورم بسرعة. ويُجري الباحثون أبحاثًا مُكثّفة على علاجات مُستهدفة للأورام المُصابة بإعادة ترتيب جين NRG1. سيُوصف ورمك بأنه إيجابي لـ NRG1 إذا وُجدت هذه إعادة الترتيب. وإذا لم تُوجد، فسيكون سلبيًا لـ NRG1.
لماذا تعتبر اختبارات المؤشرات الحيوية مهمة للعلاج؟
يُعدّ تحديد هذه المؤشرات الحيوية في ورمك أمرًا بالغ الأهمية، إذ يُساعد الأطباء على اختيار العلاجات الأكثر فعالية. بعض هذه المؤشرات الحيوية تتوافق مع أدوية مُحددة تستهدف خلايا الورم مباشرةً. غالبًا ما تكون هذه العلاجات أكثر فعالية، ولها آثار جانبية أقل من العلاج الكيميائي التقليدي.
إذا لم يحمل ورمك أي مؤشرات حيوية تتوافق مع العلاجات المُستهدفة المتاحة، فقد يوصي طبيبك بخيارات أخرى، مثل العلاج الكيميائي أو العلاج المناعي. سيساعدك فريقك الطبي على فهم نتائج فحوصاتك وأفضل خيارات العلاج المتاحة لك.
التدريج المرضي (pTNM)
يصف التصنيف المرضي مدى انتشار السرطان بناءً على نظام TNM. يوفر هذا النظام معلومات مهمة حول التشخيص وقرارات العلاج.
مرحلة الورم (pT)
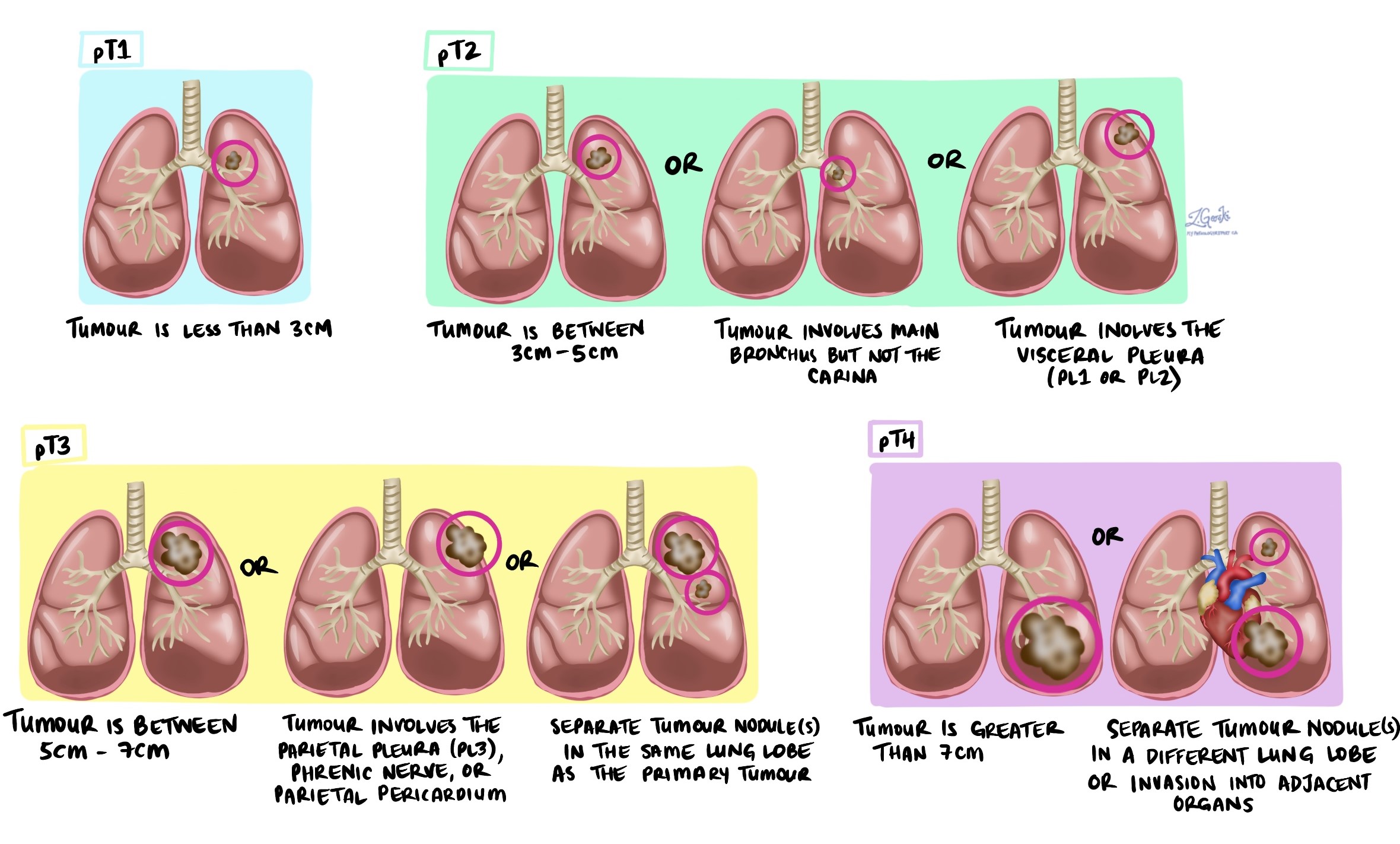
تصف المرحلة المرضية للورم حجم ومدى الورم الرئوي الأولي. تتراوح هذه المرحلة بين ١ و٤، وتساعد في تحديد التشخيص وأفضل نهج علاجي.
-
T1: الورم لا يزيد حجمه عن 3 سنتيمترات ويقتصر على الرئة فقط دون التأثير على الهياكل المجاورة.
-
T2: الورم أكبر من 3 سنتيمترات ولكن ليس أكبر من 5 سنتيمترات، أو يغزو الجنب الحشوي (غطاء الرئة)، أو يسد مجرى الهواء جزئيًا (القصبات الهوائية)، ولكنه ليس قريبًا من غشاء الرئة.
-
T3: الورم أكبر من 5 سنتيمترات ولكن ليس أكبر من 7 سنتيمترات، أو أنه غزا مباشرة الهياكل القريبة مثل جدار الصدر، أو التامور (غطاء القلب)، أو الحجاب الحاجز، أو يحتوي على عقيدات ورمية منفصلة داخل نفس الفص الرئوي.
-
T4: يكون الورم أكبر من 7 سنتيمترات، أو يكون قد غزا هياكل حيوية مثل القلب والأوعية الدموية الرئيسية والقصبة الهوائية والمريء والعمود الفقري، أو يكون لديه عقيدات ورمية منفصلة في فص مختلف من نفس الرئة.
المرحلة العقدية (pN)
تعتمد المرحلة المرضية للعقد الليمفاوية على عدد العقد الليمفاوية التي تحتوي على خلايا سرطانية وموقع العقد الليمفاوية المصابة.
-
NX: لم يتم تقديم أي عقدة ليمفاوية.
-
N0: لا يوجد خلايا سرطانية في الغدد الليمفاوية.
-
N1: الخلايا السرطانية في العقد الليمفاوية القريبة من الورم (المحطات 10-14).
-
N2: الخلايا السرطانية في الغدد الليمفاوية في منتصف الصدر (المحطات 7-9).
-
N3: الخلايا السرطانية في العقد الليمفاوية البعيدة عن الورم أو على الجانب المقابل للصدر (المحطات 1-6).
تأثير العلاج
إذا خضعتَ للعلاج الكيميائي أو الإشعاعي قبل الجراحة، فإن تأثير العلاج يصف مدى استجابة الورم. يقيس أخصائيو علم الأمراض كمية أنسجة الورم الحية المتبقية بعد العلاج، معبرًا عنها كنسبة مئوية. تشير النسبة المنخفضة للأورام الحية إلى استجابة أفضل للعلاج.
تشخيص سرطان الغدة الحرشفية في الرئة
غالبًا ما يكون تشخيص سرطان الغدد الحرشفية أضعف مقارنةً بسرطانات الرئة الأخرى نظرًا لطبيعته العدوانية وميله للانتشار مبكرًا. ومع ذلك، يعتمد التشخيص بشكل كبير على مرحلة التشخيص. عادةً ما تكون الأورام في مراحلها المبكرة أفضل من الأورام في مراحلها المتقدمة.
أسئلة لطرح طبيبك
إذا تم تشخيص إصابتك بسرطان الغدة الحرشفية، ففكر في طرح الأسئلة التالية:
-
ما هي مرحلة الورم لدي وماذا تعني؟
-
هل كانت الهوامش الجراحية واضحة (سلبية)؟
-
هل كانت الغدد الليمفاوية متأثرة؟
-
هل سأحتاج إلى علاج إضافي مثل العلاج الكيميائي أو الإشعاعي؟
-
هل يجب أن أقوم بإجراء اختبار جيني لتوجيه العلاج؟
-
ما هي المدة التي يجب أن أقوم بمتابعتها للمراقبة؟
-
هل هناك تجارب سريرية متاحة لحالتي؟