von Catherine Forse MD FRCPC und Jason Wasserman MD PhD FRCPC
Juli 24, 2025
Adenokarzinom der Speiseröhre ist eine Krebsart, die sich aus drüsenbildenden Zellen in einem Bereich von abnormalem Gewebe entwickelt, das intestinale Metaplasie. Normalerweise kommen diese Zellen nicht in der Speiseröhre vor, können aber auftreten, wenn die Speiseröhrenschleimhaut wiederholt der Magensäure ausgesetzt ist.
Dieser Krebs beginnt fast immer im unteren Teil der Speiseröhre, nahe der Stelle, an der sie in den Magen übergeht (der sogenannte ösophagogastrale Übergang). Er kann sich auch in den oberen Teil des Magens ausbreiten. Seltener kann ein Adenokarzinom in der mittleren oder oberen Speiseröhre auftreten, insbesondere in Bereichen, in denen kleine Flecken Drüsenzellen sind anwesend.
Was sind die Symptome eines Adenokarzinoms der Speiseröhre?
Zu den Symptomen eines Ösophagusadenokarzinoms gehören häufig Schluckbeschwerden (Dysphagie), Sodbrennen oder saurer Reflux, Gewichtsverlust, Brust- oder Bauchschmerzen, Übelkeit oder Erbrechen. In einigen Fällen wird der Krebs bei der Untersuchung einer Anämie oder nach bildgebenden Verfahren entdeckt.
Was verursacht ein Adenokarzinom der Speiseröhre?
Die meisten Fälle von Adenokarzinom der Speiseröhre treten bei Menschen mit einer Erkrankung namens Barrett-Ösophagus. Dieser Zustand wird durch eine langjährige gastroösophageale Refluxkrankheit (GERD) verursacht, bei der Säure und Galle aus dem Magen mit der Zeit die Schleimhaut der Speiseröhre schädigen.
Bei Barrett-Ösophagus ist der normale Plattenepithelzellen die die Speiseröhre auskleiden, werden ersetzt durch Drüsenzellen die denen im Darm ähneln. Diese Art von Veränderung nennt man intestinale Metaplasie.
Mit der Zeit können diese abnormen Drüsenzellen weitere Veränderungen erfahren und sich weiterentwickeln zu Dysplasie, eine präkanzeröse Erkrankung. Unbehandelt kann die Dysplasie schließlich zur Entwicklung eines invasiven Adenokarzinoms führen.
In der Speiseröhre wird Dysplasie in zwei Haupttypen eingeteilt:
-
Niedriggradige Dysplasie: Die Zellen sehen abnormal aus, sind aber noch teilweise organisiert. Bei dieser Art von Dysplasie besteht ein geringeres Risiko, sich zu Krebs zu entwickeln, dennoch wird häufig eine sorgfältige Überwachung oder Behandlung empfohlen.
-
Hochgradige Dysplasie: Die Zellen erscheinen sehr abnormal und unorganisiert. Hochgradige Dysplasie birgt ein deutlich höheres Risiko, sich zu einem Adenokarzinom zu entwickeln, und tritt häufig direkt neben oder sogar innerhalb kleiner Krebsherde auf.
Ihr Pathologiebericht kann eine Dysplasie erwähnen, wenn diese in der Gewebeprobe nachgewiesen wurde. Liegt neben einem Adenokarzinom eine hochgradige Dysplasie vor, deutet dies darauf hin, dass sich der Krebs wahrscheinlich aus einem bereits bestehenden Bereich des Barrett-Ösophagus entwickelt hat. In manchen Fällen, insbesondere bei großen oder tief invasiv wachsenden Tumoren, ist die umgebende Dysplasie jedoch möglicherweise nicht mehr sichtbar.
Weitere Risikofaktoren für diese Krebsart sind Übergewicht, Rauchen, männliches Geschlecht und höheres Alter. Männer sind deutlich häufiger von dieser Krebsart betroffen als Frauen und am häufigsten bei Menschen über 60 Jahren.
Wie wird diese Diagnose gestellt?
Die Diagnose eines Adenokarzinoms der Speiseröhre wird in der Regel nach einer sogenannten oberen Endoskopie (oder Gastroskopie) gestellt. Bei diesem Verfahren untersucht der Arzt mit einer dünnen, flexiblen Kamera das Innere der Speiseröhre und entnimmt kleine Gewebeproben, die Biopsien. Diese Proben werden dann unter dem Mikroskop von einem Pathologe, der nach Krebszellen sucht und die Diagnose bestätigt.
Wenn Krebs festgestellt wird, können zusätzliche Tests wie endoskopischer Ultraschall (EUS), CT-Scan oder PET-Scan durchgeführt werden, um festzustellen, wie weit sich der Tumor ausgebreitet hat, und um die Behandlungsplanung zu erleichtern.
Wie sieht ein Adenokarzinom unter dem Mikroskop aus?
Unter dem Mikroskop besteht ein Adenokarzinom aus abnormen drüsenbildenden Zellen. Pathologen können verschiedene Muster beschreiben, wie z. B. tubuläre, papilläre, muzinöse oder Siegelringzellen. Der häufigste Typ ist tubulärer Zelltyp. Diese Muster stellen keine separaten Subtypen dar, sondern beschreiben die Anordnung der Krebszellen. In manchen Fällen können mehrere Muster im selben Tumor auftreten.
If Barrett-Ösophagus or Dysplasie in der Nähe des Tumors vorhanden ist, kann dies ebenfalls in Ihren Bericht aufgenommen werden.
Tumorgrad
Der Grad beschreibt, wie sehr die Krebszellen unter dem Mikroskop normalen drüsenbildenden Zellen ähneln. Dies wird auch als histologischer Grad bezeichnet. Der Grad gibt Ihrem Arzt wichtige Informationen darüber, wie schnell der Tumor wahrscheinlich wächst und wie wahrscheinlich er sich ausbreitet.
Pathologen unterteilen das Adenokarzinom der Speiseröhre in drei Grade:
Grad 1 – Gut differenziertes Adenokarzinom
Bei dieser Tumorart bilden mehr als 95 % der Krebszellen gut organisierte Drüsen. Diese Tumoren wachsen in der Regel langsamer und breiten sich weniger aus. Dies gilt als der niedrigste Grad und ist mit einer besseren Prognose verbunden.
Grad 2 – Mäßig differenziertes Adenokarzinom
Bei mäßig differenzierten Tumoren bilden zwischen 50 % und 95 % der Krebszellen Drüsen. Diese Tumoren weisen im Vergleich zu Tumoren des ersten Grades eine größere Variation in Aussehen und Verhalten der Zellen auf. Sie neigen zu schnellerem Wachstum und einer höheren Ausbreitungswahrscheinlichkeit als gut differenzierte Tumoren.
Grad 3 – Schlecht differenziertes oder undifferenziertes Adenokarzinom
Diese Tumoren bilden in weniger als 50 % der Fälle Drüsen. In einigen Fällen ist überhaupt keine Drüsenbildung zu beobachten. Die Zellen sehen sehr abnormal aus und verhalten sich aggressiv. Schlecht differenzierte und undifferenzierte Tumoren wachsen schnell und breiten sich eher aus Lymphknoten oder entfernte Körperteile. Diese gelten als hochgradige Tumoren und sind mit einer schlechteren Prognose verbunden.
Was bedeutet Invasion bei einem Adenokarzinom der Speiseröhre?
Invasion Der Begriff „Ösophaguskarzinom“ gibt an, wie tief der Krebs in die Speiseröhrenwand oder das umliegende Gewebe eingedrungen ist. Das Ösophagusadenokarzinom entsteht aus drüsenbildenden Zellen in der Schleimhaut, der innersten Schicht der Speiseröhre. Wächst der Tumor, kann er in tiefere Gewebeschichten eindringen und sich möglicherweise auf benachbarte Organe ausbreiten.
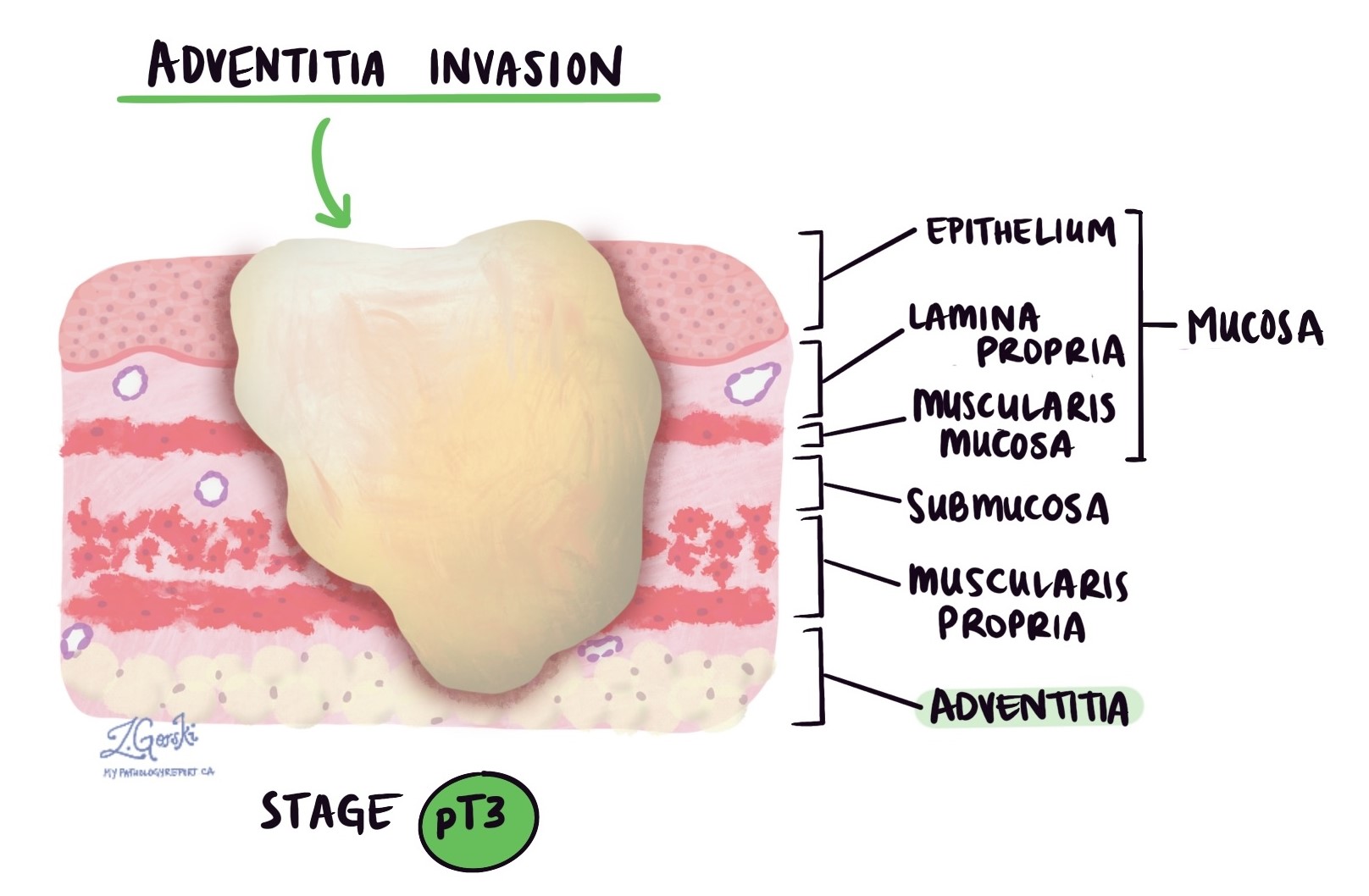
Die Wand der Speiseröhre besteht aus mehreren unterschiedlichen Schichten:
-
Schleimhaut – Die dünne innere Auskleidung, wo der Tumor normalerweise beginnt.
-
Submukosa – Eine Stützschicht direkt unter der Schleimhaut.
-
Muscularis propria – Eine dicke Muskelschicht, die dabei hilft, Nahrung durch die Speiseröhre zu transportieren.
-
Adventitia – Das äußere Bindegewebe, das die Speiseröhre an ihrem Platz verankert. Im Gegensatz zu einigen anderen Teilen des Magen-Darm-Trakts hat die Speiseröhre keine Serosa.
Wenn der Tumor wächst, kann er sich durch diese Schichten ausbreiten. In fortgeschritteneren Fällen kann er in nahegelegene Strukturen wie die Trachea (Luftröhre), die Aorta oder das Perikard (Gewebe um das Herz) eindringen.
Pathologen untersuchen den Tumor sorgfältig unter dem Mikroskop, um den tiefsten Invasionspunkt zu finden, also die Schicht, in die der Tumor am weitesten vorgedrungen ist. Dieser tiefste Punkt ist sehr wichtig, da er das pathologische Tumorstadium, auch pT-Stadium genannt, bestimmt. Dieses ist Teil des TNM-Staging-Systems, das zur Beschreibung der Ausbreitung des Krebses verwendet wird.
Pathologisches Tumorstadium beim Adenokarzinom der Speiseröhre
pT1: Der Krebs befindet sich in einem sehr frühen Stadium und ist nur in die inneren Schichten der Speiseröhre eingewachsen. Zu diesen Schichten gehören die Lamina propria, die Muscularis mucosae oder die Submukosa, die sich direkt unter der Oberflächenauskleidung (Mukosa) befinden.
pT1a: Der Krebs ist sogar noch begrenzter und kommt nur in der Lamina propria oder Muscularis mucosae vor – dünnen Schichten direkt unter der Oberfläche der Speiseröhre.
pT1b: Der Krebs ist tiefer in die Submukosa vorgedrungen, die Bindegewebsschicht direkt unter der Schleimhaut.
pT2: Der Krebs hat die Muscularis propria erreicht, eine dicke Muskelschicht, die dabei hilft, Nahrung durch die Speiseröhre zu befördern.
pT3: Der Krebs ist durch die Muskelschicht gewachsen und hat die Adventitia erreicht, die äußerste Hülle der Speiseröhre.
pT4: Der Krebs hat sich über die Speiseröhrenwand hinaus in nahegelegene Organe oder Strukturen ausgebreitet.
pT4a: Der Krebs breitet sich in benachbarte Bereiche wie Pleura (Lungenfell), Perikard (Herzfell), Vena azygos, Zwerchfell oder Peritoneum (Bauchfell) aus. Diese Tumoren können möglicherweise noch operativ entfernt werden.
pT4b: Der Krebs hat sich auf kritischere nahegelegene Strukturen wie die Aorta (ein großes Blutgefäß), die Wirbelkörper (Knochen der Wirbelsäule) oder die Atemwege ausgebreitet. Diese Tumoren gelten in der Regel als fortgeschrittener und können möglicherweise nicht operativ entfernt werden.
HER2
HER2 (humaner epidermaler Wachstumsfaktor-Rezeptor 2) ist ein Protein, das das Zellwachstum und die Zellteilung fördert. Bei einigen Speiseröhrenkrebsarten ist das HER2-Gen überaktiv und produziert zu viel HER2-Protein. Dies wird als HER2-positiver Krebs bezeichnet.
HER2-positive Speiseröhrenkrebsarten neigen zu schnellerem Wachstum und können aggressiver sein. Zielgerichtete Therapien wie Trastuzumab (Herceptin) können jedoch bei der Behandlung dieser Krebsarten sehr wirksam sein. Die Kenntnis des HER2-Status Ihres Tumors hilft Ihren Ärzten bei der Entscheidung, ob diese zielgerichteten Behandlungen Teil Ihres Behandlungsplans sein sollten.
Wie wird HER2 getestet?
Zur Überprüfung des HER2-Status werden üblicherweise zwei Tests verwendet:
-
Immunhistochemie (IHC) – Misst die Menge des HER2-Proteins auf der Oberfläche von Krebszellen.
-
Fluoreszenz-in-situ-Hybridisierung (FISH) – Misst die Anzahl der HER2-Genkopien in den Krebszellen.
HER2-Immunhistochemie (IHC)
IHC ist ein Labortest, der mithilfe spezieller Farbstoffe das HER2-Protein auf der Oberfläche von Tumorzellen erkennt. Pathologen untersuchen das gefärbte Gewebe unter dem Mikroskop und vergeben einen Wert:
-
0 (negativ) – Kein HER2-Protein vorhanden. Dies gilt als HER2-negativ, und eine gezielte HER2-Therapie ist in der Regel nicht hilfreich.
-
1+ (negativ) – Schwache oder schwache Färbung. Wird auch als HER2-negativ angesehen.
-
2+ (zweideutig oder grenzwertig) – Mäßige Färbung. Das Ergebnis ist unklar und ein zweiter Test (FISH) ist erforderlich.
-
3+ (positiv) – Starke Färbung. Dies ist HER2-positiv, und Patientinnen können von einer HER2-gezielten Therapie profitieren.
HER2-Fluoreszenz-in-situ-Hybridisierung (FISH)
Wenn das IHC-Ergebnis 2+ (unklar oder grenzwertig) ist, kann Ihr Pathologe einen FISH-Test durchführen, um das HER2-Gen in den Tumorzellen genauer zu untersuchen. Dieser Test verwendet spezielle Fluoreszenzmarker, die unter dem Mikroskop leuchten und so die Anzahl der vorhandenen HER2-Genkopien anzeigen.
-
Positiv (verstärkt) – Zu viele HER2-Genkopien. Der Krebs ist HER2-positiv und spricht möglicherweise gut auf eine HER2-gerichtete Therapie an.
-
Negativ (nicht verstärkt) – Eine normale Anzahl von HER2-Genkopien. Dies bedeutet, dass der Krebs HER2-negativ ist und eine HER2-gerichtete Therapie wahrscheinlich nicht hilft.
Manchmal enthält Ihr Bericht zusätzliche Details wie das HER2-zu-Chromosomen-Verhältnis oder die durchschnittliche Anzahl der HER2-Genkopien pro Zelle. Diese Zahlen helfen, den HER2-Status genauer zu bestätigen.
Mismatch-Reparatur-Proteintest (MMR)
MMR Proteine sind Teil des körpereigenen Systems zur Behebung von DNA-Fehlern, die bei der Zellteilung natürlicherweise auftreten. Die vier wichtigsten MMR-Proteine sind MLH1, PMS2, MSH2 und MSH6. Fehlen eines oder mehrere dieser Proteine oder funktionieren sie nicht richtig, können sich DNA-Fehler anhäufen und zu Krebs führen.
Pathologen testen MMR-Proteine mithilfe einer Methode namens Immunhistochemie (IHC). Dieser Test hilft festzustellen, ob das DNA-Reparatursystem in Ihren Krebszellen normal funktioniert.
Was bedeuten die Ergebnisse?
-
Normal (intakt) – Alle vier MMR-Proteine sind vorhanden. Das bedeutet, dass der Tumor MMR-kompetent ist und das DNA-Reparatursystem normal erscheint.
-
Abnorm (Verlust des Ausdrucks) – Ein oder mehrere MMR-Proteine fehlen. Dies wird als MMR-Mangel bezeichnet und hat zwei wichtige Auswirkungen:
-
Ihr Krebs spricht möglicherweise besser auf eine Immuntherapie an.
-
Möglicherweise leiden Sie an einer genetischen Erkrankung namens Lynch-Syndrom, die das Risiko für verschiedene Krebsarten erhöht. Weitere genetische Tests können empfohlen werden.
-
PD-L1-Test
PD-L1 ist ein Protein, das manche Krebszellen nutzen, um sich vor dem Immunsystem zu verstecken. Durch die Produktion von PD-L1 verhindern diese Zellen Angriffe von Immunzellen. Immuntherapeutika, sogenannte Immun-Checkpoint-Inhibitoren, blockieren dieses Signal, sodass das Immunsystem den Krebs erkennen und zerstören kann.
Um zu prüfen, ob eine Immuntherapie anschlägt, testen Pathologen PD-L1 mithilfe des Combined Positive Score (CPS). Der CPS vergleicht die Anzahl der PD-L1-produzierenden Zellen (sowohl Krebszellen als auch benachbarte Immunzellen) mit der Gesamtzahl der Tumorzellen.
Was bedeuten die Ergebnisse?
-
Positiv (CPS ≥ 1) – PD-L1 ist vorhanden. Eine Immuntherapie kann eine wirksame Behandlungsoption sein.
-
Negativ (CPS < 1) – Es ist sehr wenig oder kein PD-L1 vorhanden. Die Erfolgschancen einer Immuntherapie sind geringer, sie kann jedoch in manchen Situationen dennoch in Betracht gezogen werden.
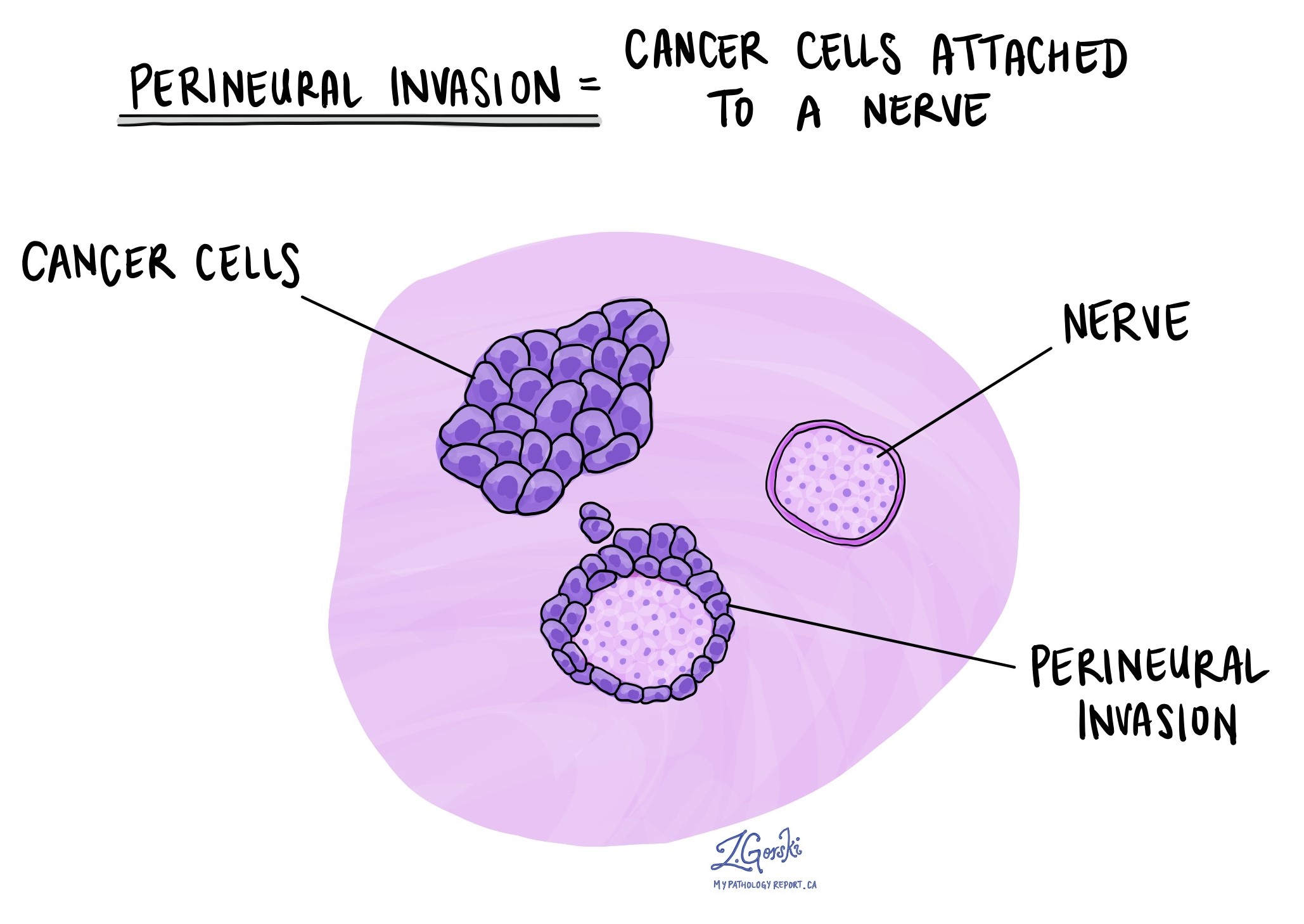
Perineurale Invasion
Perineurale Invasion (PNI) bedeutet, dass Krebszellen entlang oder um einen Nerv herum wachsen. Nerven sind wichtige Strukturen, die Signale zwischen dem Gehirn und dem Rest des Körpers übertragen. In der Speiseröhre verlaufen Nerven durch das Gewebe, das den Tumor umgibt.
Pathologen untersuchen das Gewebe sorgfältig unter dem Mikroskop, um Krebszellen zu identifizieren, die sich um die äußere Oberfläche eines Nervs wickeln oder in den Nerv selbst eindringen. Das Vorhandensein von PNI gilt als aggressives Merkmal, da es darauf hinweist, dass der Krebs in lokale Strukturen eindringt und nach der Behandlung möglicherweise wiederkehrt oder sich auf andere Bereiche ausbreitet.
Wenn eine PNI festgestellt wird, wird sie im Pathologiebericht als „positiv“ oder „vorhanden“ beschrieben. Wenn keine perineurale Invasion festgestellt wird, lautet der Bericht „negativ“ oder „nicht vorhanden“.
Lymphovaskuläre Invasion
Lymphovaskuläre Invasion (LVI) bedeutet, dass Krebszellen in kleine Blut- oder Lymphgefäße in der Nähe des Tumors in der Speiseröhre eingedrungen sind. Blutgefäße transportieren Sauerstoff und Nährstoffe zum und vom Gewebe, während Lymphgefäße den Abfluss von Flüssigkeit und den Transport von Immunzellen unterstützen. Beide Gefäßtypen können Krebszellen Wege in andere Körperteile bieten.
Wenn Pathologen das Gewebe unter dem Mikroskop untersuchen, suchen sie in den dünnwandigen Hohlräumen dieser Gefäße nach Krebszellansammlungen. Spezielle Färbungen, die sogenannte Immunhistochemie, können helfen, das Vorhandensein von Tumorzellen in den Gefäßen zu bestätigen.
LVI ist ein wichtiger Befund, da es das Risiko erhöht, dass sich der Krebs auf Lymphknoten oder andere Organe ausbreitet. Wenn LVI festgestellt wird, wird es als „vorhanden“ oder „positiv“ gemeldet. Wenn kein Krebs in den Gefäßen gefunden wird, lautet der Bericht „nicht vorhanden“ oder „negativ“. Das Vorhandensein von LVI kann Ihren Behandlungsplan beeinflussen, beispielsweise die Notwendigkeit einer Chemotherapie oder Bestrahlung nach der Operation.

Die Margen
In der Krebschirurgie Margen sind die Geweberänder, die zur Entfernung des Tumors eingeschnitten werden. Nach der Tumorentfernung untersucht ein Pathologe die Ränder unter dem Mikroskop, um festzustellen, ob sich am Rand des Gewebes Krebszellen befinden.
Ziel der Operation ist die Entfernung des gesamten Tumors mit einem Rand aus normalem Gewebe. Sind am Rand Krebszellen sichtbar, kann dies darauf hinweisen, dass Krebszellen im Körper verblieben sind. In Ihrem Pathologiebericht werden die Ränder wie folgt beschrieben:
-
Negativ (klar oder unbeteiligt) – Am Rand des Gewebes sind keine Krebszellen nachweisbar. Dies deutet darauf hin, dass der Tumor vollständig entfernt wurde.
-
Positiv (beteiligt) – Krebszellen befinden sich am Rand des Gewebes. Dies kann bedeuten, dass der Krebs im Körper verbleibt und eine zusätzliche Behandlung erforderlich ist.
 Je nach Operation und Lage des Tumors können unterschiedliche Ränder beschrieben werden:
Je nach Operation und Lage des Tumors können unterschiedliche Ränder beschrieben werden:
-
Schleimhautrand (lateral) – Die Innenfläche der Speiseröhre neben dem Tumor.
-
Tiefe Marge – Gewebe unter dem Tumor, tiefer in der Speiseröhrenwand.
-
Proximaler Rand – Die Oberkante des entfernten Gewebes, näher am Mund.
-
Distaler Rand – Die untere Kante, näher am Magen.
-
Radialer Rand – Die äußere Oberfläche der Speiseröhre, besonders wichtig bei Tumoren, die möglicherweise durch die Speiseröhrenwand in umliegendes Gewebe gewachsen sind.
In Ihrem Bericht werden alle diese Ränder aufgeführt und es wird angegeben, ob am Rand Krebs gefunden wurde oder nicht.
Lymphknoten und pathologisches Lymphknotenstadium (pN)
Lymphknoten sind kleine, bohnenförmige Organe, die Teil des Immunsystems sind. Sie helfen, Substanzen aus dem Körper zu filtern und spielen eine Rolle bei der Bekämpfung von Infektionen und Krebs. Krebszellen können sich vom ursprünglichen Tumor in der Speiseröhre über Lymphgefäße in nahegelegene Lymphknoten ausbreiten. Dieser Prozess wird genannt Metastasierung.
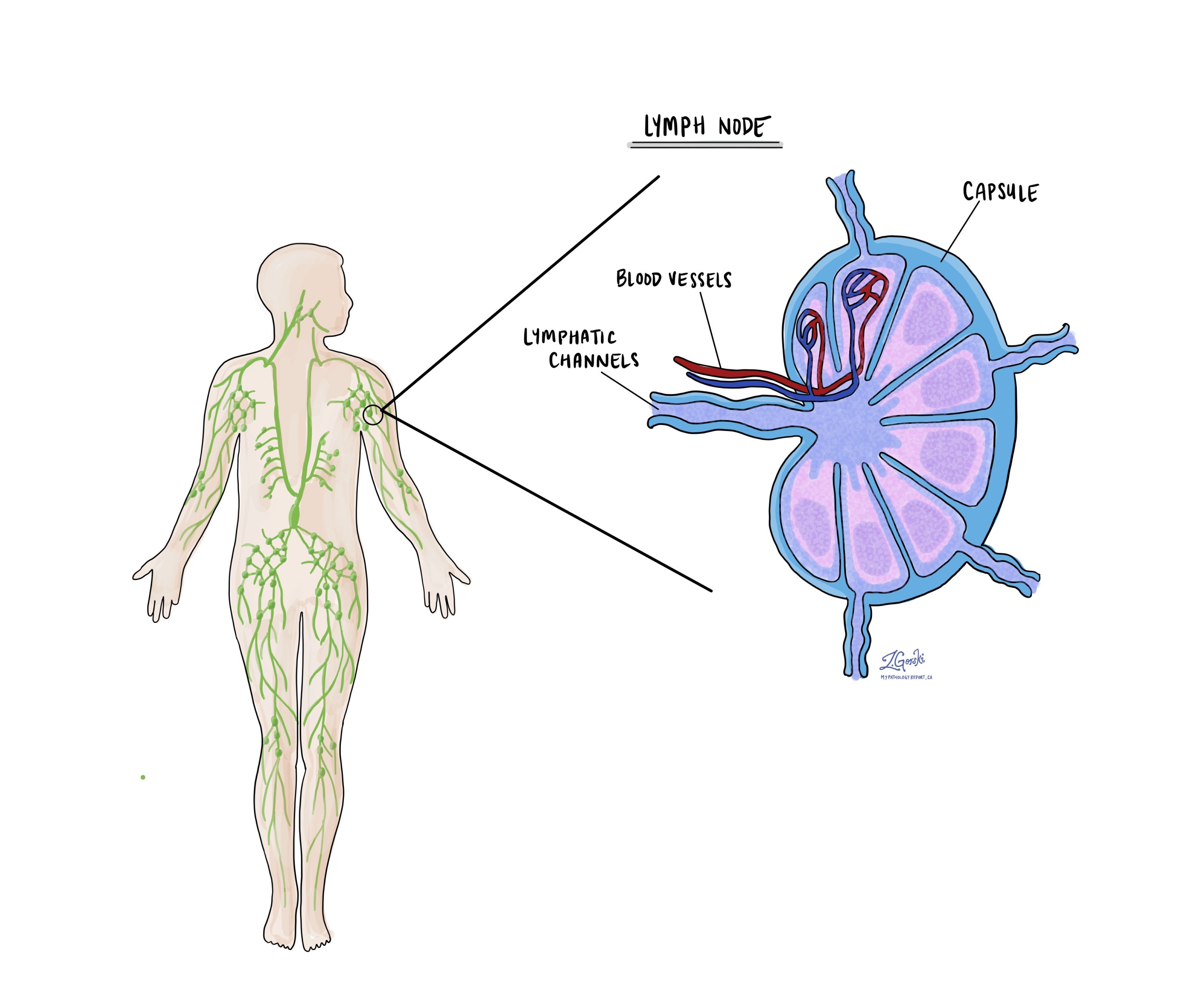
Bei Operationen bei einem Adenokarzinom der Speiseröhre werden häufig benachbarte Lymphknoten entfernt und unter dem Mikroskop auf Krebszellen untersucht. Ihr Pathologiebericht beschreibt, ob jeder Lymphknoten:
-
Positiv – Krebszellen werden im Lymphknoten gefunden.
-
Negative Gedanken und – Im Lymphknoten sind keine Krebszellen zu sehen.
Anhand der Anzahl der krebsbefallenen Lymphknoten lässt sich das pathologische Lymphknotenstadium (pN) bestimmen. Dieses ist Teil der Krebsstadienbestimmung und hilft Ihrem Arzt, das Ausmaß der Erkrankung einzuschätzen und die beste Behandlung auszuwählen.
Pathologische Knotenstadien beim Adenokarzinom der Speiseröhre:
-
pN0 – Kein Krebs in den Lymphknoten.
-
pN1 – Krebs in 1 oder 2 Lymphknoten gefunden.
-
pN2 – Krebs in 3 bis 6 Lymphknoten gefunden.
-
pN3 – Krebs in 7 oder mehr Lymphknoten gefunden.
-
pNX – Es wurden keine Lymphknoten eingesandt oder vom Pathologen ausgewertet.
Eine Lymphknotenbeteiligung ist ein starker Indikator für das mögliche Krebsverhalten und die Wahrscheinlichkeit eines Wiederauftretens oder einer Ausbreitung nach der Operation. Bei einem Krebsbefall in den Lymphknoten empfiehlt Ihr Arzt möglicherweise zusätzliche Behandlungen wie Chemotherapie, Bestrahlung oder Immuntherapie, um das Risiko eines Rückfalls zu verringern.
Reaktion auf vorherige Behandlung
Wenn Sie vor der Operation eine Chemotherapie, Strahlentherapie oder eine Kombination aus beidem (sogenannte neoadjuvante Therapie) erhalten haben, enthält Ihr Pathologiebericht häufig eine Beschreibung, wie der Tumor auf diese Behandlung reagiert hat. Dieser sogenannte Tumorregressions-Score hilft Ärzten zu verstehen, wie viel des Tumors vor der Operation zerstört wurde.
Ein häufig verwendetes System ist das modifizierte Ryan-Schema, das eine Punktzahl von 0 bis 3 vergibt, basierend darauf, wie viele Krebszellen nach der Behandlung noch unter dem Mikroskop sichtbar sind.
Punktzahl 0 – Vollständige Antwort: Im Gewebe sind keine Krebszellen mehr zu sehen. Das bedeutet, dass die Behandlung sehr gut angeschlagen hat und alle nachweisbaren Tumorzellen zerstört wurden.
Punktzahl 1 – Nahezu vollständige Reaktion: Es sind nur einzelne Krebszellen oder kleine Gruppen von Krebszellen sichtbar. Dies deutet auf eine sehr starke Reaktion auf die Behandlung hin, wobei nur sehr wenige Krebszellen übrig bleiben.
Punktzahl 2 – Teilantwort: Es sind noch Krebszellen vorhanden, aber der Pathologe sieht Anzeichen dafür, dass der Tumor durch die Behandlung geschrumpft oder beeinträchtigt wurde. Das bedeutet, dass die Behandlung zwar geholfen hat, der Tumor aber nicht vollständig zerstört wurde.
Punktzahl 3 – Schlechte oder keine Reaktion: Der Tumor sieht noch immer so aus wie vor der Behandlung, mit vielen Krebszellen und ohne deutliche Anzeichen einer Schrumpfung oder Schädigung. Das bedeutet, dass die Behandlung gegen den Tumor nicht gut gewirkt hat.
Was ist die Prognose?
Der wichtigste Faktor für die Prognose ist das Krebsstadium zum Zeitpunkt der Diagnose. Weitere Faktoren sind Tumorgrad, lymphovaskuläre Invasion (Krebs in Blutgefäßen oder Lymphgefäßen), perineurale Invasion (Krebs im Nervenbereich) und das Ansprechen auf die Behandlung. Tumoren mit HER2-Überexpression oder PD-L1-Positivität können auf zielgerichtete Therapien oder Immuntherapie ansprechen.
Fragen an Ihren Arzt
-
Welcher Teil meiner Speiseröhre ist vom Tumor betroffen?
-
War der Krebs auf die inneren Schichten der Speiseröhre beschränkt oder ist er tiefer in die Wand eingedrungen?
-
Waren Lymphknoten betroffen? Wenn ja, wie viele?
-
Gab es bei dem Krebs eine lymphovaskuläre oder perineurale Invasion?
-
Welchen histologischen Grad hatte der Tumor?
-
Waren die Operationsränder klar oder waren am Rand des entfernten Gewebes Krebszellen zu sehen?
-
Zeigte der Tumor Anzeichen einer Reaktion auf die Chemotherapie oder Bestrahlung (Tumorregression)?
-
Wurde ein Test auf HER2 durchgeführt und wenn ja, was waren die Ergebnisse?
-
Wurde der Krebs auf PD-L1 oder Mismatch-Reparaturproteine getestet und was bedeutet das für die Behandlung?
-
Was ist basierend auf dem Pathologiebericht mein pathologisches Stadium (pTNM)?
-
Welche zusätzlichen Behandlungen könnten aufgrund dieser Erkenntnisse empfohlen werden?