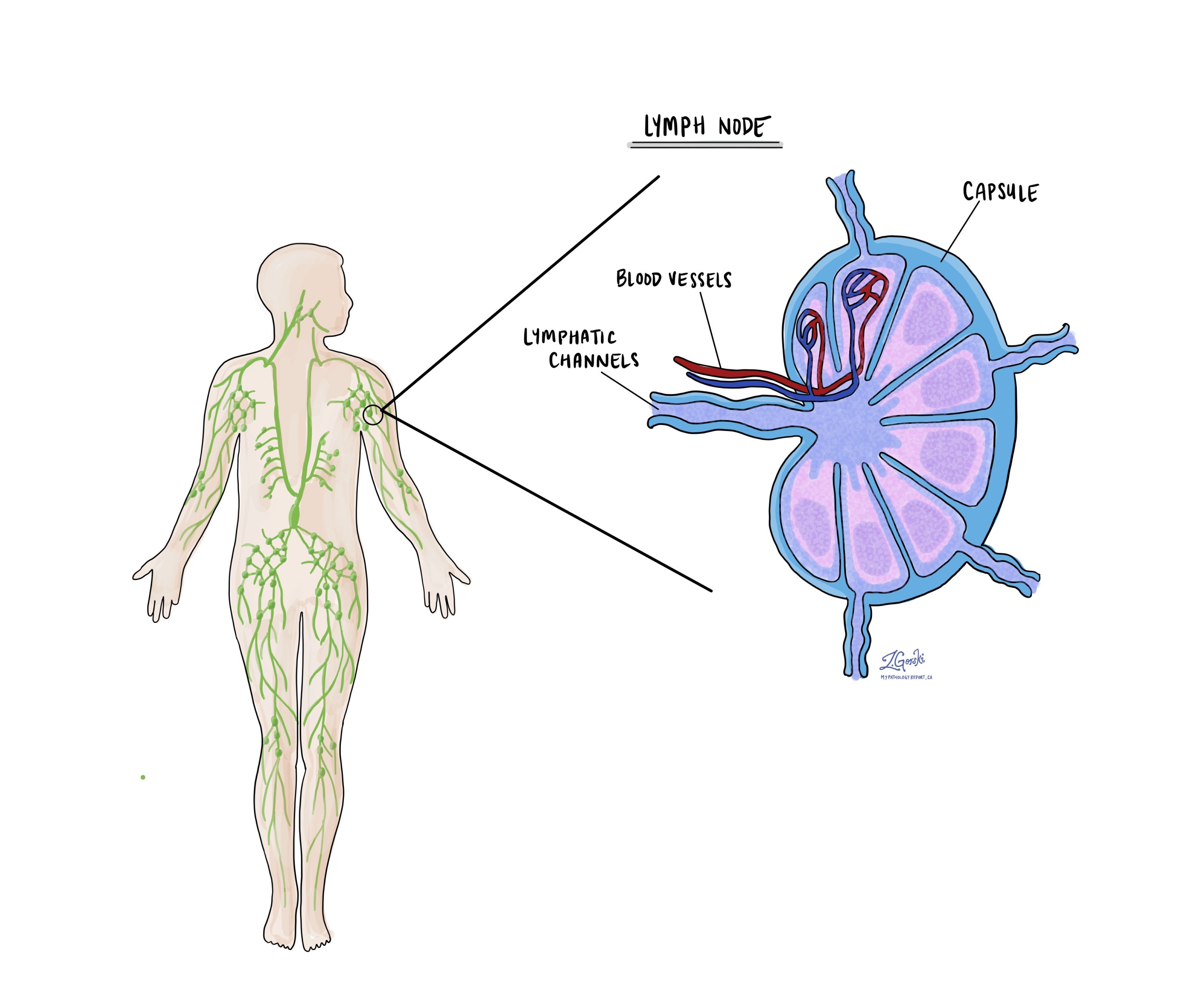
קרצינומה דוקטלי חודרנית היא הסוג הנפוץ ביותר של סרטן השד. זה נובע מ תאי האפיתל מצפים את צינורות השד ומתפשטים לתוך רקמת השד שמסביב. אם לא מטופלים, קרצינומה דוקטלי פולשנית יכולה להתפשט לחלקי גוף אחרים, כגון בלוטות לימפה, עצמות וריאות. שם נוסף לסוג זה של סרטן הוא קרצינומה פולשנית של השד.
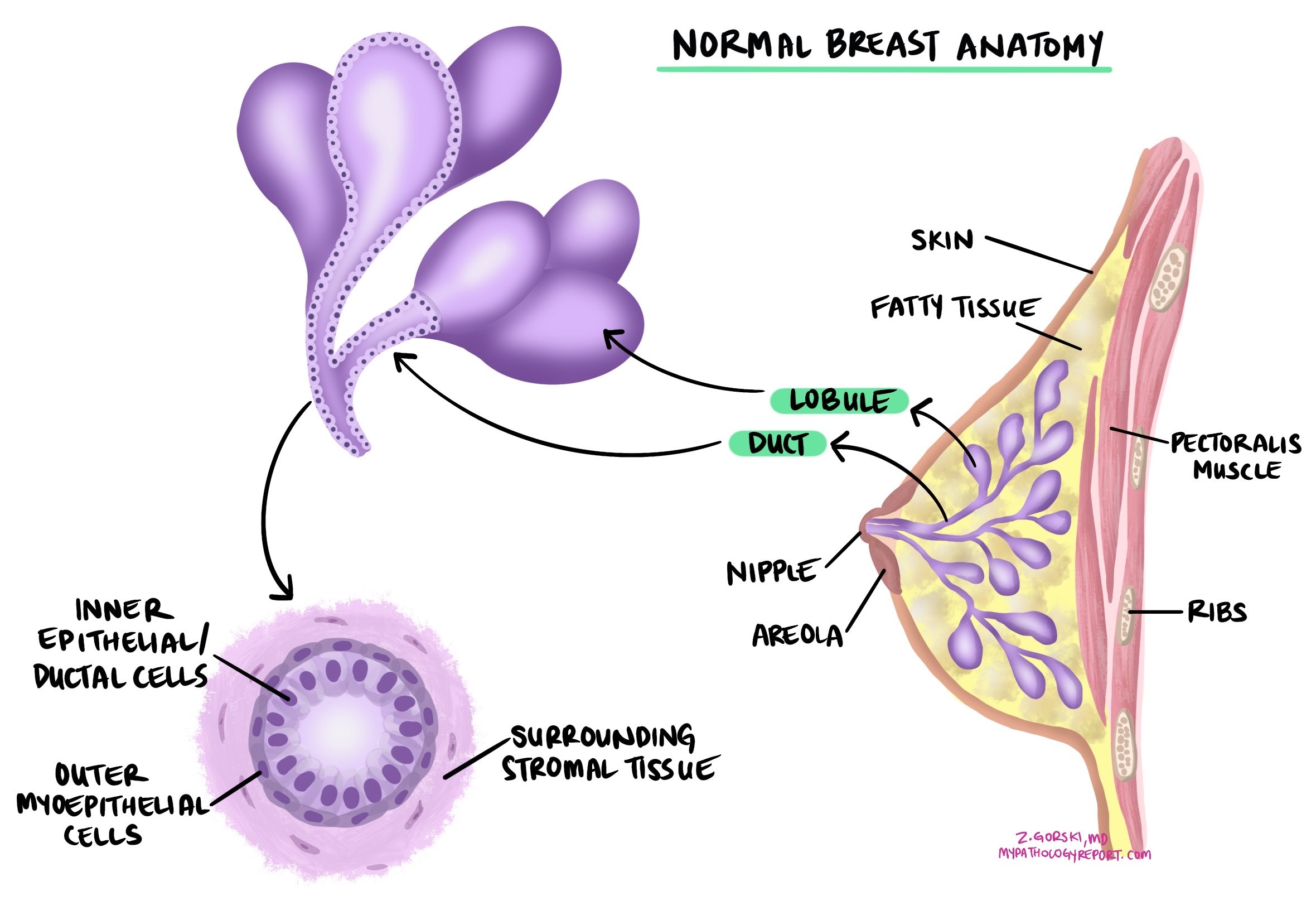
מהם התסמינים של קרצינומה דוקטלי חודרנית?
התסמין השכיח ביותר של קרצינומה צינורית פולשנית הוא גוש או מסה חדשים בשד. גושים אלה לרוב קשים ובעלי צורה לא סדירה, אך יכולים להיות גם רכים או עגולים. יש אנשים שמבחינים בשינויים בגודל או בצורה של השד, גומות או אדמומיות של העור, או שינויים בפטמה, כגון היפוך או הפרשה, במיוחד אם היא דמית. למרות שכאב בשד נגרם בדרך כלל ממצבים שאינם סרטניים, חלק מהמטופלות עשויות לחוות כאב מתמשך באזור אחד של השד. נפיחות בשד, גם ללא גוש, ובלוטות לימפה מוגדלות מתחת לזרוע או ליד עצם הבריח עשויים גם הם להיות סימנים של קרצינומה צינורית פולשנית.
מה גורם לקרצינומה דוקטלי חודרנית?
כיצד מתבצעת האבחנה הזו?
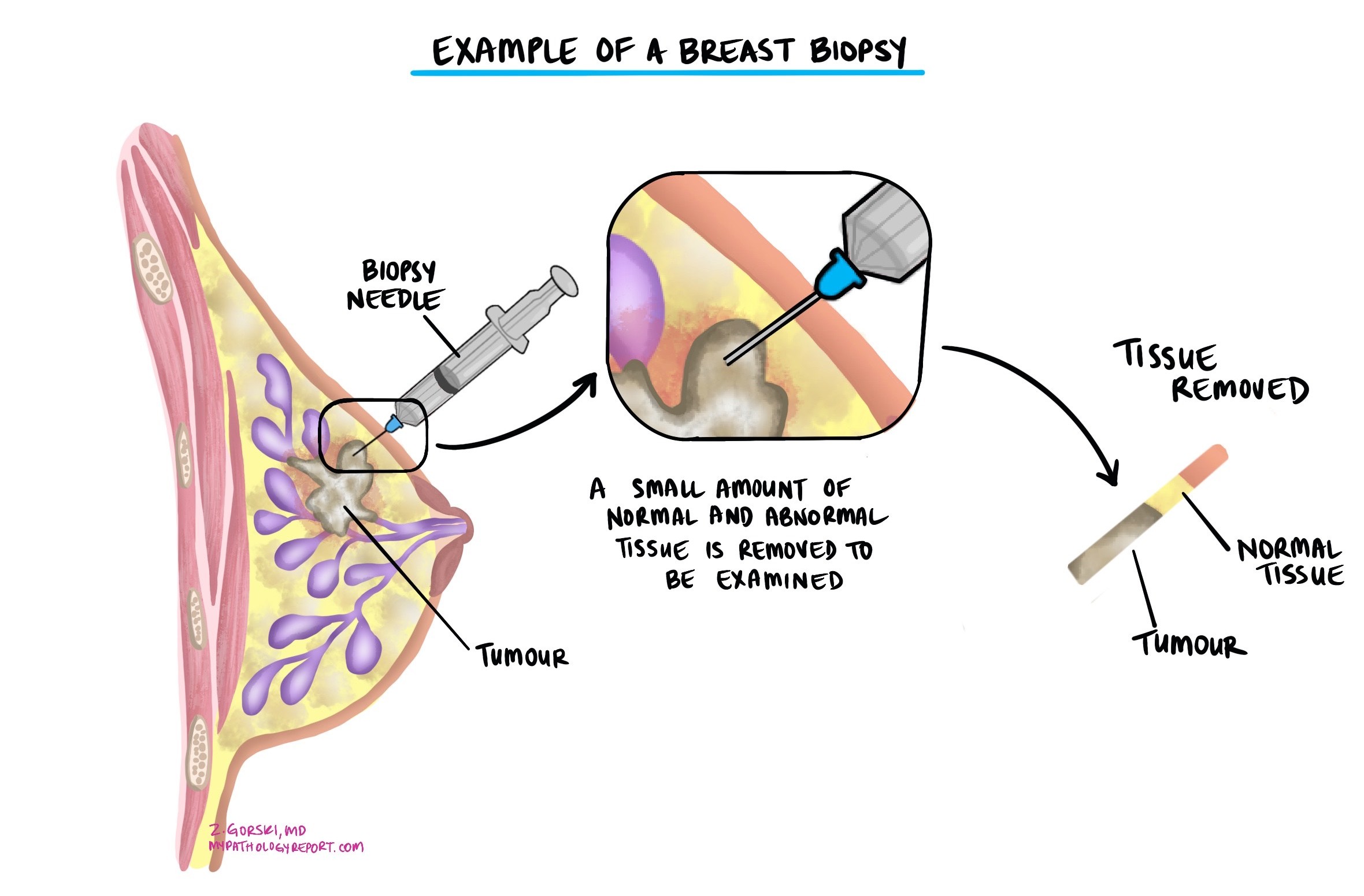
האבחנה של קרצינומה דוקטלי חודרנית נעשית בדרך כלל לאחר הסרת דגימה קטנה של הגידול בהליך הנקרא ביופסיה. לאחר מכן הרקמה נשלחת לפתולוג לבדיקה במיקרוסקופ. לאחר מכן ייתכן שיציעו לך ניתוח נוסף להסרת הגידול לחלוטין.
ציון היסטולוגי של נוטינגהאם
הדרגה ההיסטולוגית של נוטינגהאם, הידועה גם כדרגת Scarff-Bloom-Richardson שונה, היא מערכת המשמשת פתולוגים להערכת סרטן השד תחת המיקרוסקופ. זה עוזר לקבוע את האגרסיביות של הגידול ומספק מידע חשוב לתכנון הטיפול. הציון מבוסס על מידת השונות של תאי הסרטן מתאי שד רגילים וכמה מהר הם גדלים.
כדי לחשב את הציון, פתולוגים בודקים שלוש תכונות של הסרטן:
- היווצרות צינורות: זה מודד את המידה שבה תאים סרטניים יוצרים מבנים הדומים לבלוטות שד רגילות. אם רוב התאים יוצרים צינוריות, הגידול מקבל ציון נמוך יותר. פחות צינורות פירושם ציון גבוה יותר.
- פליאומורפיזם גרעיני: זה מתאר את השונות במראה של תאים סרטניים גרעינים (החלק בתא המכיל DNA) בהשוואה לתאים נורמליים. הציון נמוך אם הגרעינים אחידים ודומים לאלו של תאים רגילים. אם הם שונים מאוד ולא סדירים, הציון גבוה יותר.
- ספירה מיטוטית: זה מודד את מספר התאים הסרטניים שמתחלקים באופן פעיל. תאים שמתחלקים עוברים תהליך שנקרא מיטוזה והם מכונים דמויות מיטוטיות. מספר גבוה יותר של תאים מתחלקים מצביע על כך שהגידול גדל במהירות, וכתוצאה מכך ציון גבוה יותר.
כל תכונה מקבלת ניקוד מ-1 עד 3, כאשר 1 מציין רמה קרובה לנורמה ו-3 מציין רמה חריגה יותר. הציונים מתווספים יחד כדי לתת ציון כולל בין 3 ל-9, הקובע את הציון.

הציון הכולל מציב את הגידול באחת משלוש דרגות:
- כיתה א' (ציון נמוך): ציון כולל של 3 עד 5. תאים סרטניים לרוב דומים לתאים רגילים ובדרך כלל גדלים בקצב איטי.
- כיתה ב' (כיתה ביניים): ציון כולל של 6 עד 7. התאים הסרטניים מראים יותר הבדלים מהרגיל וגדלים בקצב מתון.
- כיתה ג' (כיתה גבוהה): ציון כולל של 8 עד 9. תאים סרטניים נראים שונים באופן מובהק מתאים רגילים ונוטים לגדול מהר יותר.
הציון עוזר לרופאים לחזות עד כמה הסרטן יהיה אגרסיבי. סוגי סרטן בדרגה 1 לרוב גדלים לאט ועשויים להיות להם תוצאה טובה יותר. סוגי סרטן דרגה 3 יכולים לגדול ולהתפשט מהר יותר ועשויים לדרוש טיפול אגרסיבי יותר. הרופא שלך ישתמש בדרגה ובגורמים אחרים, כגון גודל הגידול והאם נמצא סרטן בבלוטות הלימפה, כדי להנחות את החלטות הטיפול.
ביומרקרים לסרטן השד
קולטן לאסטרוגן (ER) וקולטן לפרוגסטרון (PR)
קולטני הורמונים הם חלבונים המצויים בחלק מתאי סרטן השד. שני הסוגים העיקריים שנבדקו הם קולטן לאסטרוגן (ER) ו קולטן פרוגסטרון (PR)תאי סרטן עם קולטנים אלה משתמשים בהורמונים כמו אסטרוגן ופרוגסטרון כדי לקדם צמיחה וחלוקה. בדיקת ER ו-PR מסייעת בהכוונת הטיפול ובניבוי הפרוגנוזה.
דוח הפתולוגיה שלך יכלול בדרך כלל:
-
אחוז תאים חיוביים: לדוגמה, "80% ER חיובי" פירושו של 80% מתאי הסרטן יש קולטנים לאסטרוגן.
-
עוצמת הצביעה: מדווח כחלש, בינוני או חזק, זה מצביע על מספר הקולטנים הקיימים בתאי הסרטן.
-
ציון כללי (ציון Allred או H): זה משלב אחוז ועוצמה, כאשר ציונים גבוהים יותר מצביעים על תגובה טובה יותר לטיפול הורמונלי.
תאי סרטן מתוארים כחיוביים לקולטני הורמונים אם ER או PR נמצאים בלפחות 1% מהתאים. סוגי סרטן אלה לרוב גדלים לאט יותר, הם פחות אגרסיביים, ובדרך כלל מגיבים היטב לטיפולים חוסמי הורמונים, כגון טמוקסיפן או מעכבי ארומטאז (למשל, אנסטרוזול, לטרוזול או אקסמסטאן). טיפול הורמונלי מסייע בהפחתת הסיכוי להישנות הסרטן.
גידולים עם רמת ER חיובית בין 1% ל-10% נחשבים ל-ER חיוביים נמוך. סוגי סרטן אלה עדיין בדרך כלל מגיבים טוב יותר לטיפול הורמונלי בהשוואה לסרטן שלילי ל-ER.
בדיקת HER2 באמצעות אימונוהיסטוכימיה
אימונוהיסטוכימיה (IHC) הוא מבחן בו משתמשים פתולוגים כדי למדוד את כמות חלבון HER2 על פני השטח של תאי סרטן השד. HER2 (קולטן גורם גדילה אפידרמלי אנושי 2) הוא חלבון המסייע בשליטה על צמיחת התאים. חלק מסוגי סרטן השד מייצרים יותר מדי חלבון HER2, מה שעלול לגרום לתאים לגדול ולהתחלק מהר יותר.
כדי לבצע את הבדיקה, הפתולוג מיישם נוגדנים מיוחדים הנקשרים לחלבוני HER2 על דגימה קטנה של רקמת גידול. צבע צבעוני הופך את הנוגדנים הללו לגלויים תחת המיקרוסקופ. על ידי בחינת עוצמת הצביעה ודפוסה, הפתולוג מקצה ציון המשקף כמה חלבון HER2 קיים על תאי הסרטן.
ציוני אימונוהיסטוכימיה של HER2
דוח הפתולוגיה שלך יתאר את תוצאת HER2 IHC כציון מ-0 עד 3+, עם סיווגים נוספים עבור ביטוי HER2 נמוך ו-HER2 נמוך במיוחד:
- 0 (שלילי) – אין צביעה גלויה של הממברנה, כלומר אין חלבון HER2 שניתן לגילוי. גידולים עם דפוס זה הם שליליים ל-HER2. טיפולי HER2 ממוקדים אינם יעילים עבור סוגי סרטן אלה.
- 0+ (אולטרה נמוך) – צביעה קלושה או כמעט ולא נראית לעין של הממברנה ב-10% או פחות מתאי הגידול. דפוס זה נקרא HER2-ultralow. למרות שעדיין נחשב HER2-שלילי, ישנם מחקרים המצביעים על כך שגידולים אלה עשויים להגיב לטיפולים ממוקדים חדשים כגון trastuzumab-deruxtecan במצב גרורתי (מתקדם). גידולים ללא צביעה כלל נותרים אינם זכאים לטיפול זה.
- 1+ (נמוך) – צביעת קרום חלשה ולא שלמה ביותר מ-10% מתאי הסרטן. גידולים אלה הם בעלי רמות HER2 נמוכות ונחשבים שליליים ל-HER2 לפי קריטריונים מסורתיים. עם זאת, במסגרת גרורתית, סרטן עם רמות HER2 נמוכות עשוי להיות זכאי גם לטיפולים המכוונים לרמות נמוכות של חלבון HER2.
- 2+ (דו משמעי) – צביעה חלשה עד בינונית של הממברנה ביותר מ-10% מתאי הגידול. תוצאה זו נחשבת גבולית, ויש צורך בבדיקות נוספות - בדרך כלל הכלאה in situ (ISH) - כדי לקבוע אם הסרטן הוא באמת HER2 חיובי או HER2 שלילי.
אם בדיקת ISH שלילית (ללא הגברת גן HER2), התוצאה מסווגת כ-HER2-נמוכה.
- 3+ (חיובי) – צביעת קרום חזקה ומלאה ביותר מ-10% מתאי הסרטן. זה מצביע על גידול חיובי ל-HER2. סוגי סרטן חיוביים ל-HER2 לרוב גדלים מהר יותר אך מגיבים היטב לטיפולים המכוונים ל-HER2 כגון טרסטוזומאב (הרספטין), פרטוזומאב או טרסטוזומאב-דרוקסטאן.
בדיקת HER2 על ידי הכלאה in situ
כאשר תוצאת HER2 IHC היא 2+ (גבולית או דו משמעית), מבוצעת בדיקה נוספת הנקראת הכלאה in situ (ISH). בדיקה זו בוחנת את הגן HER2 עצמו ולא את החלבון שעל פני התא.
בתא שד תקין, בדרך כלל ישנם שני עותקים של הגן HER2. בסוגי סרטן מסוימים, גן זה מתגבר, כלומר התא מכיל עותקים נוספים רבים. יותר גנים של HER2 מובילים לייצור של יותר חלבון HER2, מה שעלול לגרום לגידול הסרטני מהר יותר.
בדיקת ISH משתמשת בצבעי פלואורסצנציה או כסף מיוחדים כדי להפוך את גני HER2 לגלויים תחת המיקרוסקופ. פתולוג סופר כמה עותקים של גן HER2 קיימים ומשווה אותם למספר העותקים של גן אחר (CEP17) באותו כרומוזום. התוצאה מדווחת כיחס וספירת אותות, אשר יחד קובעים האם הסרטן מוגבר על ידי HER2 (חיובי) או לא מוגבר (שלילי).
הבנת תוצאות HER2 ISH
דוח הפתולוגיה שלך עשוי לתאר את תוצאת HER2 ISH באמצעות אחת מחמש קבוצות המוגדרות בהנחיות בינלאומיות:
-
קבוצה 1 (חיובי/מוגבר) – יחס HER2:CEP17 הוא 2.0 ומעלה, ויש לפחות 4 אותות HER2 לכל תא. משמעות הדבר היא שהסרטן חיובי ל-HER2, ובדרך כלל מומלץ להשתמש בטיפולים המכוונים ל-HER2.
-
קבוצה 2 (דו משמעית) – יחס HER2:CEP17 הוא 2.0 או גבוה יותר, אך ישנם פחות מ-4 אותות HER2 לכל תא. זוהי תוצאה לא שכיחה ומורכבת. ברוב המקרים, סקירה נוספת עם תוצאות IHC מסייעת לקבוע את סטטוס HER2 הסופי.
-
קבוצה 3 (דו משמעית) – יחס HER2:CEP17 נמוך מ-2.0, אך ישנם 6 אותות HER2 או יותר לכל תא. משמעות הדבר היא שישנם עותקים נוספים של גנים של HER2 אך לא מספיק יחסית ל-CEP17 כדי להיות חיובי באופן ברור. מתאם עם תוצאות IHC מסייע בהנחיית הפרשנות.
-
קבוצה 4 (דו משמעית) – יחס HER2:CEP17 נמוך מ-2.0, וישנם 4 עד 6 אותות HER2 לכל תא. זהו דפוס גבולי נוסף שמפורש יחד עם ממצאי IHC.
-
קבוצה 5 (שלילית / לא מוגברת) – יחס HER2:CEP17 נמוך מ-2.0, ויש פחות מ-4 אותות HER2 לכל תא. משמעות הדבר היא שהסרטן הוא HER2 שלילי, וטיפולים המכוונים ל-HER2 אינם יעילים.
שילוב תוצאות IHC ו-ISH
פתולוגים תמיד מפרשים תוצאות ISH לצד ציון HER2 IHC כדי לספק את הסיווג המדויק ביותר:
-
אם IHC הוא 3+, הגידול חיובי ל-HER2, ואין צורך בבדיקות נוספות.
-
אם IHC הוא 2+, תוצאת ה-ISH קובעת האם הגידול הוא HER2 חיובי או HER2 שלילי.
-
אם IHC הוא 0, 0+ או 1+, הגידול נחשב שלילי ל-HER2 לפי קריטריונים סטנדרטיים, גם אם ISH לא מראה הגברה.
עם זאת, מחקרים חדשים הראו כי סרטן שד עם תוצאות HER2 נמוכות (IHC 1+ או 2+ / ISH שלילי) או HER2 אולטרה-נמוכות (IHC 0+ / ISH שלילי) עשוי להגיב לטיפולים חדשים יותר כמו טרסטוזומאב-דרוקסטאן במסגרת גרורתית. חולות ללא צביעת HER2 כלל (IHC 0) נותרות אינן זכאיות לטיפולים אלה.
קרצינומה צינורית פולשנית עם מאפיינים מיקרופפילריים
מאפיינים מיקרופפילריים בקרצינומה דוקטלי פולשנית מתייחסים לדפוס ספציפי של גידול סרטן שנראה תחת המיקרוסקופ. המונח "מיקרו-פילרי" מתאר מקבצים קטנים של תאי גידול שנראים כמרחפים במרחבים פתוחים. תכונות אלו חשובות מכיוון שסרטן עם מאפיינים מיקרופפילריים נוטים יותר לפלוש לכלי לימפה סמוכים ולהתפשט ל בלוטות לימפה.
אם יותר מ-90% מהגידול מציג תכונות מיקרופפילריות, הוא מסווג כקרצינומה מיקרופפילרית פולשנית. זה נחשב לסוג מובחן של סרטן שד שעשוי לדרוש שיקולי טיפול ספציפיים.
בעוד שסרטן עם מאפיינים מיקרופפילריים נוטים להתנהג בצורה אגרסיבית יותר, זה לא תמיד אומר תוצאה גרועה יותר. מחקרים מראים שלגידולים אלו יש סיכוי גבוה יותר לחזור באותו אזור או לבית השחי בלוטות לימפה. ובכל זאת, הם אינם משפיעים באופן משמעותי על ההישרדות הכוללת או על הסיכון של התפשטות הסרטן לחלקים מרוחקים של הגוף בהשוואה לסוגים אחרים של קרצינומה דקטלית פולשנית באותו גודל ושלב.
קרצינומה צינורית פולשנית עם מאפיינים ריריים
מאפיינים ריריים בקרצינומה דוקטלי פולשנית מתייחסים לדפוס מסוים בהם תאי הגידול מוקפים בכמויות גדולות של מוקין, חומר דמוי ג'ל שנמצא בדרך כלל במגוון חלקי הגוף. תחת המיקרוסקופ, סוגי הסרטן הללו מופיעים כצבירים של תאי גידול הצפים בבריכות של מוצין.
אם יותר מ-90% מהגידול מציג מאפיינים ריריים, הוא מסווג כ קרצינומה רירית פולשנית. זה נחשב לסוג מובחן של סרטן שד עם מאפיינים ייחודיים ולעתים קרובות פרוגנוזה טובה יותר בהשוואה לסוגים אחרים של קרצינומה דוקטלי פולשנית.
סרטן עם מאפיינים ריריים נוטים לגדול לאט יותר ויש להם פחות סיכוי גרורות ל בלוטות לימפה או חלקים אחרים בגוף. כתוצאה מכך, הם קשורים לעתים קרובות לתוצאה חיובית יותר. עם זאת, אם לגידול יש שילוב של אזורים ריריים ולא ריריים, ההתנהגות עשויה להיות תלויה בשיעור המאפיינים הריריים ובמאפיינים אחרים של הגידול.
גודל הגידול
גודלו של גידול בשד חשוב מכיוון שהוא משמש לקביעת שלב הגידול הפתולוגי (pT) ומכיוון שגידולים גדולים יותר נוטים יותר גרורות (להתפשט) ל בלוטות לימפה ושאר חלקי הגוף. ניתן לקבוע את גודל הגידול רק לאחר הסרת הגידול כולו. מסיבה זו, הוא לא ייכלל בדוח הפתולוגי שלך לאחר א ביופסיה.
הארכת גידול
קרצינומה צינורית פולשנית מתחילה בתוך השד, אך הגידול עלול להתפשט לעור שמעליו או לשרירי דופן בית החזה. המונח "התפשטות גידול" משמש כאשר תאי גידול נמצאים בעור או בשרירים שמתחת לשד. התפשטות גידול חשובה משום שהיא קשורה לסיכון גבוה יותר שהגידול יחזור לאחר הטיפול (הישנות מקומית) או שתאי סרטן ישגרו גרורות לאתר גוף מרוחק, כמו הריאות. הוא משמש גם לקביעת שלב הגידול הפתולוגי (pT).
פלישה לימפווסקולרית
מדד נטל סרטן שיורי
מדד השארת הסרטן (RCB) מודד את כמות הסרטן שנותרה בשד ובסמוך בלוטות לימפה לאחר טיפול ניאו-אדג'ובנטי (טיפול הניתן לפני ניתוח). המדד משלב מספר מאפיינים פתולוגיים לציון אחד ומסווג את תגובת הסרטן לטיפול. רופאים מאוניברסיטת טקסס MD Anderson Cancer Center פיתחו את ה-RCB (http://www.mdanderson.org/breastcancer_RCB).
כך מחושב הציון:
- גודל מיטת הגידול בשד: פתולוגים מודדים את שני הממדים הגדולים ביותר של האזור שבו נמצא הגידול, הנקרא מיטת הגידול. אזור זה עשוי להכיל תערובת של רקמה תקינה, תאים סרטניים ורקמת צלקת מהטיפול.
- תאי סרטן: התאיות הסרטנית מעריכה את האחוז של מיטת הגידול שעדיין מכילה תאים סרטניים. זה כולל גם סרטן פולשני (סרטן שהתפשט לרקמה הסובבת) וגם סרטן באתרו (תאים סרטניים שלא התפשטו).
- אחוז של מחלות באתר: בתוך מיטת הגידול, פתולוגים מעריכים גם את אחוז הסרטן שנמצא באתרו, כלומר התאים הסרטניים מוגבלים לצינורות החלב או לאונות ולא התפשטו לרקמה שמסביב.
- מעורבות בלוטות הלימפה: מספר בלוטות הלימפה המכילות תאים סרטניים (בלוטות לימפה חיוביות) נספר, וכן נמדד גודלו של מקבץ התאים הסרטניים הגדול ביותר בבלוטות הלימפה.
תכונות אלו משולבות באמצעות נוסחה סטנדרטית לחישוב ציון RCB.
בהתבסס על ציון RCB, החולים מחולקים לארבע קטגוריות:
- RCB-0 (תגובה מלאה פתולוגית): לא מתגלה שארית סרטן פולשני בשד או בבלוטות הלימפה.
- RCB-I (נטל מינימלי): יש מעט מאוד שאריות סרטן.
- RCB-II (עומס בינוני): נותרה כמות מתונה של סרטן.
- RCB-III (נטל נרחב): נותרת כמות גדולה של סרטן בשד או בבלוטות הלימפה.
סיווג RCB עוזר לחזות את הסבירות של המטופל להישאר נקי מסרטן לאחר הטיפול. לחולים עם סיווג RCB-0 יש בדרך כלל את התוצאות הטובות ביותר, עם הסיכויים הגבוהים ביותר להישרדות ארוכת טווח ללא הישנות. ככל שקטגוריית RCB עולה מ-RCB-I ל-RCB-III, הסיכון להישנות סרטן עולה, מה שעשוי לעורר טיפולים נוספים להפחתת סיכון זה.
שלב פתולוגי לקרצינומה דוקטלי חודרנית
מערכת הבימוי הפתולוגית לקרצינומה חודרנית של השד עוזרת לרופאים להבין עד כמה הסרטן התפשט ולתכנן את הטיפול הטוב ביותר. המערכת משתמשת בעיקר ב-TNM staging, שהוא ראשי תיבות של Tumor, Nodes ו-Getastasis. סרטן בשלבים מוקדמים (כמו T1 או N0) עשויים לדרוש רק ניתוח ואולי גם הקרנות, בעוד ששלבים מתקדמים יותר (כמו T3 או N3) עשויים להזדקק לשילוב של ניתוח, הקרנות, כימותרפיה וטיפולים ממוקדים. שלב נכון מבטיח שהמטופלים יקבלו את הטיפולים היעילים ביותר בהתבסס על היקף מחלתם, מה שיכול לשפר את שיעורי ההישרדות ואיכות החיים.
שלב הגידול (pT)
תכונה זו בוחנת את הגודל וההיקף של גידול השד. הגידול נמדד בסנטימטרים, ומעריכים את צמיחתו מעבר לרקמת השד.
T0: אין עדות לגידול ראשוני. זה אומר שלא ניתן למצוא גידול בשד.
T1: הגידול הוא 2 סנטימטרים ומטה בממדים הגדולים ביותר. שלב זה מחולק עוד יותר ל:
- T1mi: הגידול הוא בגודל מילימטר אחד או פחות.
- T1a: הגידול גדול ממילימטר אחד אך לא גדול מ-1 מילימטרים.
- T1b: הגידול גדול מ-5 מילימטרים אך לא גדול מ-10 מילימטרים.
- T1c: הגידול גדול מ-10 מילימטרים אך לא יותר מ-20 מילימטרים.
T2: הגידול גדול מ-2 ס"מ אך לא גדול מ-5 ס"מ.
T3: הגידול גדול מ-5 סנטימטרים.
T4: הגידול התפשט לדופן החזה או לעור, ללא קשר לגודלו. שלב זה מחולק עוד יותר ל:
- T4a: הגידול פלש לקיר בית החזה.
- T4b: הגידול התפשט לעור, גרם לכיבים או נפיחות.
- T4c: גם T4a וגם T4b קיימים.
- T4d: סרטן שד דלקתי, המאופיין באדמומיות ונפיחות של עור השד.
שלב צמתים (pN)
תכונה זו בודקת אם הסרטן התפשט לסביבה הקרובה בלוטות לימפה, שהם מבנים קטנים בצורת שעועית המצויים בכל הגוף.
N0: לא נמצא סרטן בבלוטות הלימפה הסמוכות.
N0(i+): תאי גידול מבודדים בלבד.
N1: הסרטן התפשט ל-1 עד 3 בלוטות לימפה ביתיות (מתחת לזרוע).
- N1mi: מיקרו-גרורות בלבד.
- N1a: גרורות ב-1-3 בלוטות לימפה ביתיות, לפחות גרורה אחת גדולה מ-2.0 מ"מ.
- N1b: גרורות בבלוטות זקיף שד פנימיות איפסי-צדדיות, למעט ITCs
N2: הסרטן התפשט ל:
- N2a: 4 עד 9 בלוטות לימפה בבית השחי.
- N2b: בלוטות לימפה פנימיות בשד ללא מעורבות של בלוטות לימפה ביתיות.
N3: הסרטן התפשט ל:
- N3a: 10 בלוטות לימפה ביתיות או יותר או שתי בלוטות לימפה אינפרקלוויקולריות (מתחת לעצם הבריח).
- N3b: בלוטות לימפה פנימיות בשד ובלוטות לימפה ביתיות.
- N3c: בלוטות לימפה סופרקלביקולריות (מעל עצם הבריח).
פרוגנוזה
הפרוגנוזה של קרצינומה צינורית פולשנית תלויה במספר גורמים מרכזיים, כולל עד כמה הסרטן מתקדם, כיצד הוא נראה תחת מיקרוסקופ וכיצד הוא מגיב לטיפול. להלן כמה מהמאפיינים החשובים ביותר שיכולים להשפיע על התוצאה.
- שלב וגודל הגידול: לסרטן המתגלה מוקדם ומוגבל לשד יש את הפרוגנוזה הטובה ביותר. לדוגמה, שיעור ההישרדות ל-5 שנים עבור סרטן שד מקומי הוא מעל 95%. אם הסרטן התפשט לבלוטות הלימפה או לחלקים אחרים בגוף, התחזית פחות טובה.
- ציון גידול: הדרגה מתארת עד כמה תאי הסרטן נראים לא תקינים. גידולים בדרגה גבוהה נוטים לגדול ולהתפשט מהר יותר, מה שעלול להוביל לסיכון גבוה יותר להישנות.
- קולטן הורמונים ומצב HER2: סרטן חיובי לקולטני הורמונים (אסטרוגן או פרוגסטרון) בדרך כלל מגיב היטב לטיפול הורמונלי ובעל תחזית טובה יותר. סרטן חיובי ל-HER2 הוא אגרסיבי יותר אך לעיתים קרובות מגיב לטיפולים ממוקדים כמו טרסטוזומאב. סרטן טריפל-נגטיב (חסר שלושת הקולטנים) קשה יותר לטיפול ועשוי להיות בעל סיכון גבוה יותר להישנות.
- פלישה לימפווסקולרית: אם תאי סרטן נמצאים בכלי דם קטנים או תעלות לימפה ליד הגידול, קיים סיכון גבוה יותר להתפשטות הסרטן.
- שוליים כירורגיים: אם כל תאי הסרטן הוסרו במהלך הניתוח ואף אחד לא נראה בקצה הרקמה (שוליים שליליים), הסיכוי להישנות נמוך יותר. שוליים חיוביים עשויים להעיד על כך שחלק מהסרטן נותר מאחור.
- בדיקה גנטית של הגידול: בדיקות כמו ציון הישנות של 21 גנים או חתימת 70 גנים יכולות לעזור לחזות את הסיכון לחזרת הסרטן ולסייע בהנחיית החלטות לגבי הצורך בכימותרפיה.
- תגובה לטיפול ניאו-אדג'ובנטי: טיפול ניאו-אדג'ובנטי הוא טיפול הניתן לפני ניתוח. אם לא נמצא סרטן בזמן הניתוח (הנקרא תגובה פתולוגית מלאה), התחזית בדרך כלל טובה מאוד, במיוחד עבור סרטן HER2 חיובי ו- triple-negative. אם הסרטן נותר, רופאים עשויים להשתמש במדד נטל הסרטן השיורי כדי להעריך את הסיכון להישנות ולסייע בתכנון טיפול נוסף.
שאלות לשאול את הרופא שלך
-
מה היה גודל ודרגת הגידול בשד שלי?
-
האם היו בלוטות לימפה מעורבות, ואם כן, כמה?
-
מהו סטטוס קולטן ההורמונים ו-HER2 של הגידול שלי?
-
האם שולי הניתוח היו נקיים מסרטן?
-
האם אצטרך טיפול נוסף, כגון הקרנות, כימותרפיה או טיפול הורמונלי?
משאבים מועילים אחרים