door Jason Wasserman MD PhD FRCPC
16 november 2023
Invasief lobulair carcinoom is een vorm van borstkanker. Invasief lobulair carcinoom begint gewoonlijk met een niet-kankerachtige groei van abnormale borstcellen genaamd lobulair carcinoom in situ (LCIS). LCIS kan maanden of jaren aanwezig zijn voordat het een invasief lobulair carcinoom wordt. Bovendien hebben patiënten met een eerdere diagnose van LCIS een hoger risico op het ontwikkelen van invasief lobulair carcinoom.
Hoe wordt deze diagnose gesteld?
De diagnose invasief lobulair carcinoom wordt meestal gesteld nadat een klein stukje van de tumor is verwijderd in een procedure die a biopsie. Het weefsel wordt vervolgens naar een patholoog gestuurd voor onderzoek onder een microscoop.
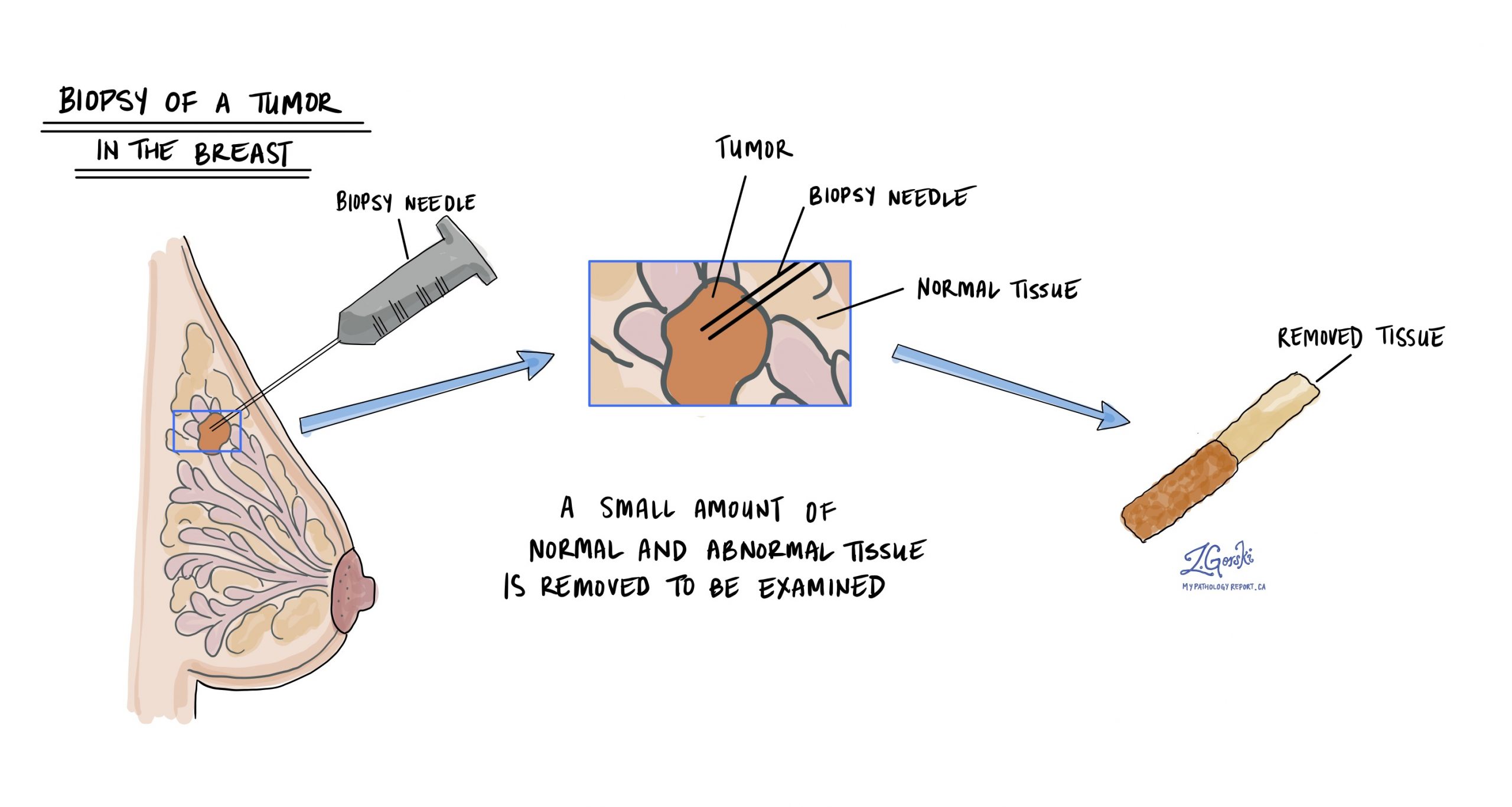
Wat betekent het als de tumor wordt beschreven als het klassieke type of het pleomorfe type?
Pathologen verdelen invasief lobulair carcinoom in twee typen – het klassieke type en het pleomorfe type – op basis van hoe de kankercellen eruitzien wanneer ze onder een microscoop worden onderzocht. Het tumortype is belangrijk omdat de kans hierop groter is bij invasief lobulair carcinoom van het pleomorfe type uitzaaien (verspreid) naar lymfeklieren en andere delen van het lichaam.
- Klassiek type – Dit is het meest voorkomende type invasief lobulair carcinoom. De kankercellen zijn klein en ze reizen door het weefsel als afzonderlijke cellen (ze zijn niet gehecht aan de andere kankercellen).
- Pleomorf type – De kankercellen van het pleomorfe type zijn groter en zien er meer abnormaal uit dan de cellen van het klassieke type. De kern van de cel (het deel van de cel dat het grootste deel van het genetische materiaal bevat) is ook hyperchromatisch (donkerder) en groter dan de kern in het klassieke type.
Wat is de histologische graad van Nottingham voor invasief lobulair carcinoom en waarom is het belangrijk?
Pathologen gebruiken een systeem dat het Nottingham-beoordelingssysteem wordt genoemd om invasief lobulair carcinoom in drie niveaus of gradaties te verdelen - 1, 2 en 3. De graad is belangrijk omdat graad 2 en graad 3 tumoren de neiging hebben om sneller te groeien en meer kans hebben om zich te verspreiden naar andere delen van het lichaam, zoals lymfeklieren.
Hoe bepalen pathologen de Nottingham-graad voor invasief lobulair carcinoom?
De graad kan pas worden bepaald nadat de tumor onder de microscoop is onderzocht. Bij het onderzoeken van de tumor letten pathologen op de volgende drie microscopische kenmerken:
- Buisje – Een tubulus is een groep cellen die met elkaar zijn verbonden om een ronde, ringachtige structuur te vormen. Tubuli lijken op elkaar, maar zijn niet hetzelfde als de tubuli klieren die normaal in de borst worden aangetroffen. Een score van 1 tot 3 wordt gegeven op basis van het percentage kankercellen dat tubuli vormt. Tumoren die voornamelijk uit tubuli bestaan, krijgen een score van 1, terwijl tumoren die uit zeer weinig klieren bestaan, een score van 3 krijgen. De cellen bij invasief lobulair carcinoom vormen geen klieren en krijgen altijd een score van 3 voor dit kenmerk.
- Nucleair pleomorfisme - The kern is een deel van de cel dat het grootste deel van het genetische materiaal (DNA) van de cel bevat. Pleomorfisme (of pleomorf) is een woord dat pathologen gebruiken wanneer de kern van een tumorcel er heel anders uitziet dan de kern van een andere tumorcel. Voor nucleair pleomorfisme wordt een score van 1 tot 3 gegeven. Wanneer de meeste kankercellen klein zijn en erg op elkaar lijken, krijgt de tumor een score van 1. Wanneer de kankercellen erg groot zijn en er abnormaal uitzien, krijgt de tumor een score van 3.
- Mitotische snelheid – Cellen delen zich om nieuwe cellen te creëren. Het proces van het maken van een nieuwe cel wordt genoemd mitosis, en een cel die aan het delen is heet a mitotische figuur. Uw patholoog telt het aantal mitotische figuren in een bepaald gebied (een high-powered field genoemd) en gebruikt dat aantal om een score tussen 1 en 3 te geven. Tumoren met zeer weinig mitotische figuren krijgen een score van 1, terwijl die met veel mitotische figuren krijgen een score van 3.
De score van elke categorie wordt als volgt opgeteld om het totaalcijfer te bepalen:
- Grade 1 (lage score) – Score van 3, 4 of 5.
- Graad 2 (hoog cijfer) – Score van 6 of 7.
- Graad 3 (hoog cijfer) – Score van 8 of 9.
Waarom is de grootte van de tumor belangrijk?
De grootte van een borsttumor is belangrijk omdat deze wordt gebruikt om het pathologische tumorstadium (pT) te bepalen en omdat grotere tumoren een grotere kans hebben om uit te zaaien (uitzaaien) naar lymfeklieren en andere delen van het lichaam. De tumorgrootte kan pas worden bepaald nadat de gehele tumor is verwijderd. Om deze reden wordt het niet opgenomen in uw pathologierapport na a biopsie.
Wat zijn borstprognostische markers en waarom zijn ze belangrijk?
Prognostische markers zijn eiwitten of andere biologische elementen die kunnen worden gemeten om te helpen voorspellen hoe een ziekte zoals kanker zich in de loop van de tijd zal gedragen en hoe deze op de behandeling zal reageren. De meest geteste prognostische markers in de borst zijn de hormoonreceptoren oestrogeenreceptor (ER) en progesteron receptor (PR) en de groeifactor HER2.
Hormoonreceptoren – ER en PR
ER en PR zijn hormoonreceptoren waarmee cellen kunnen reageren op de werking van de geslachtshormonen oestrogeen en progesteron. ER en PR worden gemaakt door normale borstcellen en door sommige borstkankers. Kankers die ER en PR aanmaken worden beschreven als 'hormoongevoelig' omdat ze afhankelijk zijn van deze hormonen om te groeien.
Pathologen voeren vaak een test uit genaamd immunohistochemie om te zien of de cellen in de tumor bij invasief lobulair carcinoom ER en PR maken. Deze test wordt vaak uitgevoerd op de biopsie steekproef. In sommige situaties mag het echter pas worden uitgevoerd nadat de hele tumor is verwijderd.
Pathologen bepalen de ER- en PR-score door het percentage tumorcellen te meten dat eiwit heeft in een deel van de cel dat de kern en de intensiteit van de vlek. De meeste rapporten geven een bereik voor het percentage cellen dat nucleaire positiviteit vertoont, terwijl de intensiteit wordt beschreven als zwak, matig of hoog.
HER2
HER2 is een eiwit dat wordt gemaakt door normale, gezonde cellen in het hele lichaam. De tumorcellen bij sommige vormen van kanker maken extra HER2 aan en hierdoor kunnen de cellen in de tumor sneller groeien dan normale cellen.
Er worden gewoonlijk twee tests uitgevoerd om de hoeveelheid HER2 bij invasief lobulair carcinoom te meten. De eerste test wordt genoemd immunohistochemie en het stelt uw patholoog in staat om het HER2-eiwit op het oppervlak van de cel te zien. Deze test krijgt een score van 0 tot en met 3.
HER2-immunohistochemiescore:
- Negatief (0 en 1) – Een score van 0 of 1 betekent dat de tumorcellen geen extra HER2-eiwit maken.
- dubbelzinnig (2) – Een score van 2 betekent dat de cellen mogelijk extra HER2-eiwit aanmaken en een andere test genaamd fluorescentie in situ hybridisatie (zie hieronder) moet worden uitgevoerd om de resultaten te bevestigen.
- Positief (3) – Een score van 3 betekent dat de cellen extra HER2-eiwit maken.
De tweede test die wordt gebruikt om HER2 te meten heet fluorescentie in situ hybridisatie (FISH). Deze test wordt meestal pas uitgevoerd na een score van 2 op de immunohistochemische test. In plaats van naar HER2 aan de buitenkant van de cel te zoeken, gebruikt FISH een sonde die zich aan het HER2-gen in de celkern hecht. Normale cellen hebben 2 kopieën van het HER2-gen in de kern van de cel. Het doel van de HER FISH-test is om tumorcellen te identificeren die meer kopieën van het HER2-gen hebben, waardoor ze meer kopieën van het HER2-eiwit kunnen maken.
HER2 FISH-score:
- Positief (versterkt) – De tumorcellen hebben extra kopieën van het HER2-gen. Deze cellen maken hoogstwaarschijnlijk extra HER2-eiwit aan.
- Negatief (niet versterkt) – De tumorcellen hebben geen extra kopieën van het HER2-gen. Deze cellen maken hoogstwaarschijnlijk geen extra HER2-eiwit aan.
Wat is lobulair carcinoom in situ en hoe is het gerelateerd aan invasief lobulair carcinoom?
Lobulair carcinoom in situ (LCIS) is een niet-invasieve tumor die ontstaat vóór de ontwikkeling van invasief lobulair carcinoom. Omdat LCIS leidt tot invasief lobulair carcinoom, is het gebruikelijk dat pathologen LCIS en invasief lobulair carcinoom in hetzelfde weefsel aantreffen.
Wat betekent tumorextensie en waarom is het belangrijk?
Invasief lobulair carcinoom begint in de borst, maar de tumor kan zich uitbreiden naar de bovenliggende huid of de spieren van de borstwand. De term tumorextensie wordt gebruikt wanneer tumorcellen worden gevonden in de huid of de spieren onder de borst. Tumorverlenging is belangrijk omdat het gepaard gaat met een hoger risico dat de tumor na de behandeling teruggroeit (plaatselijk recidief) of dat kankercellen naar een verre lichaamsplaats zoals de long gaan. Tumorextensie wordt ook gebruikt om het pathologische tumorstadium (pT) te bepalen.
Wat is lymfovasculaire invasie en waarom is het belangrijk?
Lymfovasculaire invasie betekent dat kankercellen werden gezien in een bloedvat of lymfevat. Bloedvaten zijn lange dunne buizen die bloed door het lichaam vervoeren. Lymfevaten zijn vergelijkbaar met kleine bloedvaten, behalve dat ze een vloeistof vervoeren die lymfe wordt genoemd in plaats van bloed. De lymfevaten verbinden zich met kleine immuunorganen genaamd lymfeklieren die door het hele lichaam voorkomen. Lymfovasculaire invasie is belangrijk omdat kankercellen bloedvaten of lymfevaten kunnen gebruiken om zich naar andere delen van het lichaam te verspreiden, zoals lymfeklieren of de longen.

Wat zijn lymfeklieren en waarom zijn ze belangrijk?
Lymfeklieren zijn kleine immuunorganen die door het hele lichaam worden aangetroffen. Kankercellen kunnen zich van een tumor naar de lymfeklieren verspreiden via kleine bloedvaten die lymfevaten worden genoemd. Om deze reden worden lymfeklieren vaak verwijderd en onder een microscoop onderzocht om naar kankercellen te zoeken. De verplaatsing van kankercellen van de tumor naar een ander deel van het lichaam, zoals een lymfeklier, wordt a . genoemd uitzaaiing.
Kankercellen verspreiden zich meestal eerst naar lymfeklieren dicht bij de tumor, hoewel lymfeklieren ver weg van de tumor ook betrokken kunnen zijn. Om deze reden bevinden de eerste verwijderde lymfeklieren zich meestal dicht bij de tumor. Lymfeklieren verder weg van de tumor worden meestal alleen verwijderd als ze vergroot zijn en er een groot klinisch vermoeden bestaat dat er kankercellen in de lymfeklier zitten.
Als er lymfeklieren uit uw lichaam zijn verwijderd, worden deze onder de microscoop onderzocht door een patholoog en de resultaten van dit onderzoek worden beschreven in uw rapport. De meeste rapporten bevatten het totale aantal onderzochte lymfeklieren, waar in het lichaam de lymfeklieren werden gevonden en het aantal (indien aanwezig) dat kankercellen bevat. Als er kankercellen werden gezien in een lymfeklier, wordt ook de grootte van de grootste groep kankercellen (vaak beschreven als "focus" of "afzetting") opgenomen.
Het onderzoek van lymfeklieren is om twee redenen belangrijk. Eerst wordt deze informatie gebruikt om het pathologische nodale stadium (pN) te bepalen. Ten tweede verhoogt het vinden van kankercellen in een lymfeklier het risico dat kankercellen in de toekomst in andere delen van het lichaam worden gevonden. Als gevolg hiervan zal uw arts deze informatie gebruiken bij de beslissing of aanvullende behandeling zoals chemotherapie, bestralingstherapie of immunotherapie nodig is.
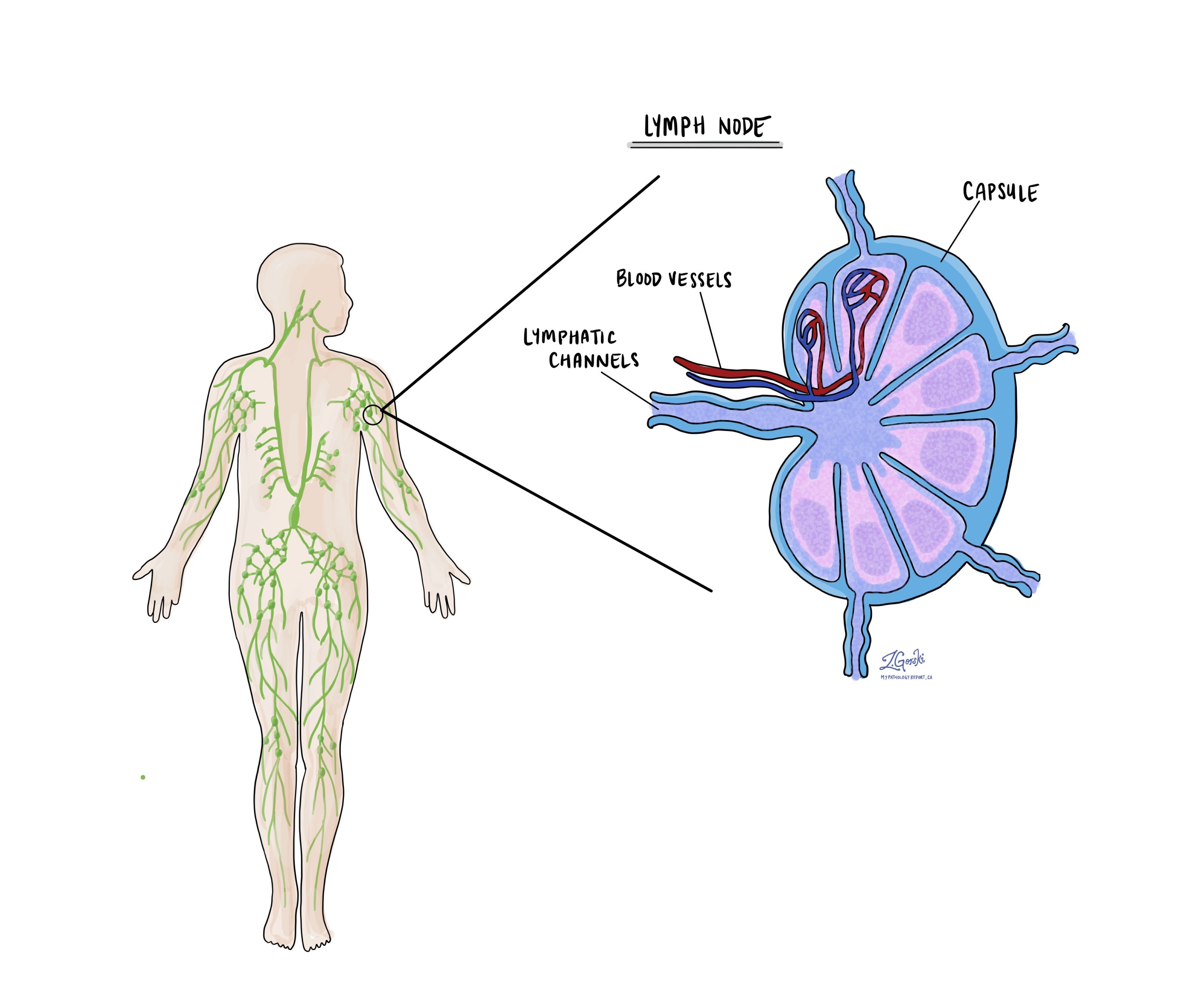
Wat betekent het als een lymfeklier als positief wordt beschreven?
Pathologen gebruiken de term 'positief' vaak om een lymfeklier die kankercellen bevat. Een lymfeklier die kankercellen bevat, kan bijvoorbeeld 'positief voor maligniteit' of 'positief voor uitgezaaid carcinoom' worden genoemd.
Wat betekent het als een lymfeklier als negatief wordt beschreven?
Pathologen gebruiken vaak de term 'negatief' om een lymfeklier die geen kankercellen bevat. Een lymfeklier die geen kankercellen bevat, kan bijvoorbeeld "negatief voor maligniteit" of "negatief voor gemetastaseerd carcinoom" worden genoemd.
Wat zijn geïsoleerde tumorcellen (ITC's)?
Pathologen gebruiken de term 'geïsoleerde tumorcellen' om een groep tumorcellen te beschrijven die 0.2 mm of kleiner is en wordt aangetroffen in een lymfeklier. Lymfeklieren met alleen geïsoleerde tumorcellen (ITC's) worden voor het pathologische nodale stadium (pN) niet als 'positief' geteld.
Wat is een micrometastase?
Een 'micrometastase' is een groep tumorcellen die van 0.2 mm tot 2 mm groot is en wordt aangetroffen in a lymfeklier. Als in alle onderzochte lymfeklieren alleen micrometastasen worden gevonden, is het pathologische nodale stadium pN1mi.
Wat is een macrometastase?
Een 'macrometastase' is een groep tumorcellen die groter is dan 2 mm en wordt aangetroffen in a lymfeklier. Macrometastasen zijn geassocieerd met een slechtere prognose en kan een aanvullende behandeling nodig zijn.
Wat is een schildwachtklier?
A schildwachtklier is de eerste lymfeklier in de keten van lymfeklieren die vloeistof uit de borst afvoert. Het wordt meestal gevonden in de oksel (de oksel). Als kanker in de oksel wordt gevonden, wordt deze meestal eerst in de schildwachtklier gevonden.
Wat is een niet-schildwachtklier axillaire lymfeklier?
Een niet-schildwacht oksel lymfeklier bevindt zich na de schildwachtklier in de oksel (oksel). Kankercellen verspreiden zich meestal naar deze lymfeklieren nadat ze door de schildwachtklier zijn gepasseerd.
Wat betekent extranodale extensie?
Alle lymfeklieren zijn omgeven door een dunne laag weefsel die een capsule wordt genoemd. Extranodale extensie betekent dat kankercellen in de lymfeklier door het kapsel zijn gebroken en zich hebben verspreid in het weefsel buiten de lymfeklier. Extranodale extensie is belangrijk omdat het het risico vergroot dat de tumor na de operatie op dezelfde locatie teruggroeit. Voor sommige vormen van kanker is extranodale extensie ook een reden om aanvullende behandeling te overwegen, zoals chemotherapie of bestraling.
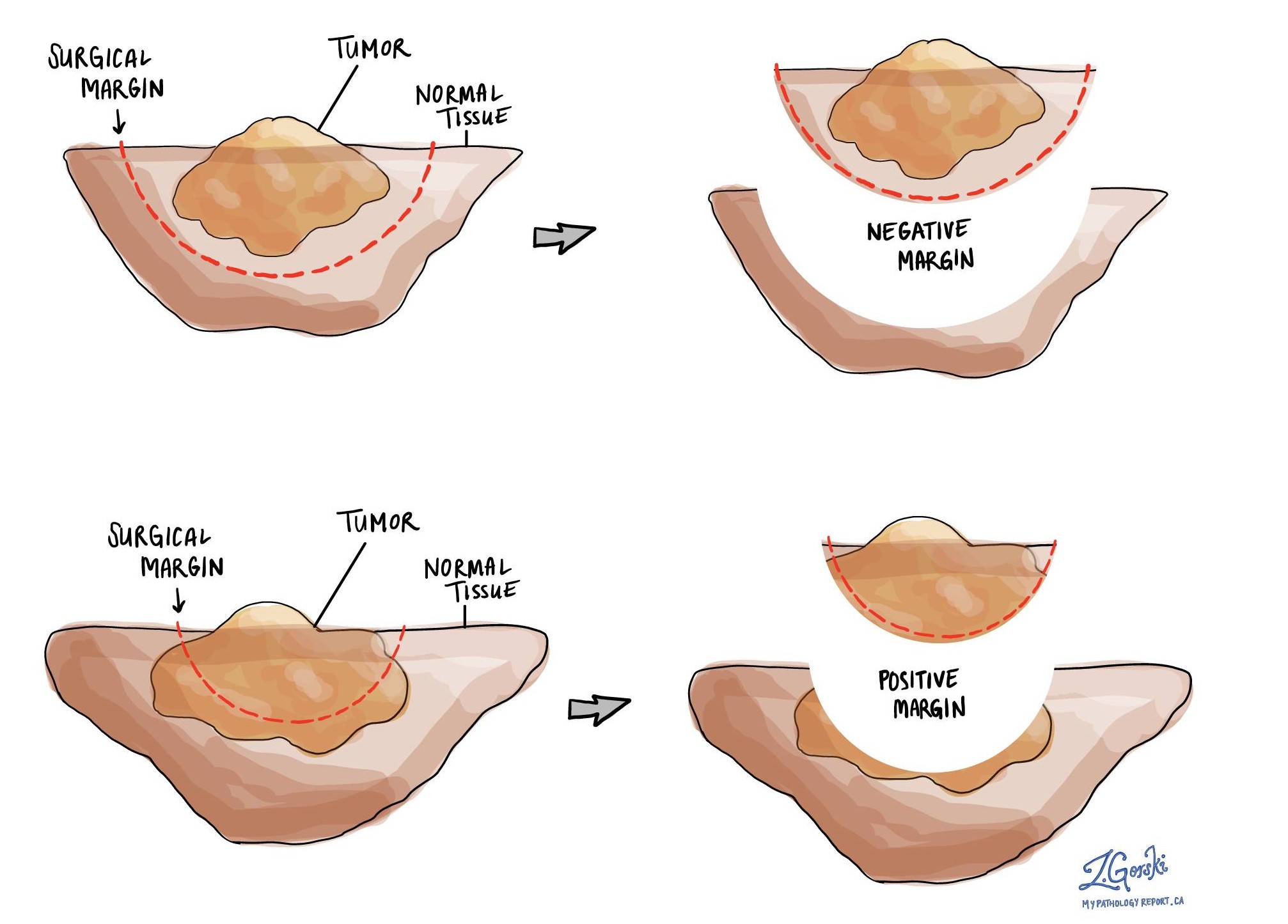
Wat is een marge en waarom zijn marges belangrijk?
In de pathologie is een marge de rand van een weefsel dat wordt gesneden bij het verwijderen van een tumor uit het lichaam. De marges die in een pathologierapport worden beschreven, zijn erg belangrijk omdat ze je vertellen of de hele tumor is verwijderd of dat er een deel van de tumor is achtergebleven. De margestatus bepaalt welke (eventuele) aanvullende behandeling u nodig heeft.
De meeste pathologierapporten beschrijven alleen marges na een chirurgische ingreep genaamd an uitsnijding or resectie uitgevoerd om de gehele tumor te verwijderen. Om deze reden worden marges meestal niet beschreven na een procedure die a wordt genoemd biopsie wordt uitgevoerd om slechts een deel van de tumor te verwijderen. Het aantal marges dat in een pathologierapport wordt beschreven, is afhankelijk van het soort weefsel dat wordt verwijderd en de locatie van de tumor. De grootte van de marge (de hoeveelheid normaal weefsel tussen de tumor en de snijrand) is afhankelijk van het type tumor dat wordt verwijderd en de locatie van de tumor.
Pathologen onderzoeken zorgvuldig de marges om te zoeken naar tumorcellen aan de snijrand van het weefsel. Als er tumorcellen worden gezien aan de snijrand van het weefsel, wordt de marge als positief beschreven. Als er geen tumorcellen worden gezien aan de snijrand van het weefsel, wordt een marge als negatief beschreven. Zelfs als alle marges negatief zijn, zullen sommige pathologierapporten ook een meting geven van de tumorcellen die zich het dichtst bij de snijrand van het weefsel bevinden.
Een positieve (of zeer nauwe) marge is belangrijk omdat dit betekent dat er tumorcellen in uw lichaam kunnen zijn achtergebleven toen de tumor operatief werd verwijderd. Om deze reden kan aan patiënten met een positieve marge een andere operatie worden aangeboden om de rest van de tumor te verwijderen of bestralingstherapie naar het deel van het lichaam met de positieve marge. De beslissing om aanvullende behandeling aan te bieden en het soort behandelingsopties dat wordt aangeboden, hangt af van een aantal factoren, waaronder het type tumor dat is verwijderd en het betrokken lichaamsgebied. Een aanvullende behandeling is bijvoorbeeld misschien niet nodig voor een goedaardig (niet-kankerachtig) type tumor, maar kan sterk worden aanbevolen voor a kwaadaardig (kanker) type tumor.
Wat betekent behandeleffect?
Als u een behandeling (chemotherapie of bestralingstherapie) heeft ondergaan voordat de tumor werd verwijderd, zal uw patholoog al het ingezonden weefsel onderzoeken om te zien hoeveel van de tumor nog in leven is (levensvatbaar). Lymfeklieren met kankercellen zal ook worden onderzocht op behandeleffecten. Een groter behandelingseffect (geen of zeer weinig resterende levensvatbare tumorcellen) wordt geassocieerd met een betere ziektevrije en algehele overleving.
Over dit artikel
Dit artikel is geschreven door artsen om u te helpen uw pathologierapport te lezen en te begrijpen. Contact als u vragen heeft over dit artikel of uw pathologierapport. Lezen dit artikel voor een meer algemene inleiding tot de onderdelen van een typisch pathologierapport.


