door Jason Wasserman MD PhD FRCPC
14 december 2023
Plaveiselcelcarcinoom (SCC), ook wel invasief plaveiselcelcarcinoom genoemd, is de meest voorkomende vorm van baarmoederhalskanker. De tumor begint vanaf plaveiselcellen normaal te vinden in de epitheel op het buitenoppervlak van de hals.
SCC van de baarmoederhals kan keratiniserend (KSCC), niet-keratiniserend (NKSCC) of basaloïde zijn. Keratiniseren betekent dat de tumorcellen een eiwit aanmaken dat keratine wordt genoemd. Niet-keratiniserend betekent dat de tumorcellen geen keratine aanmaken. Basaloïde betekent dat de tumorcellen lijken op de basale cellen die normaal aan de basis van het epitheel worden aangetroffen. Ondanks deze verschillen vertonen alle drie de subtypen vergelijkbaar gedrag prognose.
Wat veroorzaakt plaveiselcelcarcinoom in de baarmoederhals?
De meest voorkomende oorzaak van SCC van de baarmoederhals is een infectie met een seksueel overdraagbaar virus humaan papillomavirus (HPV). Het virus infecteert cellen in een gebied van de baarmoederhals dat de baarmoederhals wordt genoemd transformatie zone. HPV is onderverdeeld in typen en twaalf typen (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 en 59) zijn verantwoordelijk voor meer dan 90% van alle gevallen van SCC in de baarmoederhals. Tumoren veroorzaakt door HPV worden HPV-geassocieerd genoemd, tumoren die dat niet zijn, worden HPV-onafhankelijk genoemd.
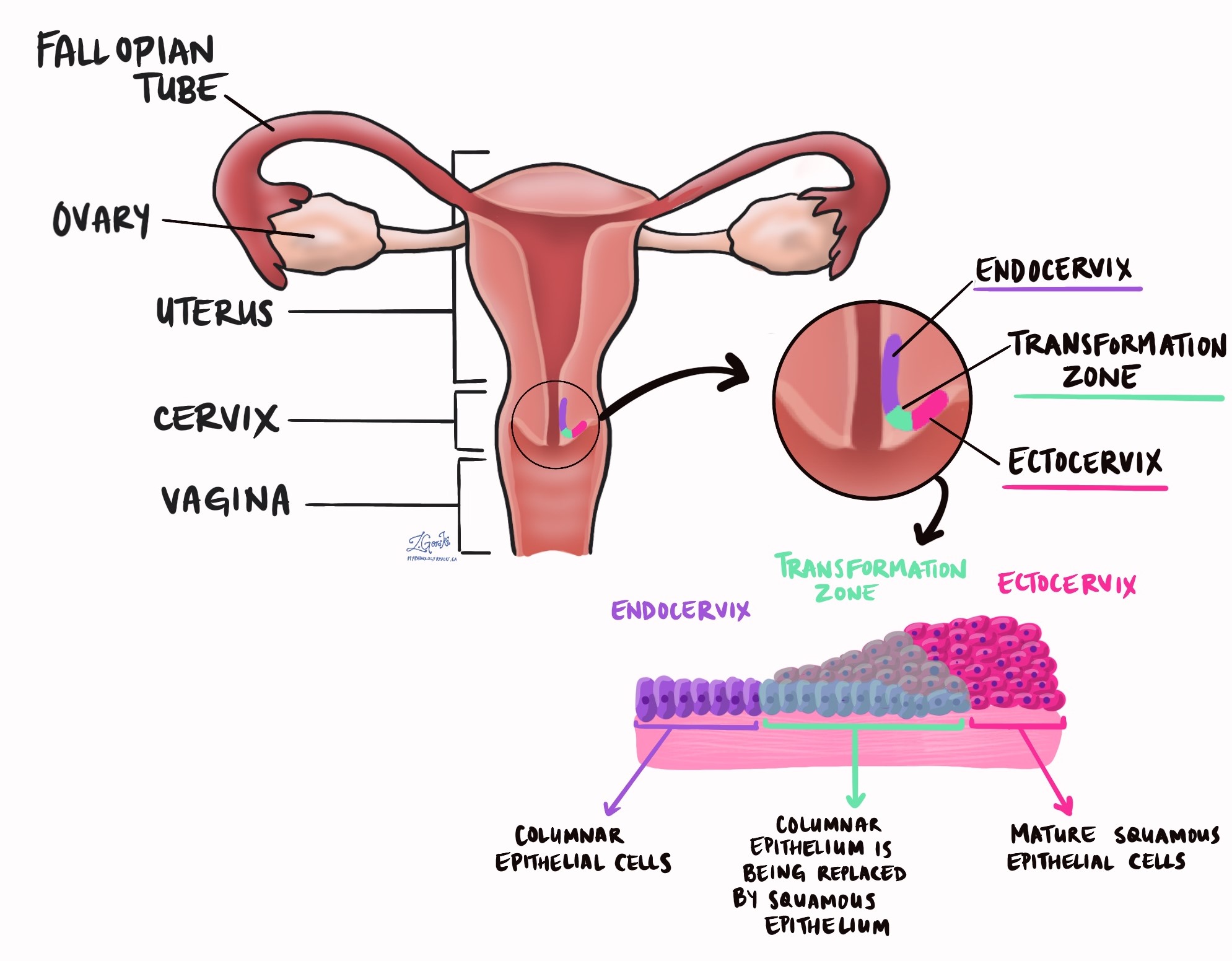
Wat zijn de symptomen van plaveiselcelcarcinoom van de baarmoederhals?
Kleine tumoren veroorzaken doorgaans geen symptomen en de tumor wordt ontdekt wanneer een screening-uitstrijkje wordt uitgevoerd. Symptomen geassocieerd met grotere tumoren zijn onder meer abnormale vaginale bloedingen, afscheiding en pijn.
Uw pathologierapport voor plaveiselcelcarcinoom van de baarmoederhals
De informatie in uw pathologierapport voor SCC van de baarmoederhals is afhankelijk van de uitgevoerde procedure. Voor kleine ingrepen zoals a Pap uitstrijkje, mag uw rapport alleen de diagnose bevatten. A biopsie rapport kan ook de tumor omvatten graad en immunohistochemie kan worden uitgevoerd om naar te zoeken p16 in de tumorcellen. Voor grotere procedures zoals een uitsnijding or resectie uitgevoerd om de gehele tumor te verwijderen, aanvullende informatie zoals de grootte van de tumor, de diepte van de invasie en de beoordeling van marges mag ook beschreven worden. Zie de onderstaande secties voor meer details.
Wat betekent het als plaveiselcelcarcinoom van de cervix ook, matig of slecht gedifferentieerd wordt beschreven?
Pathologen verdelen SCC van de baarmoederhals in drie graden – goed, matig en slecht gedifferentieerd – op basis van de mate waarin de tumorcellen er normaal uitzien plaveiselcellen wanneer het onder de microscoop wordt onderzocht. De graad is belangrijk omdat tumoren van hogere kwaliteit (bijvoorbeeld slecht gedifferentieerde tumoren) zich agressiever gedragen en vaker uitzaaien (verspreid) naar andere delen van het lichaam.
SCC van de baarmoederhals wordt als volgt beoordeeld:
- Goed gedifferentieerde SCC van de baarmoederhals (graad 1) – Goed gedifferentieerde SCC van de baarmoederhals bestaat uit tumorcellen die er bijna hetzelfde uitzien als normale plaveiselcellen.
- Matig gedifferentieerde SCC van de baarmoederhals (graad 2) – Matig gedifferentieerde SCC van de baarmoederhals bestaat uit tumorcellen die er anders uitzien dan normale plaveiselcellen, maar die nog steeds als plaveiselcellen kunnen worden herkend.
- Slecht gedifferentieerde SCC van de baarmoederhals (graad 3) – Slecht gedifferentieerde SCC van de baarmoederhals bestaat uit tumorcellen die weinig op normale plaveiselcellen lijken. Deze cellen kunnen er zo abnormaal uitzien dat uw patholoog mogelijk een aanvullende test moet bestellen, zoals: immunohistochemie om de diagnose te bevestigen. Deze tumoren hebben de neiging zich zeer agressief te gedragen en gaan gepaard met erger prognose vergeleken met goed en matig gedifferentieerde tumoren.
Hoe bepalen pathologen de tumorgrootte bij plaveiselcelcarcinoom van de baarmoederhals en waarom is dit belangrijk?
Nadat de tumor operatief is verwijderd, wordt deze in drie dimensies gemeten: lengte, breedte en invasiediepte. Tumoren met een invasiediepte groter dan 5 mm en een breedte groter dan 7 mm lijken daar meer op uitzaaien (verspreid) naar andere delen van het lichaam, zoals lymfeklieren. Deze metingen worden ook gebruikt om het pathologische tumorstadium (pT) te bepalen.
- Lengte – De tumor wordt van boven naar beneden gemeten.
- Breedte – De tumor wordt van links naar rechts gemeten.
- Diepte van invasie – De tumor wordt gemeten vanaf de epitheel op het oppervlak van de baarmoederhals naar de kankercellen op het diepste punt van invasie.
Wat betekent tumorextensie en waarom is het belangrijk?
Tumoruitbreiding beschrijft de afstand die de kankercellen hebben verspreid vanaf de plaats waar de tumor begon hals. Grote tumoren kunnen voorbij de baarmoederhals groeien en omliggende organen en weefsels omvatten, zoals het parametrium, het endometrium, de vagina, de blaas en het rectum. Als een van deze weefsels wordt verwijderd, worden deze zorgvuldig onderzocht op kankercellen.
Uw patholoog kan de mate van tumoruitbreiding pas bepalen nadat de gehele tumor is verwijderd. Het wordt niet beschreven in uw rapport na a Pap uitstrijkje of biopsie. Tumoruitbreiding naar het parametrium of andere organen rond de baarmoederhals gaat gepaard met een slechtere prognose en wordt gebruikt om het pathologische tumorstadium (pT) te bepalen.
Wat betekent stromale invasie en waarom is het belangrijk?
Het weefsel dat de binnenkant van de baarmoederhals bedekt, wordt de epitheel terwijl het weefsel net onder het epitheel de stroma. SCC van de baarmoederhals begint in het epitheel, maar naarmate de tumor groeit, verspreiden de cellen zich naar het stroma. Dit wordt stromaal genoemd invasie. De hoeveelheid stromale invasie is niet hetzelfde als de tumorgrootte, omdat de tumorgrootte ook alle eventuele invasies omvat HSIL dat kan zich boven het invasiegebied bevinden. Om die reden kan de omvang van de tumor groter zijn dan de hoeveelheid stroma-invasie.
De meeste pathologierapporten beschrijven de mate van stromale invasie in twee richtingen:
- Diepte van invasie – Dit is de hoeveelheid invasie gemeten vanaf het oppervlak van de tumor tot het diepste punt van invasie.
- Horizontale omvang van invasie – Dit is de hoeveelheid invasie gemeten van de ene kant van de tumor naar de andere.
De hoeveelheid stromale invasie is belangrijk omdat deze wordt gebruikt om het pathologische tumorstadium (pT) te bepalen. Over het algemeen wordt minder stromale invasie geassocieerd met een betere prognose terwijl meer invasie wordt geassocieerd met een slechtere prognose.
Wat betekent lymfovasculaire invasie en waarom is het belangrijk?
Lymfovasculaire invasie betekent dat kankercellen worden aangetroffen in een bloed- of lymfevatenvat. Bloedvaten zijn lange dunne buisjes die bloed door het lichaam transporteren. Lymfatische vaten lijken op kleine bloedvaten, behalve dat ze een vloeistof bevatten die lymfe wordt genoemd in plaats van bloed. De lymfevaten verbinden zich met kleine immuunorganen, genaamd lymfeklieren die door het hele lichaam voorkomen. Lymfovasculaire invasie is belangrijk omdat kankercellen bloedvaten of lymfevaten kunnen gebruiken om zich naar andere delen van het lichaam te verspreiden, zoals lymfeklieren of de longen. Als lymfovasculaire invasie wordt gezien, wordt dit in uw rapport opgenomen.

Wat is een marge en waarom zijn marges belangrijk?
A marge is elk weefsel dat door de chirurg moet worden weggesneden om de tumor uit uw lichaam te verwijderen. Als u een chirurgische ingreep heeft ondergaan om de hele tumor uit uw lichaam te verwijderen, zal uw patholoog de marge nauwkeurig onderzoeken om er zeker van te zijn dat er geen kankercellen aan de snijrand van het weefsel zitten.
Een marge wordt negatief genoemd als er geen kankercellen aan de snijrand van het weefsel zijn. Daarentegen wordt een marge als positief beschouwd wanneer de kankercellen aan de rand van het gesneden weefsel worden gezien. Als HSIL wordt gezien in de marge die ook in uw rapport zal worden beschreven. Het vinden van kankercellen in de marge verhoogt het risico dat de tumor op die locatie teruggroeit.
Het aantal en type marges dat in uw rapport wordt beschreven, is afhankelijk van het type procedure dat wordt uitgevoerd om de tumor uit uw lichaam te verwijderen. Pap-uitstrijkjes hebben geen marges.
Gemeenschappelijke marges zijn onder meer:
- Endocervicale marge - Dit is waar de baarmoederhals de binnenkant van de baarmoeder ontmoet.
- Ectocervicale marge – Dit is de onderkant van de baarmoederhals, het dichtst bij de vagina.
- Diepe marge – Dit is het weefsel in de wand van de baarmoederhals.
- radiale marge - Dit is het zachte weefsel dat de baarmoederhals omringt. De radiale marge wordt alleen in uw rapport beschreven als u tegelijkertijd uw gehele baarmoederhals en baarmoeder heeft laten verwijderen.

Wat zijn lymfeklieren en waarom zijn ze belangrijk?
Lymfeklieren zijn kleine immuunorganen die door het hele lichaam worden aangetroffen. Kankercellen kunnen zich van een tumor naar de lymfeklieren verspreiden via kleine bloedvaten die lymfevaten worden genoemd. Lymfeklieren worden niet altijd tegelijk met de tumor verwijderd. Wanneer lymfeklieren echter worden verwijderd, worden ze onder een microscoop onderzocht en worden de resultaten beschreven in uw rapport.
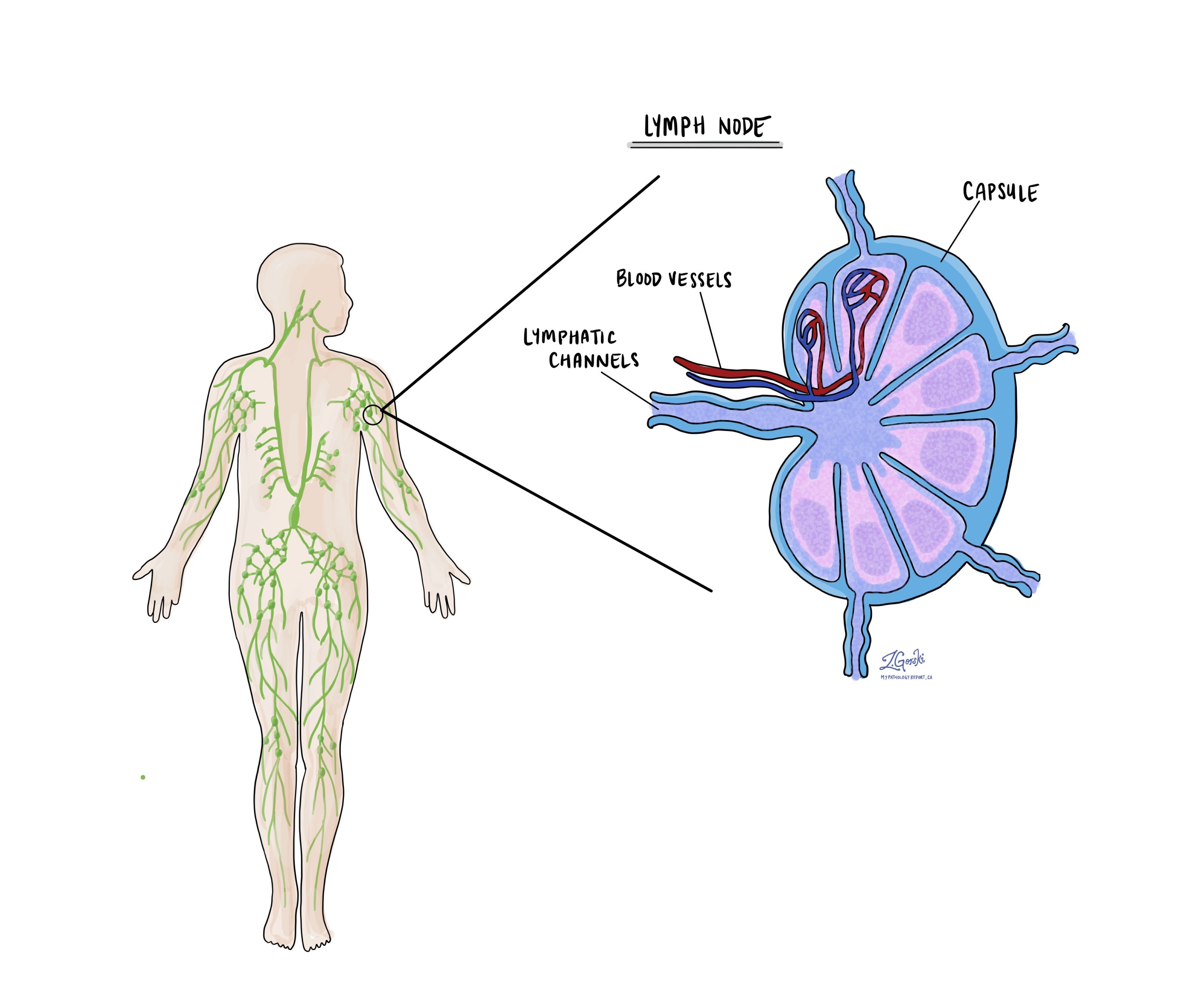
Kankercellen verspreiden zich doorgaans eerst naar lymfeklieren dichtbij de tumor, hoewel ook lymfeklieren ver weg van de tumor betrokken kunnen zijn. Om deze reden bevinden de eerste verwijderde lymfeklieren zich meestal dicht bij de tumor. Lymfeklieren die verder van de tumor verwijderd zijn, worden doorgaans alleen verwijderd als ze vergroot zijn en er een hoog klinisch vermoeden bestaat dat er mogelijk kankercellen in de lymfeklier zitten. De meeste rapporten bevatten het totale aantal onderzochte lymfeklieren, waar in het lichaam de lymfeklieren zijn gevonden en het aantal (indien aanwezig) dat kankercellen bevat. Een groep kankercellen in een lymfeklier wordt een metastase of metastatische afzetting genoemd. Bij plaveiselcelcarcinoom van de baarmoederhals wordt de grootte van de metastase ook als volgt gemeten:
- Geïsoleerde tumorcellen – Het gebied binnen de lymfeklier met kankercellen is minder dan 0.2 millimeter groot.
- Micrometastasen – Het gebied binnen de lymfeklier met kankercellen is meer dan 0.2 millimeter maar kleiner dan 2 millimeter.
- Macrometastasen – Het gebied binnen de lymfeklier met kankercellen is meer dan 2 millimeter groot.
Het onderzoek van lymfeklieren is om twee redenen belangrijk. Ten eerste bepaalt deze informatie het pathologische knooppuntstadium (pN). Ten tweede vergroot het vinden van kankercellen in een lymfeklier het risico dat kankercellen in de toekomst in andere delen van het lichaam worden aangetroffen. Als gevolg hiervan zal uw arts deze informatie gebruiken bij de beslissing of aanvullende behandeling, zoals chemotherapie, bestralingstherapie of immunotherapie, nodig is.
Wat betekent het als een lymfeklier als positief wordt beschreven?
Pathologen gebruiken de term 'positief' vaak om een lymfeklier te beschrijven die kankercellen bevat. Een lymfeklier die kankercellen bevat, kan bijvoorbeeld 'positief voor maligniteit' of 'positief voor uitgezaaid carcinoom' worden genoemd.
Wat betekent het als een lymfeklier als negatief wordt beschreven?
Pathologen gebruiken de term 'negatief' vaak om een lymfeklier te beschrijven die geen kankercellen bevat. Een lymfeklier die geen kankercellen bevat, kan bijvoorbeeld "negatief voor maligniteit" of "negatief voor gemetastaseerd carcinoom" worden genoemd.
Welke informatie wordt gebruikt om het pathologische stadium (pTNM) te bepalen?
Het pathologische stadium voor SCC van de cervix is gebaseerd op het TNM-stadiëringssysteem, een internationaal erkend systeem gecreëerd door de Amerikaans Gemengd Comité voor Kanker. Dit systeem gebruikt informatie over de primaire tumor (T), lymfeklieren (N), en verre metastatische ziekte (M) om het volledige pathologische stadium (pTNM) te bepalen. Uw patholoog onderzoekt het ingeleverde weefsel en geeft elk onderdeel een nummer. Over het algemeen betekent een hoger aantal een meer gevorderde ziekte en een slechtere prognose.
Tumorstadium (pT)
Het pathologische tumorstadium voor SCC van de baarmoederhals is gebaseerd op drie factoren: de hoeveelheid stromale invasie, de grootte van de tumor en de uitbreiding van de tumor naar omliggende organen of weefsels.
- T1a – Tumoren in deze categorie werden pas gevonden nadat het weefsel onder de microscoop was onderzocht. Deze tumoren hebben ook een invasiediepte van 5 millimeter of minder EN en een horizontale spreiding van 7 millimeter of minder.
- T1b – Uw arts heeft de tumor gezien tijdens uw lichamelijk onderzoek OR de diepte van de invasie is groter dan 5 millimeter OR de horizontale spreiding is groter dan 7 millimeter.
- T2a – De tumor breidt zich uit buiten de baarmoeder maar niet in het parametrium.
- T2b – De tumor breidt zich uit tot in het parametrium.
- T3a - De tumor strekt zich uit tot het onderste deel van de vagina.
- T3b – De tumor breidt zich uit tot in de wand van het bekken OR de tumor heeft schade aan de nier veroorzaakt.
- T4 – De tumor breidt zich uit tot in de blaas of het rectum OR de tumor strekt zich uit buiten het bekken in de buik.
Nodale fase (pN)
Het pathologische knooppuntstadium (pN) is gebaseerd op het onderzoek van lymfeklieren op kankercellen.
- NX – Er zijn geen lymfeklieren voor onderzoek naar de pathologie gestuurd.
- N0 – In geen van de onderzochte lymfeklieren zijn kankercellen gevonden.
- N0(i+) – In een lymfeklier werden alleen geïsoleerde kankercellen gevonden.
- N1 – In minimaal één lymfeklier is een groep kankercellen gevonden die groter is dan 0.2 millimeter.
Gemetastaseerd stadium (pM)
SCC krijgt een metastatisch stadium van 0 of 1 op basis van de aanwezigheid van kankercellen op een afgelegen plek in het lichaam (bijvoorbeeld de longen). Het metastatische stadium kan alleen worden vastgesteld als weefsel van een afgelegen locatie wordt aangeboden voor pathologisch onderzoek. Omdat dit weefsel zelden aanwezig is, kan het metastatische stadium niet worden vastgesteld en wordt het vermeld als pMX.
Over dit artikel
Dit artikel is geschreven door artsen om u te helpen uw pathologierapport te lezen en te begrijpen. Contact als u vragen heeft over dit artikel of uw pathologierapport. Lezen dit artikel voor een meer algemene inleiding tot de onderdelen van een typisch pathologierapport.


