por Catherine Forse MD FRCPC e Jason Wasserman MD PhD FRCPC
24 de julho de 2025
O adenocarcinoma do esôfago é um tipo de câncer que se desenvolve a partir de células formadoras de glândulas em uma área de tecido anormal chamada metaplasia intestinal. Essas células normalmente não são encontradas no esôfago, mas podem aparecer quando o revestimento do esôfago é repetidamente exposto ao ácido estomacal.
Este câncer quase sempre se inicia na parte inferior do esôfago, próximo à junção com o estômago (chamada junção esofagogástrica). Também pode se estender para a parte superior do estômago. Menos comumente, o adenocarcinoma pode ocorrer no esôfago médio ou superior, especialmente em áreas onde pequenas manchas de células glandulares estão presentes.
Quais são os sintomas do adenocarcinoma do esôfago?
Os sintomas do adenocarcinoma esofágico geralmente incluem dificuldade para engolir (disfagia), azia ou refluxo ácido, perda de peso, dor no peito ou abdominal, náuseas ou vômitos. Em alguns casos, o câncer é descoberto durante a investigação de anemia ou após exames de imagem.
O que causa o adenocarcinoma do esôfago?
A maioria dos casos de adenocarcinoma do esôfago se desenvolve em pessoas com uma condição chamada Esôfago de Barrett. Essa condição é causada pela doença do refluxo gastroesofágico (DRGE) de longa data, que permite que o ácido e a bile do estômago danifiquem o revestimento do esôfago ao longo do tempo.
No esôfago de Barrett o normal células escamosas que revestem o esôfago são substituídos por células glandulares que se assemelham às encontradas nos intestinos. Esse tipo de alteração é chamado de metaplasia intestinal.
Com o tempo, essas células glandulares anormais podem adquirir alterações adicionais e progredir para displasia, que é uma condição pré-cancerosa. Se não tratada, a displasia pode levar ao desenvolvimento de adenocarcinoma invasivo.
No esôfago, a displasia é classificada em dois tipos principais:
-
Displasia de baixo grau: as células parecem anormais, mas ainda estão parcialmente organizadas. Esse tipo de displasia apresenta menor risco de evoluir para câncer, mas monitoramento ou tratamento cuidadoso costuma ser recomendado.
-
Displasia de alto grau: As células parecem muito anormais e desorganizadas. A displasia de alto grau tem um risco muito maior de se transformar em adenocarcinoma e frequentemente se localiza ao lado ou mesmo dentro de pequenas áreas de câncer.
Seu laudo patológico pode mencionar displasia, caso tenha sido observada na amostra de tecido. Se houver displasia de alto grau associada ao adenocarcinoma, isso sugere que o câncer provavelmente se desenvolveu a partir de uma área preexistente do esôfago de Barrett. No entanto, em alguns casos, especialmente quando o tumor é grande ou profundamente invasivo, qualquer displasia adjacente pode não ser mais visível.
Outros fatores de risco para esse tipo de câncer incluem obesidade, tabagismo, sexo masculino e idade avançada. O câncer é muito mais comum em homens do que em mulheres e ocorre com mais frequência em pessoas com mais de 60 anos.
Como é feito esse diagnóstico?
O diagnóstico de adenocarcinoma de esôfago geralmente é feito após um procedimento chamado endoscopia digestiva alta (ou gastroscopia). Durante esse procedimento, o médico utiliza uma câmera fina e flexível para examinar o interior do esôfago e coletar pequenas amostras de tecido, chamadas de biópsias. Essas amostras são então examinadas ao microscópio por um patologista, que procura células cancerígenas e confirma o diagnóstico.
Se o câncer for encontrado, exames adicionais, como ultrassom endoscópico (EUS), tomografia computadorizada ou tomografia por emissão de pósitrons (PET), podem ser realizados para avaliar o quanto o tumor se espalhou e ajudar a planejar o tratamento.
Como é a aparência do adenocarcinoma no microscópio?
Ao microscópio, o adenocarcinoma é composto por células anormais formadoras de glândulas. Os patologistas podem descrever diferentes padrões, como células tubulares, papilares, mucinosas ou em anel de sinete. O tipo mais comum é o tubular. Esses padrões não são subtipos separados, mas descrevem como as células cancerosas estão organizadas. Em alguns casos, mais de um padrão pode ser observado no mesmo tumor.
If Esôfago de Barrett or displasia estiver presente perto do tumor, isso também pode ser incluído no seu relatório.
Grau de tumor
O grau descreve o quão próximas as células cancerígenas se assemelham às células normais formadoras de glândulas quando observadas ao microscópio. Isso também é chamado de grau histológico. O grau fornece ao médico informações importantes sobre a velocidade de crescimento do tumor e a probabilidade de sua disseminação.
Os patologistas dividem o adenocarcinoma esofágico em três graus:
Grau 1 – Adenocarcinoma bem diferenciado
Nesse tipo de tumor, mais de 95% das células cancerígenas formam glândulas bem organizadas. Esses tumores geralmente crescem mais lentamente e têm menor probabilidade de se espalhar. Este é considerado o grau mais baixo e está associado a um melhor prognóstico.
Grau 2 – Adenocarcinoma moderadamente diferenciado
Em tumores moderadamente diferenciados, entre 50% e 95% das células cancerígenas formam glândulas. Esses tumores apresentam maior variação na aparência e no comportamento das células em comparação com os de grau 1. Eles tendem a crescer mais rápido e têm maior probabilidade de se espalhar do que os tumores bem diferenciados.
Grau 3 – Adenocarcinoma pouco diferenciado ou indiferenciado
Esses tumores formam glândulas em menos de 50% dos casos de câncer. Em alguns casos, não há formação de glândulas. As células parecem muito anormais e se comportam de forma agressiva. Tumores pouco diferenciados e indiferenciados crescem rapidamente e têm maior probabilidade de se espalhar para gânglios linfáticos ou em partes distantes do corpo. São considerados tumores de alto grau e estão associados a um pior prognóstico.
O que significa invasão no adenocarcinoma de esôfago?
Invasão refere-se à profundidade com que o câncer se desenvolveu na parede do esôfago ou nos tecidos circundantes. O adenocarcinoma esofágico se origina a partir de células formadoras de glândulas na mucosa, a camada mais interna do esôfago. À medida que o tumor cresce, ele pode invadir camadas mais profundas do tecido e potencialmente se espalhar para órgãos próximos.
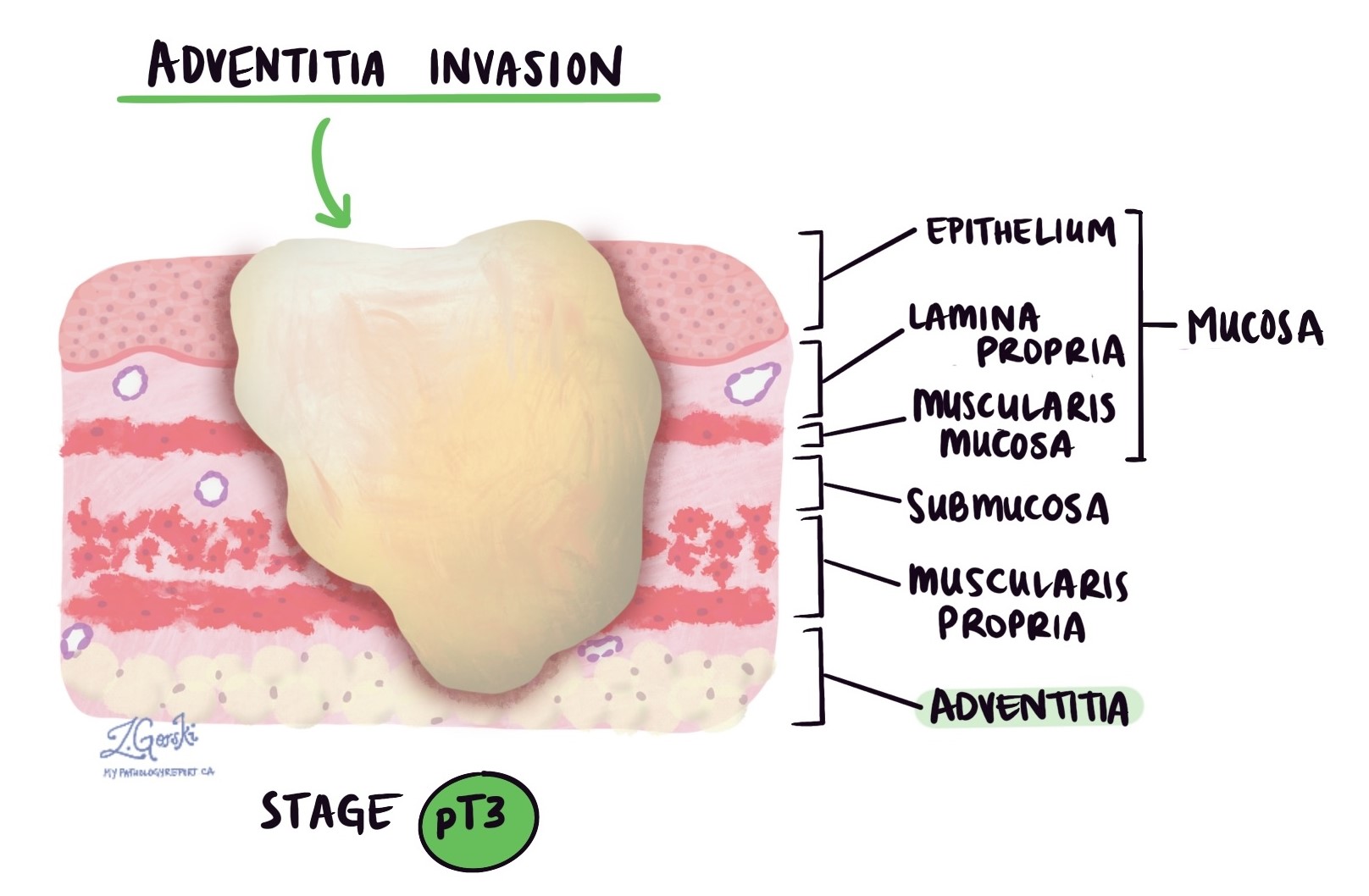
A parede do esôfago é composta por várias camadas distintas:
-
Mucosa – O fino revestimento interno onde o tumor geralmente começa.
-
Submucosa – Uma camada de suporte logo abaixo da mucosa.
-
Muscular própria – Uma espessa camada muscular que ajuda a mover os alimentos através do esôfago.
-
adventícia – Tecido conjuntivo externo que ancora o esôfago no lugar. Ao contrário de outras partes do trato gastrointestinal, o esôfago não possui serosa.
À medida que o tumor cresce, ele pode se espalhar por essas camadas. Em casos mais avançados, pode invadir estruturas próximas, como a traqueia, a aorta ou o pericárdio (tecido ao redor do coração).
Os patologistas examinam cuidadosamente o tumor ao microscópio para encontrar o ponto mais profundo de invasão, que é a camada mais profunda que o tumor atingiu. Esse ponto mais profundo é muito importante porque determina o estadiamento patológico do tumor, também chamado de estadiamento pT, que faz parte do sistema de estadiamento TNM usado para descrever a extensão da disseminação do câncer.
Estadiamento tumoral patológico para adenocarcinoma de esôfago
pT1: O câncer está em estágio inicial e atingiu apenas as camadas internas do esôfago. Essas camadas incluem a lâmina própria, a muscular da mucosa ou a submucosa, que ficam logo abaixo do revestimento superficial (mucosa).
pT1a: O câncer é ainda mais limitado e é encontrado apenas na lâmina própria ou muscular da mucosa — camadas finas logo abaixo da superfície do esôfago.
pT1b: O câncer se aprofundou, atingindo a submucosa, que é a camada de tecido conjuntivo logo abaixo da mucosa.
pT2: O câncer atingiu a muscular própria, uma espessa camada muscular que ajuda a empurrar os alimentos pelo esôfago.
pT3: O câncer cresceu através da camada muscular e atingiu a adventícia, que é o revestimento mais externo do esôfago.
pT4: O câncer se espalhou além da parede do esôfago para órgãos ou estruturas próximas.
pT4a: O câncer está se espalhando para áreas próximas, como a pleura (revestimento que envolve os pulmões), o pericárdio (revestimento que envolve o coração), a veia ázigos, o diafragma ou o peritônio (revestimento do abdômen). Esses tumores ainda podem ser removidos por meio de cirurgia.
pT4b: O câncer se espalhou para estruturas próximas mais críticas, como a aorta (um importante vaso sanguíneo), o corpo vertebral (ossos da coluna vertebral) ou as vias aéreas. Esses tumores geralmente são considerados mais avançados e podem não ser removíveis com cirurgia.
HER2
HER2 (receptor 2 do fator de crescimento epidérmico humano) é uma proteína que ajuda as células a crescer e se dividir. Em alguns tipos de câncer de esôfago, o gene HER2 torna-se hiperativo e produz uma quantidade excessiva da proteína HER2. Isso é chamado de câncer HER2-positivo.
Cânceres de esôfago HER2-positivos tendem a crescer mais rápido e podem ser mais agressivos. No entanto, terapias direcionadas, como o trastuzumabe (Herceptin), podem ser muito eficazes no tratamento desses tipos de câncer. Saber o status HER2 do seu tumor ajuda seus médicos a decidir se esses tratamentos direcionados devem fazer parte do seu plano de tratamento.
Como o HER2 é testado?
Dois testes são comumente usados para verificar o status do HER2:
-
Imuno-histoquímica (IHC) – Mede a quantidade de proteína HER2 na superfície das células cancerígenas.
-
Hibridização in situ fluorescente (FISH) – Mede o número de cópias do gene HER2 nas células cancerígenas.
Imuno-histoquímica (IHQ) HER2
A imunohistoquímica é um exame laboratorial que utiliza colorações especiais para detectar a proteína HER2 na superfície das células tumorais. Os patologistas examinam o tecido corado ao microscópio e atribuem uma pontuação:
-
0 (negativo) – Nenhuma proteína HER2 observada. Este é considerado HER2 negativo, e a terapia direcionada para HER2 geralmente não é eficaz.
-
1+ (negativo) – Coloração fraca ou tênue. Também considerado HER2 negativo.
-
2+ (ambíguo ou limítrofe) – Coloração moderada. O resultado é incerto e um segundo teste (FISH) é necessário.
-
3+ (positivo) – Coloração forte. É HER2-positivo, e os pacientes podem se beneficiar da terapia direcionada ao HER2.
Hibridização in situ por fluorescência HER2 (FISH)
Se o resultado do exame imunohistoquímico (IHQ) for 2+ (duvidoso ou limítrofe), o patologista poderá realizar um teste de FISH para examinar mais de perto o gene HER2 dentro das células tumorais. Este teste utiliza marcadores fluorescentes especiais que brilham sob o microscópio para mostrar quantas cópias do gene HER2 estão presentes.
-
Positivo (amplificado) – Excesso de cópias do gene HER2. O câncer é HER2-positivo e pode responder bem à terapia direcionada ao HER2.
-
Negativo (não amplificado) – Um número normal de cópias do gene HER2. Isso significa que o câncer é HER2-negativo e a terapia direcionada ao HER2 provavelmente não ajudará.
Às vezes, seu relatório pode incluir detalhes adicionais, como a proporção HER2/cromossomo ou o número médio de cópias do gene HER2 por célula. Esses números ajudam a confirmar o status HER2 com mais precisão.
Teste de proteína de reparo de incompatibilidade (MMR)
MMR As proteínas fazem parte do sistema do corpo para corrigir erros de DNA que ocorrem naturalmente durante a divisão celular. As quatro principais proteínas MMR são MLH1, PMS2, MSH2 e MSH6. Se uma ou mais dessas proteínas estiverem ausentes ou não funcionarem corretamente, erros de DNA podem se acumular, levando ao câncer.
Patologistas testam proteínas MMR usando um método chamado imuno-histoquímica (IHQ). Este teste ajuda a determinar se o sistema de reparo de DNA nas células cancerígenas está funcionando normalmente.
o que os resultados significam?
-
Normal (intacto) – Todas as quatro proteínas MMR estão presentes. Isso significa que o tumor é proficiente em MMR e o sistema de reparo de DNA parece normal.
-
Anormal (perda de expressão) – Uma ou mais proteínas MMR estão ausentes. Isso é chamado de deficiência de MMR e tem duas implicações importantes:
-
Seu câncer pode responder melhor à imunoterapia.
-
Você pode ter uma condição genética chamada síndrome de Lynch, que aumenta o risco de vários tipos de câncer. Testes genéticos adicionais podem ser recomendados.
-
Teste PD-L1
PD-L1 é uma proteína que algumas células cancerígenas usam para se esconder do sistema imunológico. Ao produzir PD-L1, essas células evitam ser atacadas pelas células imunológicas. Medicamentos de imunoterapia, chamados inibidores de ponto de controle imunológico, atuam bloqueando esse sinal para que o sistema imunológico possa encontrar e destruir o câncer.
Para verificar se a imunoterapia pode funcionar, os patologistas testam a PD-L1 usando uma pontuação chamada Pontuação Positiva Combinada (CPS). A CPS compara o número de células produtoras de PD-L1 (células cancerígenas e células imunes próximas) com o número total de células tumorais.
o que os resultados significam?
-
Positivo (CPS ≥ 1) – PD-L1 presente. A imunoterapia pode ser uma opção de tratamento eficaz.
-
Negativo (CPS < 1) – Há muito pouco ou nenhum PD-L1 presente. A imunoterapia tem menor probabilidade de funcionar, embora ainda possa ser considerada em algumas situações.
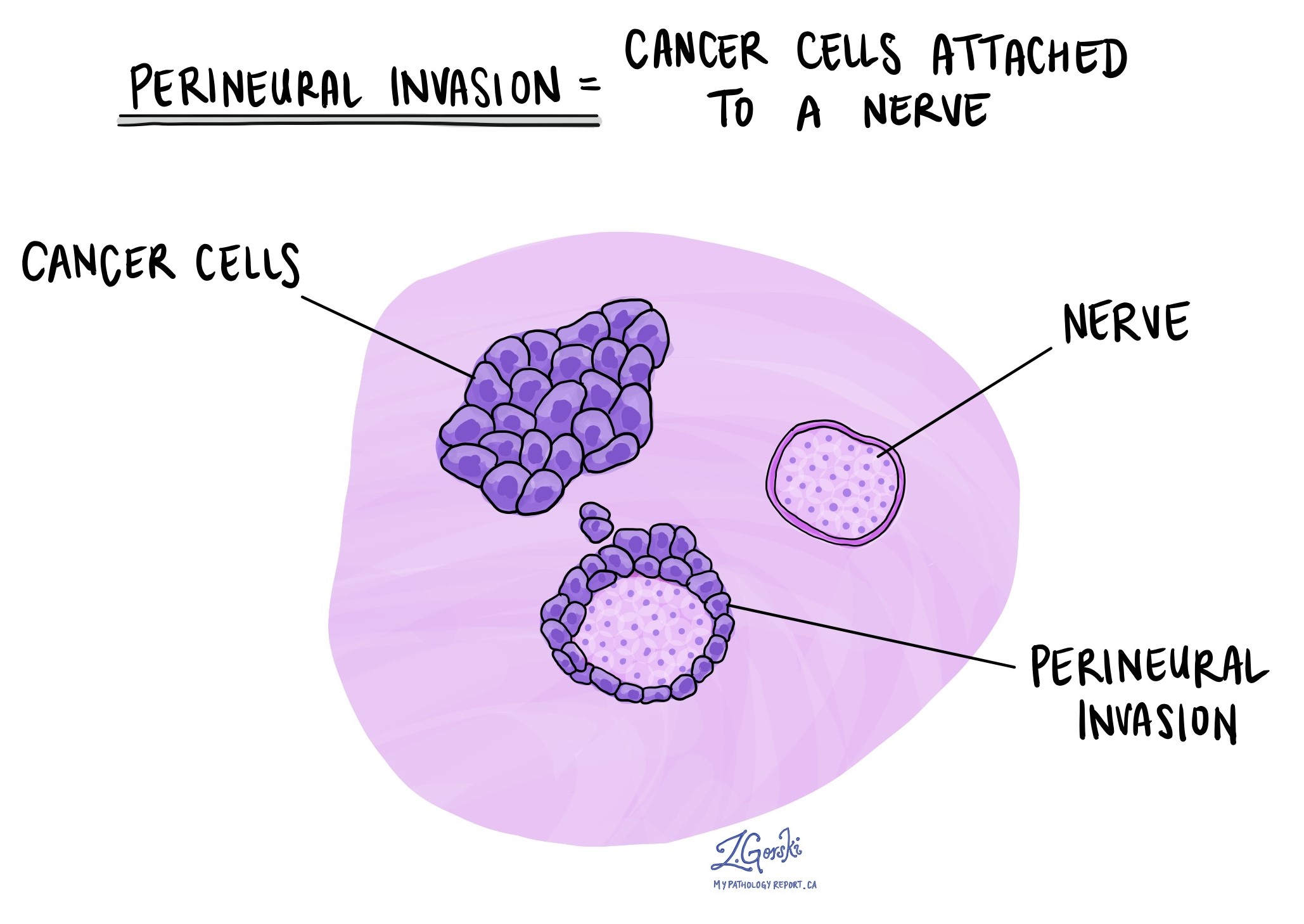
Invasão perineural
Invasão perineural (PNI) significa que células cancerígenas são vistas crescendo ao longo ou ao redor de um nervo. Os nervos são estruturas importantes que transportam sinais entre o cérebro e o resto do corpo. No esôfago, os nervos percorrem o tecido ao redor do tumor.
Patologistas examinam cuidadosamente o tecido ao microscópio para identificar células cancerígenas envolvendo a superfície externa de um nervo ou invadindo o próprio nervo. A presença de PNI é considerada uma característica agressiva, pois indica que o câncer está invadindo estruturas locais e pode ter maior probabilidade de recidiva após o tratamento ou disseminação para outras áreas.
Se PNI for observado, ele será descrito em seu relatório de patologia como "positivo" ou "presente". Se nenhuma invasão perineural for encontrada, o relatório dirá "negativo" ou "ausente".
Invasão linfovascular
Invasão linfovascular (LVI) significa que células cancerígenas entraram em pequenos vasos sanguíneos ou vasos linfáticos próximos ao tumor no esôfago. Os vasos sanguíneos transportam oxigênio e nutrientes de e para os tecidos, enquanto os vasos linfáticos ajudam a drenar fluidos e a transportar células imunológicas. Ambos os tipos de vasos podem fornecer caminhos para as células cancerígenas viajarem para outras partes do corpo.
Ao examinar o tecido ao microscópio, os patologistas procuram aglomerados de células cancerígenas dentro dos espaços de paredes finas que revestem esses vasos. Colorações especiais, chamadas imuno-histoquímica, podem ser usadas para ajudar a confirmar a presença de células tumorais dentro dos vasos.
LVI é um achado importante porque aumenta o risco de disseminação do câncer para os linfonodos ou outros órgãos. Se LVI for observado, será relatado como "presente" ou "positivo". Se não houver câncer nos vasos, o laudo indicará "ausente" ou "negativo". A presença de LVI pode influenciar seu plano de tratamento, como a necessidade de quimioterapia ou radioterapia após a cirurgia.

margens
Na cirurgia do câncer, margens são as bordas do tecido que são cortadas para remover o tumor. Após a remoção do tumor, um patologista examina as margens ao microscópio para verificar se há células cancerígenas presentes nas bordas do tecido.
O objetivo da cirurgia é remover todo o tumor com uma borda de tecido normal ao redor. Se células cancerígenas forem observadas na borda, pode significar que algum câncer permaneceu no corpo. Seu laudo patológico descreverá as margens como:
-
Negativo (claro ou não envolvido) – Não foram encontradas células cancerígenas na borda do tecido. Isso sugere que o tumor foi completamente removido.
-
Positivo (envolvido) – Células cancerígenas estão presentes na borda do tecido. Isso pode significar que o câncer permanece no corpo e pode ser necessário tratamento adicional.
 Dependendo da cirurgia e da localização do tumor, diferentes margens podem ser descritas:
Dependendo da cirurgia e da localização do tumor, diferentes margens podem ser descritas:
-
Margem mucosa (lateral) – Superfície interna do esôfago próxima ao tumor.
-
Margem profunda – Tecido abaixo do tumor, mais profundamente na parede esofágica.
-
Margem proximal – Borda superior do tecido removido, mais próxima da boca.
-
Margem distal – A borda inferior, mais próxima do estômago.
-
Margem radial – A superfície externa do esôfago, especialmente importante em tumores que podem ter crescido através da parede esofágica para tecidos próximos.
Seu relatório listará cada uma dessas margens e se o câncer foi encontrado ou não na borda.
Linfonodos e estágio patológico nodal (pN)
Gânglios linfáticos são pequenos órgãos em forma de feijão que fazem parte do sistema imunológico. Eles ajudam a filtrar substâncias do corpo e desempenham um papel no combate a infecções e ao câncer. As células cancerígenas podem se espalhar do tumor original no esôfago para os linfonodos próximos através dos vasos linfáticos. Esse processo é chamado de metástase.
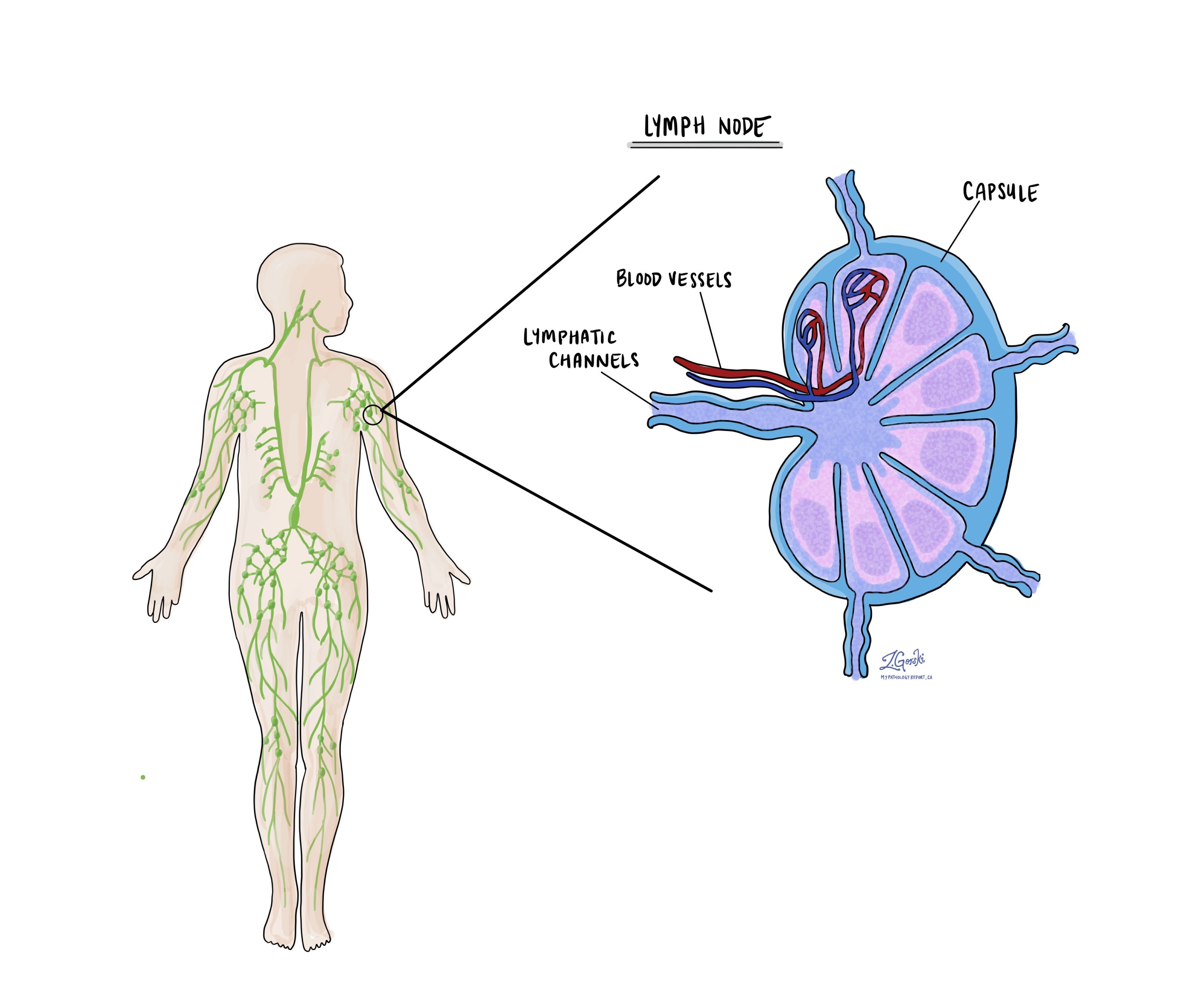
Durante a cirurgia para adenocarcinoma esofágico, os linfonodos adjacentes são frequentemente removidos e examinados ao microscópio para verificar se contêm células cancerígenas. O seu relatório patológico descreverá se cada linfonodo está:
-
Atitude – As células cancerígenas são encontradas no linfonodo.
-
Negativo – Não são observadas células cancerígenas no linfonodo.
O número de linfonodos que contêm câncer é usado para determinar o estágio patológico (pN), que faz parte do estadiamento do câncer e ajuda o médico a avaliar a extensão da doença e escolher o melhor tratamento.
Estágios patológicos nodais para adenocarcinoma esofágico:
-
pN0 – Nenhum câncer em nenhum gânglio linfático.
-
pN1 – Câncer encontrado em 1 ou 2 linfonodos.
-
pN2 – Câncer encontrado em 3 a 6 linfonodos.
-
pN3 – Câncer encontrado em 7 ou mais linfonodos.
-
pNX – Nenhum linfonodo foi submetido ou avaliado pelo patologista.
O envolvimento dos linfonodos é um forte indicador de como o câncer pode se comportar e da probabilidade de retorno ou disseminação após a cirurgia. Se o câncer for encontrado nos linfonodos, seu médico poderá recomendar tratamentos adicionais, como quimioterapia, radioterapia ou imunoterapia, para reduzir o risco de recorrência.
Resposta ao tratamento anterior
Se você recebeu quimioterapia, radioterapia ou uma combinação de ambas antes da cirurgia (chamada terapia neoadjuvante), seu laudo patológico geralmente incluirá uma descrição de como o tumor respondeu a esse tratamento. Isso é chamado de escore de regressão tumoral e ajuda os médicos a entender a extensão do tumor destruída antes da cirurgia.
Um sistema comumente usado é o esquema de Ryan modificado, que atribui uma pontuação de 0 a 3 com base em quantas células cancerígenas ainda são visíveis no microscópio após o tratamento.
Pontuação 0 – Resposta completa: Não há células cancerígenas no tecido. Isso significa que o tratamento funcionou extremamente bem e destruiu todas as células tumorais detectáveis.
Pontuação 1 – Resposta quase completa: Apenas células cancerígenas isoladas ou pequenos grupos de células cancerígenas são observados. Isso indica uma resposta muito forte ao tratamento, com pouquíssimas células cancerígenas restantes.
Pontuação 2 – Resposta parcial: Ainda há células cancerígenas presentes, mas o patologista observa sinais de que o tumor diminuiu ou foi afetado pelo tratamento. Isso significa que o tratamento ajudou, mas o tumor não foi completamente destruído.
Pontuação 3 – Resposta fraca ou nenhuma resposta: O tumor ainda se parece muito com o que tinha antes do tratamento, com muitas células cancerígenas e sem sinais claros de que tenha encolhido ou sido danificado. Isso significa que o tratamento não funcionou bem contra o tumor.
Qual é o prognóstico?
O fator mais importante que determina o prognóstico é o estágio do câncer no momento do diagnóstico. Outros fatores incluem o grau do tumor, a invasão linfovascular (câncer nos vasos sanguíneos ou linfáticos), a invasão perineural (câncer ao redor dos nervos) e a resposta ao tratamento. Tumores com superexpressão de HER2 ou positividade para PD-L1 podem responder a terapias direcionadas ou imunoterapia.
Perguntas para fazer ao seu médico
-
Que parte do meu esôfago é afetada pelo tumor?
-
O câncer estava limitado às camadas internas do esôfago ou cresceu mais profundamente na parede?
-
Houve envolvimento de algum linfonodo? Se sim, quantos?
-
O câncer apresentou alguma invasão linfovascular ou perineural?
-
Qual era o grau histológico do tumor?
-
As margens cirúrgicas estavam limpas ou foram vistas células cancerígenas na borda do tecido removido?
-
O tumor mostrou sinais de resposta à quimioterapia ou radiação (regressão do tumor)?
-
Foi feito teste para HER2 e, se sim, quais foram os resultados?
-
O câncer foi testado para PD-L1 ou proteínas de reparo de incompatibilidade e o que isso significa para o tratamento?
-
Com base no relatório de patologia, qual é meu estágio patológico (pTNM)?
-
Quais tratamentos adicionais podem ser recomendados com base nessas descobertas?