por Jason Wasserman MD PhD FRCPC
21 de diciembre de 2023
El adenocarcinoma de estómago, también conocido como cáncer gástrico, es un tipo de cáncer que comienza en las células que recubren la superficie interna del estómago. Es la forma más común de cáncer de estómago y representa aproximadamente del 90% al 95% de todos los cánceres de estómago. El pronóstico para el adenocarcinoma de estómago varía ampliamente según el grado histológico, el estadio en el momento del diagnóstico y la diseminación de las células cancerosas a ganglios linfáticos.
Este artículo le ayudará a comprender el diagnóstico y el informe patológico del adenocarcinoma de estómago.
El estomago
El estómago es un órgano musculoso y hueco del tracto gastrointestinal de los seres humanos y de muchos animales. Desempeña un papel crucial en el sistema digestivo al procesar los alimentos ingeridos, descomponerlos en una forma semilíquida llamada quimo y liberarlos gradualmente en el intestino delgado.
El estómago se divide en cuatro secciones principales, cada una con funciones específicas:
- Cardias: Esta es la primera sección por donde los alimentos ingresan al estómago desde el esófago. Contiene glándulas que secretan moco, protegiendo el revestimiento del estómago del jugo gástrico ácido.
- Fondo de ojo: Ubicado encima del cardias, el fondo de ojo almacena los alimentos no digeridos y los gases liberados por la digestión química de los alimentos. Desempeña un papel menor en el proceso de digestión.
- Cuerpo (cuerpo): la sección más grande y la principal parte digestiva del estómago, el cuerpo secreta ácido y enzimas digestivas para descomponer químicamente los alimentos en una forma semilíquida, el quimo.
- Píloro: La sección final del estómago que actúa como válvula para controlar el vaciado del contenido del estómago hacia el intestino delgado. Contiene el esfínter pilórico, que se abre para permitir que el quimo pase al intestino delgado y se cierra para evitar el reflujo.
El antro es la ubicación más común del adenocarcinoma invasivo de estómago. Esta área es particularmente susceptible al adenocarcinoma debido a su exposición a diversos factores que pueden contribuir al desarrollo del cáncer, como Helicobacter pylori infección, inflamación crónica, factores dietéticos y presencia de ácidos biliares.
¿Qué causa el adenocarcinoma en el estómago?
Los factores ambientales asociados con el adenocarcinoma en el estómago incluyen Helicobacter pylori infección, Virus de Epstein-Barr (EBV) infección, tabaquismo y factores dietéticos. Las mutaciones genéticas que involucran los genes CDH1 o APC también están asociadas con un mayor riesgo de desarrollar adenocarcinoma de estómago.
¿Cuáles son los síntomas del adenocarcinoma de estómago?
Los síntomas del adenocarcinoma de estómago pueden incluir dificultad para tragar, pérdida de peso, dolor de estómago, náuseas, vómitos y sensación de saciedad después de ingerir pequeñas cantidades de alimentos. Sin embargo, las primeras etapas de la enfermedad a menudo producen pocos o ningún síntoma, lo que dificulta la detección temprana.
Qué buscar en su informe de patología para el adenocarcinoma de estómago:
Grado histológico
El adenocarcinoma invasivo de estómago se divide en tres grados: bien diferenciado, moderadamente diferenciado y poco diferenciado. El grado se basa en el porcentaje de células tumorales que forman estructuras redondas llamadas glándulas. Un tumor que no forma glándulas se llama indiferenciado. El grado es importante porque los tumores poco diferenciados e indiferenciados tienden a comportarse de manera más agresiva; por ejemplo, estos tumores tienen más probabilidades de propagarse a ganglios linfáticos y otras partes del cuerpo.
- Bien diferenciado: más del 95% del tumor está formado por glándulas. Los patólogos también describen estos tumores como grado 1.
- Moderadamente diferenciado: del 50 al 95% del tumor está formado por glándulas. Los patólogos también describen estos tumores como de grado 2.
- Pobremente diferenciado: menos del 50% del tumor está formado por glándulas. Los patólogos también describen estos tumores como de grado 3.
- Indiferenciado: se ven muy pocas glándulas en cualquier parte del tumor.
Adenocarcinoma de estómago de tipo difuso
El adenocarcinoma de estómago de tipo difuso es un subtipo histológico específico caracterizado por células cancerosas que se diseminan ampliamente por todo el revestimiento del estómago sin formar una masa distintiva. Esta clasificación es parte del sistema de clasificación de Lauren, que divide el adenocarcinoma de estómago en tipos intestinal y difuso. Un nombre alternativo para el adenocarcinoma de tipo difuso es adenocarcinoma poco cohesivo.
El cáncer gástrico de tipo difuso se caracteriza por la distribución dispersa de células cancerosas a lo largo de la pared del estómago, que a menudo incluyen células en anillo de sello, que son conocidos por su apariencia distintiva debido a una gran vacuola que desplaza el núcleo de la célula. Este subtipo está menos asociado con factores ambientales y más con predisposiciones genéticas, afectando potencialmente a pacientes más jóvenes y mostrando un patrón familiar.
El adenocarcinoma de estómago de tipo difuso plantea importantes desafíos en términos de diagnóstico y tratamiento. Debido a su naturaleza generalizada y a la falta de una masa tumoral bien definida, puede resultar difícil detectarlo tempranamente. Generalmente se considera más agresivo que el tipo intestinal, con propensión a metástasis tempranas y peor respuesta a la quimioterapia tradicional. En consecuencia, el pronóstico del cáncer gástrico de tipo difuso suele ser peor, lo que subraya la importancia de identificar este subtipo tempranamente para adaptar las estrategias de tratamiento más efectivas.
Adenocarcinoma de estómago de tipo poco cohesivo
El adenocarcinoma de estómago poco cohesivo es un subtipo histológico específico caracterizado por células cancerosas que no se pegan entre sí ni forman tumores sólidos, sino que se diseminan de forma difusa por todo el revestimiento y la pared del estómago. Esta característica hace que el cáncer sea difícil de detectar y diagnosticar tempranamente, ya que la falta de una masa definida significa que es posible que no se identifique fácilmente mediante imágenes o endoscopia. Un nombre alternativo para el adenocarcinoma de tipo poco cohesivo es adenocarcinoma de tipo difuso.
El tipo de adenocarcinoma poco cohesivo se caracteriza por la distribución dispersa de células cancerosas a lo largo de la pared del estómago, que a menudo incluyen células en anillo de sello. Estas células son conocidas por su apariencia distintiva debido a una gran vacuola que desplaza el núcleo de la célula.
Identificar un subtipo poco discohesivo es crucial para la planificación y el pronóstico del tratamiento. Debido a que estas células cancerosas se diseminan ampliamente y carecen de conexiones intercelulares, pueden penetrar más profundamente en la pared del estómago y hacer metástasis a otros órganos antes que las formas más cohesivas de cáncer. Este comportamiento contribuye a un escenario de tratamiento más desafiante y generalmente indica un peor pronóstico. Reconocer este subtipo permite a los médicos considerar enfoques terapéuticos más agresivos y personalizados, reconociendo los desafíos únicos en el manejo de esta forma de cáncer de estómago.
Células en anillo de sello
Células en anillo de sello Por lo general, se encuentran en el adenocarcinoma de estómago difuso o poco cohesivo. Estas células contienen grandes vacuolas de mucina que empujan el núcleo hacia la periferia, dándole a la célula una apariencia de anillo. Esta característica es importante porque el carcinoma de células en anillo de sello es conocido por su comportamiento agresivo y tendencia a diseminarse de manera más difusa por toda la pared del estómago y más allá, en comparación con otras formas de cáncer de estómago. Las células en anillo de sello se observan típicamente en el adenocarcinoma de tipo poco cohesivo y en el adenocarcinoma de estómago de tipo difuso.
La identificación de las células en anillo de sello es importante por varias razones. En primer lugar, a menudo sugiere un peor pronóstico debido a la naturaleza agresiva del cáncer y su capacidad de propagarse rápidamente. En segundo lugar, este hallazgo puede influir en las decisiones de tratamiento, ya que los cánceres con células en anillo de sello pueden responder de manera diferente a la quimioterapia y otros tratamientos que otros tipos de cáncer de estómago.
Profundidad de la invasión y estadio patológico (pT)
En patología “invasión“Se refiere al proceso por el cual las células cancerosas se propagan desde el sitio original del tumor a los tejidos u órganos circundantes. En concreto, en el caso del adenocarcinoma, que se origina en la pared del estómago mucosa (el revestimiento más interno), la invasión significa que las células cancerosas se han movido a otras capas del estómago o incluso a órganos fuera del estómago. Un patólogo sólo puede observar la invasión examinando el tumor con un microscopio.
Durante este examen microscópico, el patólogo determina hasta qué punto las células cancerosas se han movido más allá de la mucosa hacia el tejido cercano, lo que se conoce como profundidad o nivel de invasión. La importancia de identificar la profundidad de la invasión radica en su capacidad para predecir la agresividad del cáncer: los tumores que penetran más profundamente en la pared del estómago son más propensos a metastatizar a otras partes del cuerpo, incluyendo ganglios linfáticos, hígado o pulmones. Además, la profundidad de la invasión ayuda a establecer el estadio patológico (pT) del tumor, que es crucial para decidir la estrategia de tratamiento más adecuada.
La mayoría de los informes de patología del adenocarcinoma invasivo de estómago describirán la profundidad o el nivel de la invasión de la siguiente manera:
- Intramuscosal: El tumor se llama intramucoso si las células cancerosas no se han diseminado fuera de la mucosa. La mucosa incluye la lámina propia o muscularis mucosa.
- Submucosa: Submucosa significa que las células cancerosas han pasado la muscular de la mucosa y se encuentran en la submucosa.
- Muscular propia: La muscular propia es el haz grueso de músculos que se encuentra en el medio del estómago. Por lo general, este nivel de invasión solo se puede observar después de que se ha extirpado todo el tumor.
- Tejido blando subseroso: Las células cancerosas del tejido blando subseroso se encuentran cerca de la superficie exterior del estómago.
- Serosa: Células cancerosas que pasan por la serosa en la superficie exterior del estómago. Desde aquí, las células cancerosas pueden propagarse a órganos cercanos como el bazo, el páncreas, el intestino delgado, el colon, la glándula suprarrenal o el riñón.
Su patólogo utilizará la profundidad de la invasión para determinar el estadio patológico del tumor (pT) de la siguiente manera:
- T1a: Las células cancerosas sólo se encontraron en la mucosa. Esto también se llama adenocarcinoma intramucoso.
- T1b: Las células cancerosas se han extendido a la submucosa.
- T2: Las células cancerosas se han diseminado hacia la muscular propia.
- T3: Las células cancerosas se encuentran en el tejido blando subseroso, justo debajo de la superficie exterior del estómago.
- T4a: Las células cancerosas han atravesado la serosa y se encuentran en la superficie exterior del estómago.
- T4b: Las células cancerosas se han diseminado a órganos cercanos al estómago.
HER2
Las células de todo el cuerpo producen la HER2 proteína, que actúa como un interruptor para promover el crecimiento y la división celular. Sin embargo, cuando las células cancerosas producen en exceso HER2, crecen y se dividen mucho más rápido que las células normales. Aproximadamente uno de cada cinco tumores de estómago produce en exceso HER2. Por lo tanto, su patólogo analizará sus células cancerosas para detectar la presencia de HER2.
Inmunohistoquímica (IHC) Es la prueba más utilizada para detectar HER2 en células cancerosas. Otro método se llama hibridación fluorescente in situ (FISH). Algunos laboratorios realizarán una prueba FISH solo después de que la prueba IHC produzca un resultado equívoco.
Si su tumor se analizó mediante inmunohistoquímica, su informe clasificará los resultados como:
– Negativo (0 o 1): indica que las células cancerosas no están produciendo en exceso HER2.
– Equívoco (2) – Sugiere que las células cancerosas podrían estar produciendo en exceso HER2.
– Positivo (3): confirma que las células cancerosas están produciendo en exceso HER2.
Los pacientes con tumores HER2 positivos pueden calificar para tratamientos específicos. Hable con su médico sobre las opciones de tratamiento que están disponibles para usted.
Proteínas reparadoras de desajustes (MMR)
La reparación de errores de coincidencia (MMR) es un sistema crítico dentro de todas las células normales y sanas que corrige los errores del ADN. Este sistema se basa en diferentes proteínas, principalmente MSH2, MSH6, MLH1 y PMS2.
Estas cuatro proteínas, MSH2, MSH6, MLH1 y PMS2, se emparejan (MSH2 con MSH6 y MLH1 con PMS2) para reparar el ADN dañado. Si falta una proteína, su par no puede reparar el ADN de forma eficaz, lo que aumenta el riesgo de cáncer.
Los patólogos realizan pruebas de reparación de discrepancias en muestras de tumores para verificar la ausencia de cualquiera de estas proteínas, un proceso que se detalla en los informes de patología. El método principal para esta prueba es inmunohistoquímica, que identifica si las células tumorales producen las cuatro proteínas reparadoras de errores de coincidencia.
Si falta una proteína, el informe de patología la anotará como "perdida" o "deficiente". A menudo, cuando falta una proteína, también se pierde su par. Si la proteína se expresa normalmente, el informe de patología la anotará como “intacta”.
Para el adenocarcinoma de estómago, la ausencia de una o más proteínas reparadoras de discordancias generalmente indica un mejor pronóstico e indica una posible mayor capacidad de respuesta a los inhibidores de puntos de control inmunológico, un tipo de tratamiento contra el cáncer.
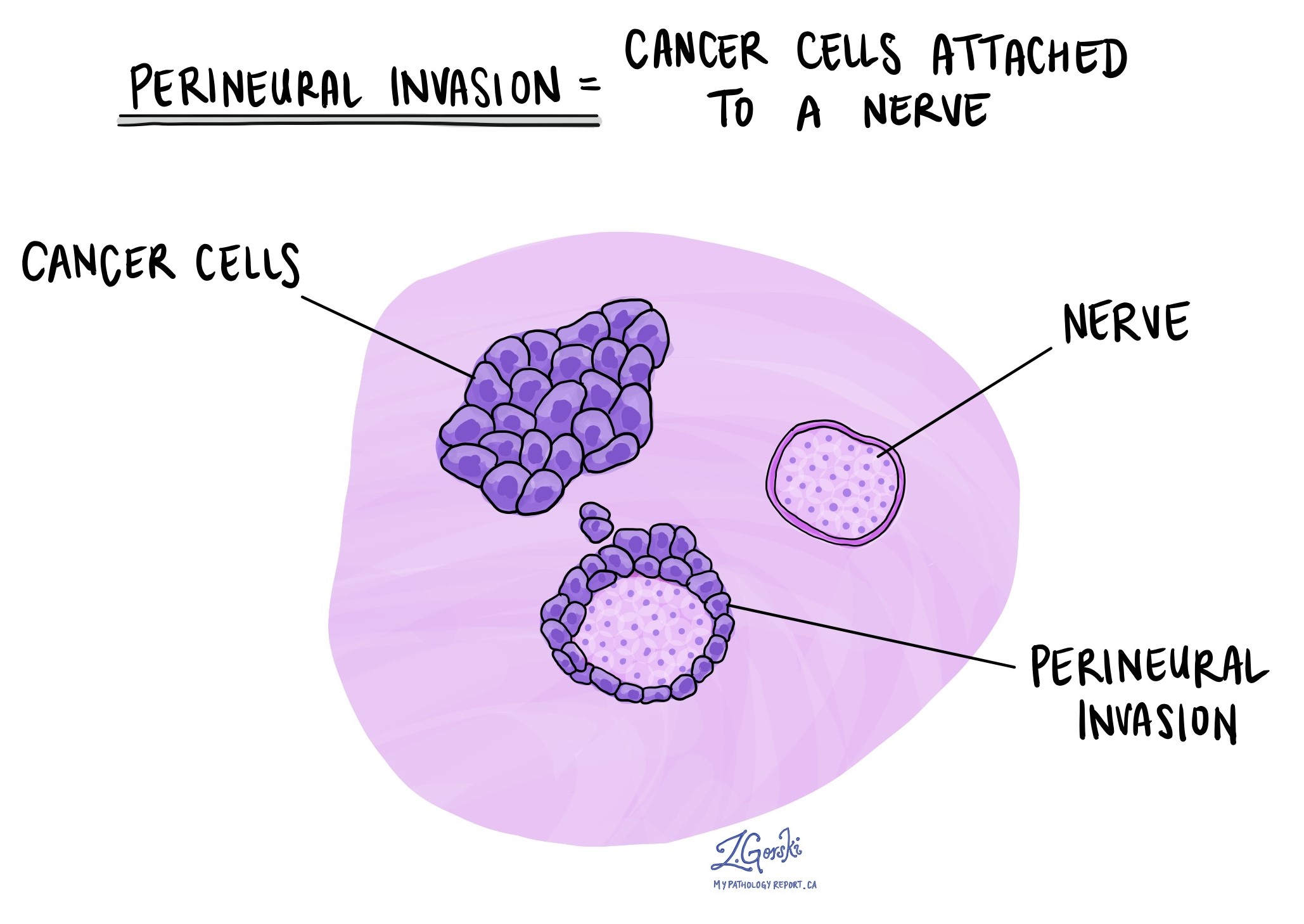
Invasión perineural
Los patólogos utilizan el término "invasión perineural" para describir una situación en la que las células cancerosas se adhieren a un nervio o lo invaden. "Invasión intraneural" es un término relacionado que se refiere específicamente a las células cancerosas que se encuentran dentro de un nervio. Los nervios, que parecen cables largos, están formados por grupos de células conocidas como neuronas. Estos nervios, presentes en todo el cuerpo, transmiten información como temperatura, presión y dolor entre el cuerpo y el cerebro. La presencia de invasión perineural es importante porque permite que las células cancerosas viajen a lo largo del nervio hasta los órganos y tejidos cercanos, lo que aumenta el riesgo de que el tumor reaparezca después de la cirugía.
Invasión linfovascular
La invasión linfovascular ocurre cuando las células cancerosas invaden un vaso sanguíneo o un vaso linfático. Los vasos sanguíneos, tubos delgados que transportan sangre por todo el cuerpo, contrastan con los vasos linfáticos, que transportan un líquido llamado linfa en lugar de sangre. Estos vasos linfáticos se conectan a pequeños órganos inmunes conocidos como ganglios linfáticos, esparcidos por todo el cuerpo. La invasión linfovascular es importante porque permite que las células cancerosas se propaguen a otras partes del cuerpo, incluidos los ganglios linfáticos o el hígado, a través de la sangre o los vasos linfáticos.

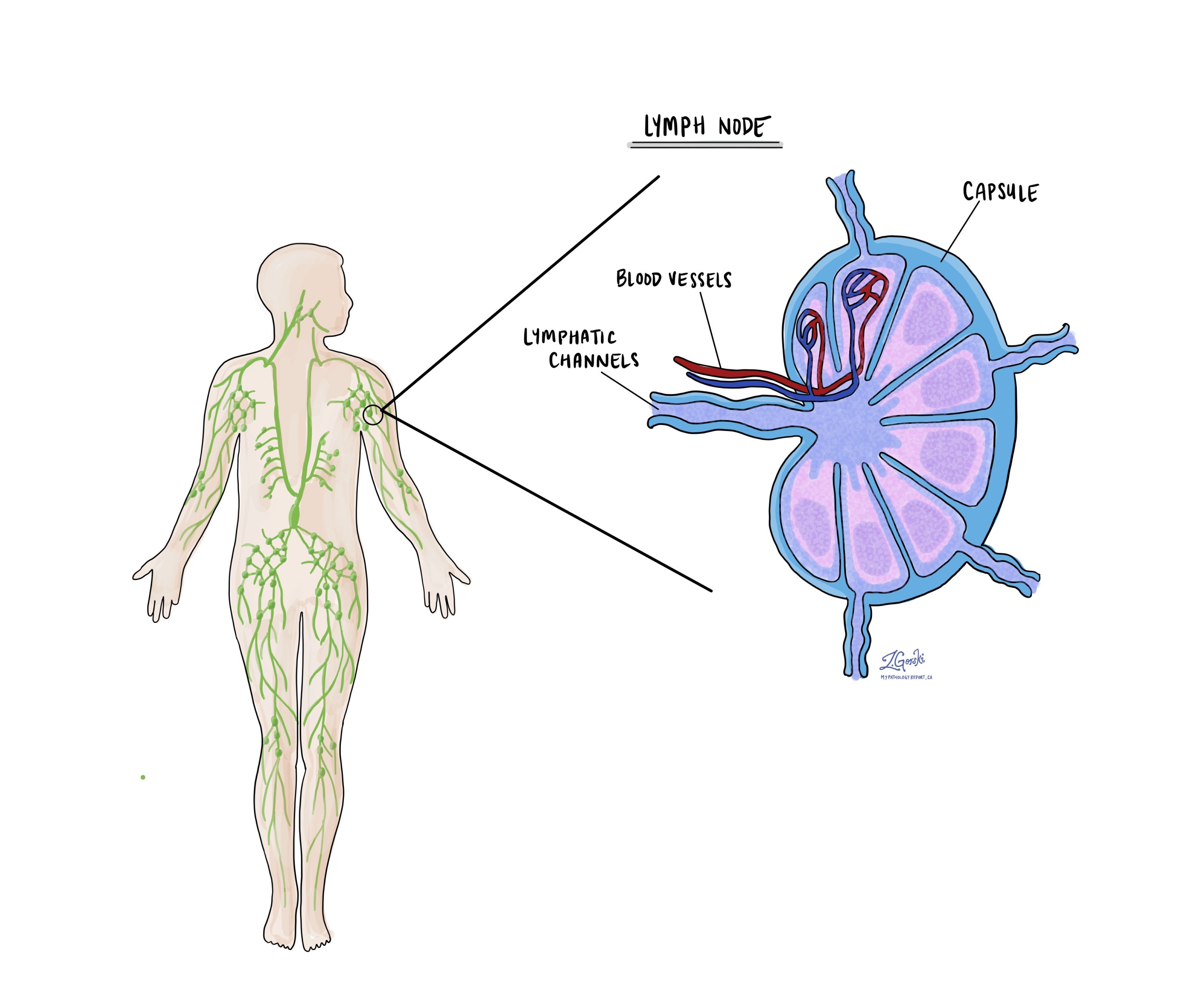
Ganglios linfáticos
Pequeños órganos inmunitarios, conocidos como ganglios linfáticos, se encuentran en todo el cuerpo. Las células cancerosas pueden viajar desde un tumor hasta estos ganglios linfáticos a través de pequeños vasos linfáticos. Por esta razón, los médicos suelen extirpar y examinar microscópicamente los ganglios linfáticos en busca de células cancerosas. Este proceso, en el que las células cancerosas se mueven desde el tumor original a otra parte del cuerpo como un ganglio linfático, se denomina metastásica.
Las células cancerosas suelen migrar primero a los ganglios linfáticos cercanos al tumor, aunque los ganglios linfáticos distantes también pueden verse afectados. En consecuencia, los cirujanos suelen extirpar primero los ganglios linfáticos más cercanos al tumor. Es posible que extirpen los ganglios linfáticos más alejados del tumor si están agrandados y existe una fuerte sospecha de que contienen células cancerosas.
Los patólogos examinarán los ganglios linfáticos extirpados bajo un microscopio y los hallazgos se detallarán en su informe. Un resultado "positivo" indica la presencia de células cancerosas en el ganglio linfático, mientras que un resultado "negativo" significa que no se encontraron células cancerosas. Si el informe encuentra células cancerosas en un ganglio linfático, también podría especificar el tamaño del grupo más grande de estas células, a menudo denominado "foco" o "depósito". Extensión extraganglionar Ocurre cuando las células tumorales penetran la cápsula externa del ganglio linfático y se diseminan al tejido adyacente.
El examen de los ganglios linfáticos es importante por dos razones. En primer lugar, ayuda a determinar el estadio ganglionar patológico (pN). En segundo lugar, descubrir células cancerosas en un ganglio linfático sugiere un mayor riesgo de encontrar células cancerosas en otras partes del cuerpo más adelante. Esta información guía a su médico a la hora de decidir si necesita tratamientos adicionales, como quimioterapia, radioterapia o inmunoterapia.
Márgenes
En patología, un margen es el borde del tejido extirpado durante la cirugía tumoral. El estado de los márgenes en un informe de patología es importante ya que indica si se extirpó todo el tumor o si quedó parte. Esta información ayuda a determinar la necesidad de tratamiento adicional.
Los patólogos suelen evaluar los márgenes después de un procedimiento quirúrgico como un excisión or resección, destinado a extirpar todo el tumor. Los márgenes no suelen evaluarse después de un biopsia, que extirpa sólo una parte del tumor. La cantidad de márgenes informados y su tamaño (cuánto tejido normal hay entre el tumor y el borde cortado) varían según el tipo de tejido y la ubicación del tumor.
Los patólogos examinan los márgenes para comprobar si hay células tumorales en el borde cortado del tejido. Un margen positivo, donde se encuentran las células tumorales, sugiere que es posible que quede algo de cáncer en el cuerpo. Por el contrario, un margen negativo, sin células tumorales en el borde, sugiere que el tumor se extirpó por completo. Algunos informes también miden la distancia entre las células tumorales más cercanas y el margen, incluso si todos los márgenes son negativos.

Sobre este articulo
Los médicos escribieron este artículo para ayudarlo a leer y comprender su informe de patología. Contacto si tiene preguntas sobre este artículo o su informe de patología. Para obtener una introducción completa a su informe de patología, lea este artículo.


