par Jason Wasserman MD PhD FRCPC
6 février 2026
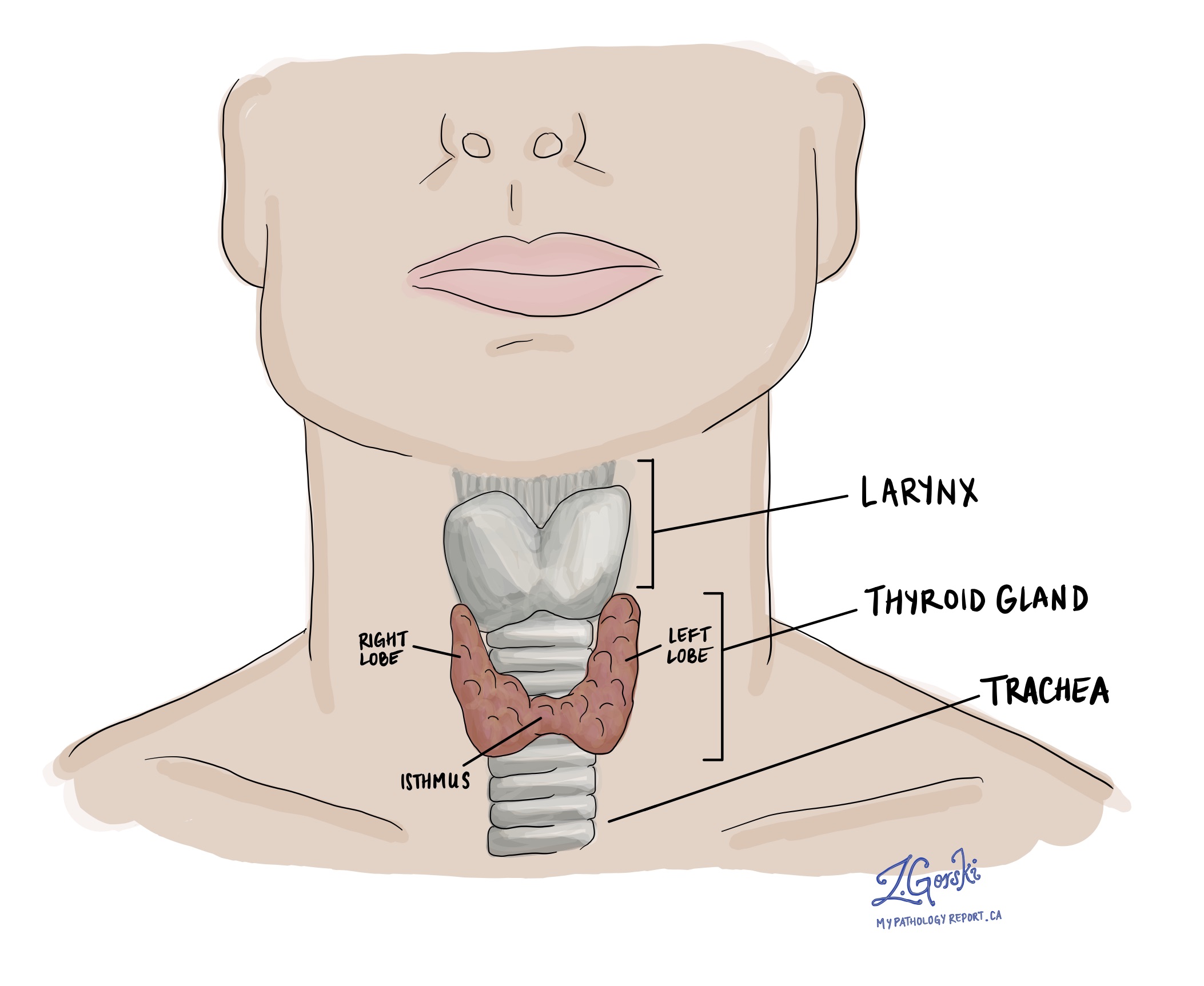
Carcinome thyroïdien folliculaire Il s'agit d'un type de cancer de la thyroïde qui se développe à partir des cellules folliculaires, les cellules de la glande thyroïde qui produisent les hormones thyroïdiennes. La thyroïde est une petite glande en forme de papillon située à l'avant du cou et qui contribue à réguler la façon dont le corps utilise l'énergie.
Ce cancer est considéré comme bien différencié, ce qui signifie que les cellules tumorales ressemblent encore à des cellules thyroïdiennes normales au microscope. Ce qui distingue le carcinome folliculaire de la thyroïde d'une simple tumeur est un cancer. bénin tumeur, est invasionL’invasion signifie que les cellules tumorales ont traversé la capsule tumorale (la fine couche de tissu entourant la tumeur) et/ou ont pénétré dans les vaisseaux sanguins voisins.
Cet article explique comment le carcinome folliculaire de la thyroïde est diagnostiqué, classé et évalué, et quelles en sont les caractéristiques. pathologistes rechercher et comment ces résultats sont liés au pronostic et au traitement.
Le carcinome folliculaire de la thyroïde est-il fréquent ?
Le carcinome folliculaire de la thyroïde représente environ 5 à 15 % des cancers de la thyroïde. Il est moins fréquent que carcinome papillaire de la thyroïde Elle est plus fréquente chez l'adulte que chez l'enfant. Son incidence est plus élevée dans les régions du monde où l'apport alimentaire en iode est faible.
Quels sont les symptômes du carcinome folliculaire de la thyroïde ?
De nombreuses personnes remarquent d'abord une grosseur indolore dans le cou, généralement au niveau de la glande thyroïde. Certaines tumeurs sont découvertes fortuitement lors d'examens d'imagerie ou d'un examen physique de routine.
Les tumeurs plus volumineuses peuvent provoquer des symptômes liés à la compression des structures avoisinantes, tels que des difficultés à avaler, un enrouement ou une sensation de tension dans la nuque. La plupart des patients présentent des taux d'hormones thyroïdiennes normaux ; les symptômes d'hyperthyroïdie ou d'hypothyroïdie sont donc rares.
Dans un faible pourcentage de cas, le cancer s'est déjà propagé à des organes distants, comme les poumons ou les os. Lorsque cela se produit, les symptômes peuvent provenir du site de propagation, comme des douleurs osseuses ou un essoufflement.
Quelles sont les causes du carcinome folliculaire de la thyroïde ?
La cause exacte n'est pas toujours connue. Plusieurs facteurs sont associés à un risque accru, notamment une carence en iode, une exposition aux radiations (surtout pendant l'enfance) et des syndromes tumoraux héréditaires tels que le syndrome tumoral hamartomateux PTEN (syndrome de Cowden), le syndrome DICER1, le syndrome de Werner et le complexe de Carney.
La plupart des cas sont sporadiques, c'est-à-dire qu'ils surviennent par hasard et ne sont pas héréditaires.
Comment diagnostique-t-on le carcinome folliculaire de la thyroïde ?
Le diagnostic du carcinome folliculaire de la thyroïde nécessite plusieurs étapes, car cette tumeur ne peut être diagnostiquée de manière définitive par imagerie ou biopsie à l'aiguille seule.
Le processus de diagnostic comprend généralement des examens d'imagerie, biopsie par aspiration à l'aiguille fine (FNA)L’ablation chirurgicale de la tumeur et un examen microscopique minutieux permettent d’établir le diagnostic définitif. Ce diagnostic est presque toujours posé après l’intervention, lorsque la capsule tumorale et les vaisseaux sanguins avoisinants peuvent être examinés en détail.
Imagerie
L'échographie est généralement le premier examen d'imagerie réalisé. Le carcinome folliculaire de la thyroïde se présente souvent comme un nodule thyroïdien solide et bien délimité, parfois entouré d'un halo dû à la capsule tumorale. L'imagerie ne permet pas de distinguer avec certitude un carcinome folliculaire de la thyroïde d'un adénome folliculaire bénin.
Aspiration à l'aiguille fine (FNA)
La cytoponction à l'aiguille fine (FNA) peut révéler qu'une tumeur est composée de cellules folliculaires, mais elle ne permet pas de déterminer si elle est bénigne ou maligne. En effet, l'invasion ne peut être évaluée sur de petits échantillons de biopsie. Par conséquent, les comptes rendus de FNA utilisent souvent des termes tels que : néoplasme folliculaire or suspect de néoplasme folliculaireet une intervention chirurgicale est nécessaire pour établir le diagnostic.
Caractéristiques microscopiques
Au microscope, le carcinome folliculaire de la thyroïde est composé de cellules folliculaires organisées en follicules (espaces ronds qui stockent normalement les hormones thyroïdiennes) ou selon des structures solides ou trabéculaires. Les cellules tumorales ressemblent à celles d'une tumeur bénigne. adénome folliculairemais la principale différence réside dans leur nature invasive.
L'invasion capsulaire signifie que les cellules tumorales ont complètement envahi la capsule tumorale. L'invasion vasculaire signifie que des cellules tumorales se trouvent à l'intérieur des vaisseaux sanguins, souvent adhérentes à la paroi vasculaire ou mêlées à un caillot sanguin. L'identification d'au moins un foyer d'invasion capsulaire ou vasculaire est nécessaire pour poser le diagnostic de carcinome folliculaire de la thyroïde.
Immunohistochimie
Immunohistochimie Il s'agit d'un test de laboratoire utilisant des anticorps pour détecter des protéines spécifiques dans les cellules tumorales. Dans le carcinome folliculaire de la thyroïde, les cellules tumorales expriment généralement la thyroglobuline, le TTF-1 et le PAX8, confirmant ainsi que la tumeur provient des cellules folliculaires thyroïdiennes.
Ces tests permettent de confirmer l'origine de la tumeur et d'exclure d'autres types de cancer. Cependant, l'immunohistochimie ne permet pas de distinguer avec certitude le carcinome folliculaire de la thyroïde de l'adénome folliculaire. Le diagnostic repose donc toujours sur l'identification de l'invasion au microscope.
Classification des tumeurs (sous-types)
Le carcinome folliculaire de la thyroïde est divisé en sous-types selon l'étendue de l'invasion tumorale des structures environnantes. Cette classification est importante car elle influence fortement le pronostic et le suivi.
Carcinome thyroïdien folliculaire mini-invasif
Les tumeurs peu invasives présentent uniquement une invasion capsulaire, ce qui signifie que les cellules tumorales ont traversé la capsule sans pénétrer dans les vaisseaux sanguins. Ces tumeurs sont généralement bien circonscrites et évoluent de façon indolente. Lorsqu'elles sont complètement retirées, le pronostic est excellent et aucun traitement complémentaire n'est souvent nécessaire.
Carcinome folliculaire thyroïdien angio-invasif encapsulé
Ces tumeurs sont entourées d'une capsule, mais elles présentent une invasion vasculaire, c'est-à-dire que des cellules tumorales se trouvent à l'intérieur des vaisseaux sanguins. Ces vaisseaux sanguins agissent comme des autoroutes, transportant les cellules tumorales vers des organes distants.
Les pathologistes subdivisent en outre l'invasion vasculaire en :
-
Invasion vasculaire limitée : les cellules tumorales sont présentes dans moins de 4 vaisseaux sanguins.
-
Invasion vasculaire étendue : des cellules tumorales sont retrouvées dans 4 vaisseaux sanguins ou plus.
Les tumeurs présentant une invasion vasculaire limitée ont un pronostic bon à intermédiaire, tandis que celles présentant une invasion vasculaire étendue comportent un risque plus élevé de propagation à distance et nécessitent un suivi plus étroit.
Carcinome folliculaire thyroïdien largement invasif
Les tumeurs très invasives présentent une infiltration importante du tissu thyroïdien environnant ou des tissus mous adjacents. Ces tumeurs ne sont pas toujours complètement encapsulées, ce qui rend l'invasion plus évidente. Elles impliquent souvent de nombreux vaisseaux sanguins et présentent le risque le plus élevé de récidive et de métastases à distance.
Ganglions
Ganglions Ce sont de petits organes immunitaires qui filtrent la lymphe. Les cellules cancéreuses peuvent se propager de la thyroïde aux ganglions lymphatiques voisins par les vaisseaux lymphatiques.
Le carcinome folliculaire de la thyroïde se propage moins souvent aux ganglions lymphatiques que le carcinome papillaire, mais cela reste possible. Tout ganglion lymphatique prélevé lors de l'intervention chirurgicale est examiné au microscope et son résultat est interprété comme positif ou négatif pour les cellules tumorales.
La présence de cellules tumorales dans les ganglions lymphatiques peut entraîner une augmentation du stade du cancer et influencer les recommandations en matière de traitement et de suivi complémentaires.
Les marges
A marge Il s'agit du bord du tissu retiré lors d'une intervention chirurgicale. Les pathologistes examinent les marges pour déterminer si des cellules tumorales sont présentes au niveau du bord de coupe du tissu.
Une marge négative signifie qu'aucune cellule tumorale n'est visible au niveau de la marge, ce qui suggère que la tumeur a été complètement retirée. Une marge positive signifie que des cellules tumorales sont présentes au niveau de la marge, indiquant qu'il peut subsister des cellules tumorales. L'évaluation des marges permet d'orienter les décisions concernant les traitements complémentaires et la surveillance.
Stade pathologique (pTNM)
Le stade pathologique du carcinome folliculaire de la thyroïde est déterminé selon la classification TNM, qui prend en compte la tumeur primitive (T), les ganglions lymphatiques (N) et les métastases à distance (M). En général, un stade plus élevé indique une maladie plus avancée et un pronostic plus défavorable.
Stade tumoral (pT)
Le stade de la tumeur est déterminé par sa taille et par le fait que les cellules tumorales s'étendent ou non au-delà de la thyroïde :
-
T1 : tumeur ≤ 2 cm, confinée à la thyroïde.
-
T2 : tumeur > 2 cm mais ≤ 4 cm, confinée à la thyroïde.
-
T3 : tumeur > 4 cm ou extension minimale aux muscles du cou voisins.
-
T4 : la tumeur s’étend aux structures majeures telles que la trachée, le larynx ou l’œsophage.
Stade nodal (pN)
-
N0 : aucune cellule tumorale n’a été trouvée dans les ganglions lymphatiques.
-
N1 : cellules tumorales trouvées dans les ganglions lymphatiques.
-
NX : Aucun ganglion lymphatique n’a été soumis à l’examen.
Biomarqueurs du cancer de la thyroïde
Les biomarqueurs sont des tests réalisés sur des tissus tumoraux afin de détecter des modifications génétiques ou protéiques qui permettent de comprendre le développement et l'évolution potentielle du cancer. Dans le cas du cancer de la thyroïde, les tests de biomarqueurs contribuent au diagnostic, à l'estimation du risque de récidive et à l'identification des patients susceptibles de bénéficier de traitements ciblés. Ces tests ne sont pas systématiques et les gènes analysés dépendent du type de tumeur et du contexte clinique.
FRÈRE
Le gène BRAF contribue à réguler la croissance cellulaire normale en envoyant des signaux qui indiquent aux cellules le moment de se diviser. Dans le cancer de la thyroïde, une mutation spécifique appelée BRAF V600E active de façon permanente ce signal de croissance, permettant aux cellules tumorales de proliférer et de survivre alors qu'elles ne le devraient pas. Cette mutation est plus fréquente dans le carcinome papillaire de la thyroïde et est associée à un risque accru de récidive chez certains patients, notamment lorsqu'elle est associée à d'autres facteurs de risque. Les tumeurs porteuses de mutations BRAF peuvent répondre à des thérapies ciblées appelées inhibiteurs de BRAF, parfois en association avec des inhibiteurs de MEK, en particulier dans les formes avancées ou résistantes à l'iode radioactif.
RAS (NRAS, HRAS, KRAS)
La famille de gènes RAS joue un rôle important dans la transmission des signaux de croissance au sein des cellules thyroïdiennes normales. Lorsqu'un gène RAS mute, les signaux qu'il code deviennent hyperactifs, favorisant la croissance et la survie cellulaires. Les mutations RAS sont fréquentes dans les tumeurs thyroïdiennes à structure folliculaire, notamment le carcinome folliculaire de la thyroïde, le carcinome oncocitaire et le NIFTP. Bien que les mutations RAS ne soient pas spécifiques du cancer et puissent être observées dans des tumeurs bénignes, leur présence contribue à expliquer le développement tumoral et peut influencer la fréquence et la pertinence du suivi. À l'heure actuelle, il n'existe pas de thérapies ciblées RAS standard pour le cancer de la thyroïde, mais ces tumeurs peuvent répondre différemment à certains traitements systémiques.
Promoteur TERT
Le promoteur de TERT contrôle l'activité de la télomérase, une protéine qui permet aux cellules de maintenir leurs chromosomes lors des divisions successives. Dans les cellules normales, l'activité de la télomérase est étroitement régulée, mais des mutations du promoteur de TERT permettent aux cellules tumorales de se diviser indéfiniment. Dans le cancer de la thyroïde, les mutations du promoteur de TERT sont associées à un comportement plus agressif, un risque de récidive plus élevé et un pronostic plus sombre, en particulier lorsqu'elles sont associées à des mutations de BRAF ou de RAS. Bien qu'il n'existe pas de thérapie ciblée spécifique contre TERT, la présence de cette mutation influence souvent l'intensité du traitement et le plan de suivi.
RET
Le gène RET code pour un récepteur impliqué dans la croissance et le développement cellulaires. Dans le cancer de la thyroïde, RET peut contribuer à la cancérogenèse de deux manières différentes : par des réarrangements géniques (le plus souvent dans le carcinome papillaire de la thyroïde) ou par des mutations ponctuelles (caractéristiques du carcinome médullaire de la thyroïde). Ces modifications entraînent une activation continue du système de signalisation de la croissance. Les altérations de RET sont importantes car des thérapies ciblées très efficaces existent et peuvent être utilisées dans les formes avancées ou métastatiques de la maladie, souvent avec moins d’effets secondaires que la chimiothérapie conventionnelle.
NTRK (NTRK1, NTRK3)
Les gènes NTRK contribuent normalement à la croissance et à la communication des cellules nerveuses. Dans certains cancers de la thyroïde, ces gènes fusionnent anormalement avec d'autres gènes, créant ainsi une protéine qui stimule continuellement la croissance tumorale. Bien que rare, l'identification d'une fusion NTRK est cruciale car les tumeurs présentant cette anomalie répondent souvent de façon spectaculaire aux inhibiteurs de TRK, qui sont très efficaces même aux stades avancés de la maladie.
PPARG (réarrangement PAX8::PPARG)
Le gène PPARG régule le métabolisme et la différenciation cellulaires. Dans certains carcinomes folliculaires de la thyroïde, PPARG fusionne anormalement avec un autre gène, PAX8, créant une fusion qui perturbe le contrôle normal de la croissance. Les tumeurs présentant ce réarrangement sont souvent bien différenciées et peuvent être moins agressives, bien qu'il existe des exceptions. Il n'existe actuellement aucun traitement ciblé standard spécifique aux réarrangements de PPARG, mais ce résultat contribue à préciser le type de tumeur et son évolution attendue.
PIK3CA et AKT1
Les gènes PIK3CA et AKT1 font partie d'une voie de signalisation qui contrôle la croissance, le métabolisme et la survie cellulaires. Des mutations de ces gènes peuvent rendre les cellules tumorales plus résistantes aux mécanismes de contrôle de la croissance. Dans le cancer de la thyroïde, ces mutations sont plus fréquentes dans les tumeurs avancées, peu différenciées ou de haut grade. Leur présence peut indiquer un cancer à risque plus élevé et, dans certains cas, une éligibilité à des thérapies ciblées agissant sur la voie PI3K/AKT/mTOR, généralement dans le cadre d'essais cliniques ou en situation avancée.
TP53
Le gène TP53 est souvent qualifié de « gardien du génome » car il contribue à empêcher la division des cellules endommagées. Lorsqu'il mute, ce mécanisme de protection est perdu, permettant ainsi aux cellules génétiquement altérées de survivre et de se multiplier. Les mutations de TP53 sont rares dans les cancers de la thyroïde bien différenciés, mais fréquentes dans les carcinomes thyroïdiens peu différenciés et anaplasiques. Lorsqu'elle est identifiée, une mutation de TP53 suggère une tumeur plus agressive et peut influencer les décisions thérapeutiques et le pronostic, bien qu'il n'existe actuellement aucun traitement ciblant directement TP53.
CTNNB1 (β-caténine)
Le gène CTNNB1 produit la β-caténine, une protéine impliquée dans l'adhérence cellulaire et la signalisation de la croissance. L'activation anormale de cette voie peut entraîner une prolifération cellulaire incontrôlée. Les mutations de CTNNB1 sont rares dans les cancers thyroïdiens différenciés typiques, mais plus fréquentes dans les tumeurs de haut grade ou peu différenciées. Leur présence oriente vers un diagnostic de maladie agressive et contribue à expliquer la résistance aux traitements standards.
ALK
Le gène ALK joue normalement un rôle dans le développement cellulaire précoce. Dans de rares cancers de la thyroïde, ALK fusionne anormalement avec un autre gène, entraînant une activation continue du système immunitaire. Bien que peu fréquent, l'identification d'un réarrangement du gène ALK est importante car les thérapies ciblées contre ALK peuvent être efficaces chez les patients atteints d'une maladie avancée.
Pronostic
Le pronostic du carcinome folliculaire de la thyroïde dépend principalement de l'étendue de l'invasion. Les tumeurs peu invasives ont un excellent pronostic. Celles présentant une invasion vasculaire limitée ont un risque légèrement plus élevé, mais restent favorables avec un traitement approprié. Les tumeurs largement invasives et celles présentant une invasion vasculaire étendue comportent un risque plus élevé de récidive et de métastases à distance.
La présence de métastases à distance et de certaines modifications moléculaires, telles que les mutations du promoteur TERT, est associée à un pronostic plus défavorable.
Questions à poser à votre médecin
-
De quel sous-type de carcinome folliculaire de la thyroïde suis-je atteint ?
-
Y avait-il une invasion capsulaire ou vasculaire ?
-
Quelle était l'étendue de l'invasion vasculaire ?
-
Des ganglions lymphatiques étaient-ils touchés ?
-
Aurai-je besoin d’une thérapie à l’iode radioactif ?
-
Quel est mon risque de récidive à long terme ?
-
À quelle fréquence aurai-je besoin de tests de suivi ou d’imagerie ?


