بواسطة جايسون واسرمان دكتوراه في الطب دكتوراه FRCPC
6 كانون الثاني 2025
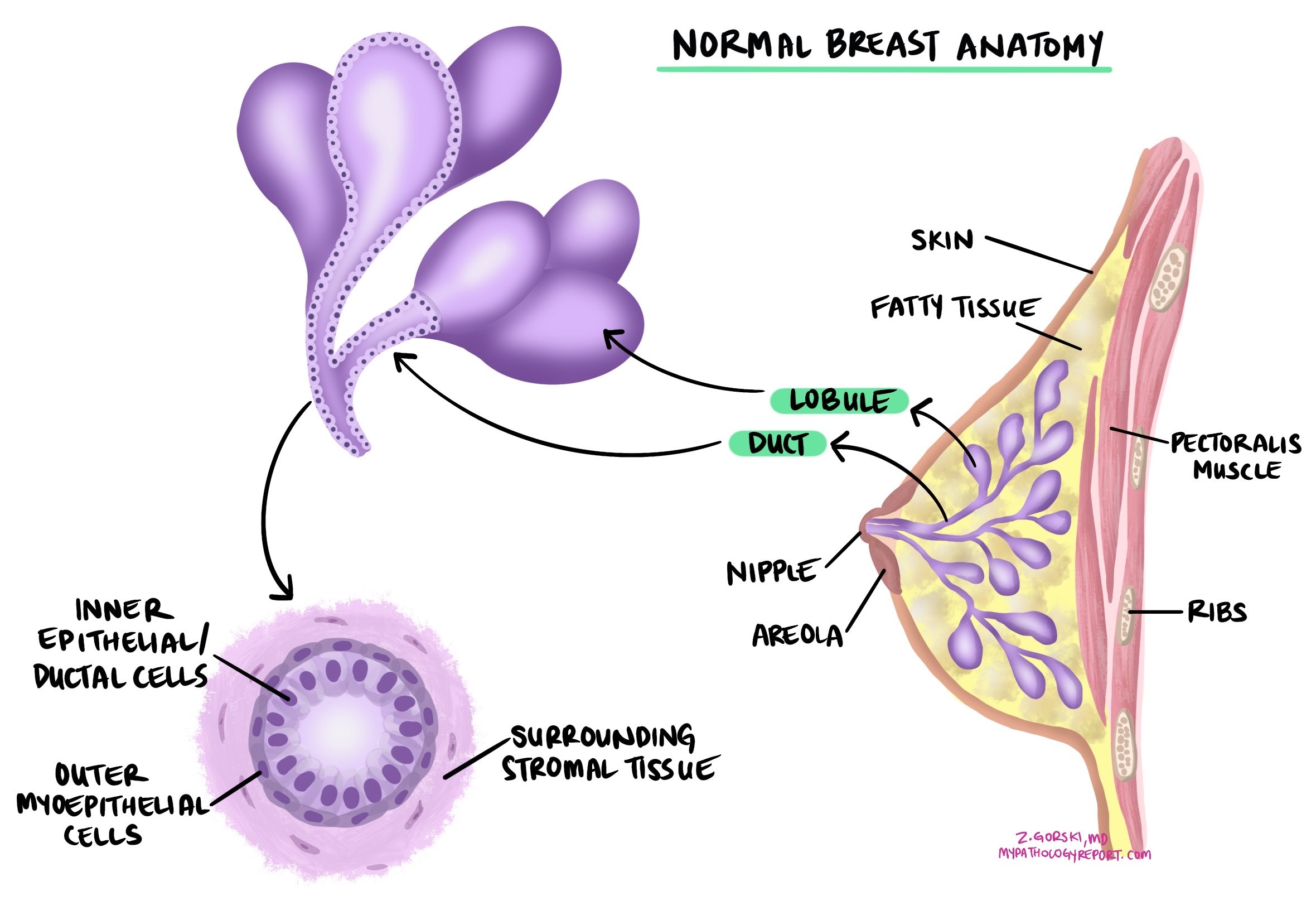
سرطان الثدي الغازية (لم يُحدد خلاف ذلك) هو أكثر أنواع سرطان الثدي شيوعًا. يبدأ في الخلايا المبطنة لقنوات الثدي ويغزو أنسجة الثدي المحيطة. يُشار إلى هذا النوع من السرطان غالبًا بسرطان القنوات الغازي. وهو أكثر أنواع سرطان الثدي شيوعًا.
يتم تشخيص سرطان الثدي الغازي عندما لا يلبي الورم معايير نوع فرعي محدد من سرطان الثدي، مثل سرطان مفصص الغازية، سرطان أنبوبي، سرطان غربي، سرطان مخاطي، سرطان غدي كيسي مخاطي، سرطان حليمي مجهري غازي، سرطان مع تمايز إفرازي، أو سرطان الخلايا الحرشفية.
ما هي أعراض سرطان الثدي الغازي؟
يمكن أن تختلف أعراض سرطان الثدي الغازي، ولكن الأعراض الشائعة تشمل:
- كتلة أو كتلة: العرض الأكثر شيوعًا هو وجود كتلة أو كتلة جديدة في الثدي. غالبًا ما تكون هذه الكتل صلبة وغير منتظمة الشكل، ولكنها قد تكون أيضًا ناعمة أو مستديرة.
- التغيرات في شكل الثدي أو حجمه: أي تغير ملحوظ في حجم أو شكل أو مظهر الثدي.
- تغييرات الجلد: نقر أو تجعد أو احمرار في جلد الثدي.
- تغيرات الحلمة: انقلاب الحلمة، أو إفرازات (خاصة إذا كانت دموية)، أو تغيرات في مظهر الحلمة.
- الم: على الرغم من أن ألم الثدي يرتبط بشكل أكثر شيوعًا بالحالات الحميدة، إلا أن بعض النساء المصابات بسرطان الأقنية الغازية قد يعانين من ألم مستمر في منطقة معينة من الثدي.
- تورم وانتفاخ: تورم جزء أو كل الثدي، حتى بدون الشعور بوجود كتلة.
- تضخم الغدد الليمفاوية: تورم أو كتل في الغدد الليمفاوية تحت الذراع أو حول عظمة الترقوة.
ما هي أسباب سرطان الثدي الغازي؟
لم يتم فهم السبب الدقيق لسرطان الثدي الغازي بشكل كامل، ولكن من المعروف أن هناك عدة عوامل تزيد من خطر الإصابة. وتشمل هذه العوامل التأثيرات الهرمونية والغذائية والإنجابية والوراثية.
إن سرطان الثدي أكثر شيوعاً في المجتمعات التي تتبع نمط حياة "غربي"، والذي يتضمن نظاماً غذائياً عالي السعرات الحرارية غنياً بالدهون الحيوانية والبروتينات، ونشاطاً بدنياً محدوداً، والسمنة. وتشمل عوامل الخطر الأخرى الدورة الشهرية الأولى المبكرة، وانقطاع الطمث المتأخر، وقلة حالات الحمل، والتقدم في السن عند الولادة الأولى، وقصر مدة الرضاعة الطبيعية. كما يرتبط العلاج بالهرمونات البديلة بعد انقطاع الطمث واستهلاك الكحول بزيادة المخاطر، وخاصة بالنسبة لسرطانات مستقبلات الهرمونات الإيجابية.
تلعب الجينات أيضًا دورًا. الطفرات في جينات معينة، مثل B و Bتزيد الطفرات الجينية بشكل كبير من خطر الإصابة بسرطان الثدي. غالبًا ما ترتبط هذه الطفرات الجينية بأنواع فرعية معينة من سرطان الثدي. على سبيل المثال، ترتبط طفرات BRCA1 بشكل أكثر شيوعًا بسرطان الثدي الثلاثي السلبي، بينما ترتبط طفرات BRCA2 بسرطان الثدي الإيجابي لمستقبلات الهرمونات. بالإضافة إلى ذلك، قد تؤثر عوامل مثل وزن الجسم والنشاط البدني على المخاطر بشكل مختلف بالنسبة لأنواع فرعية مختلفة من سرطان الثدي.
كيف يتم هذا التشخيص؟
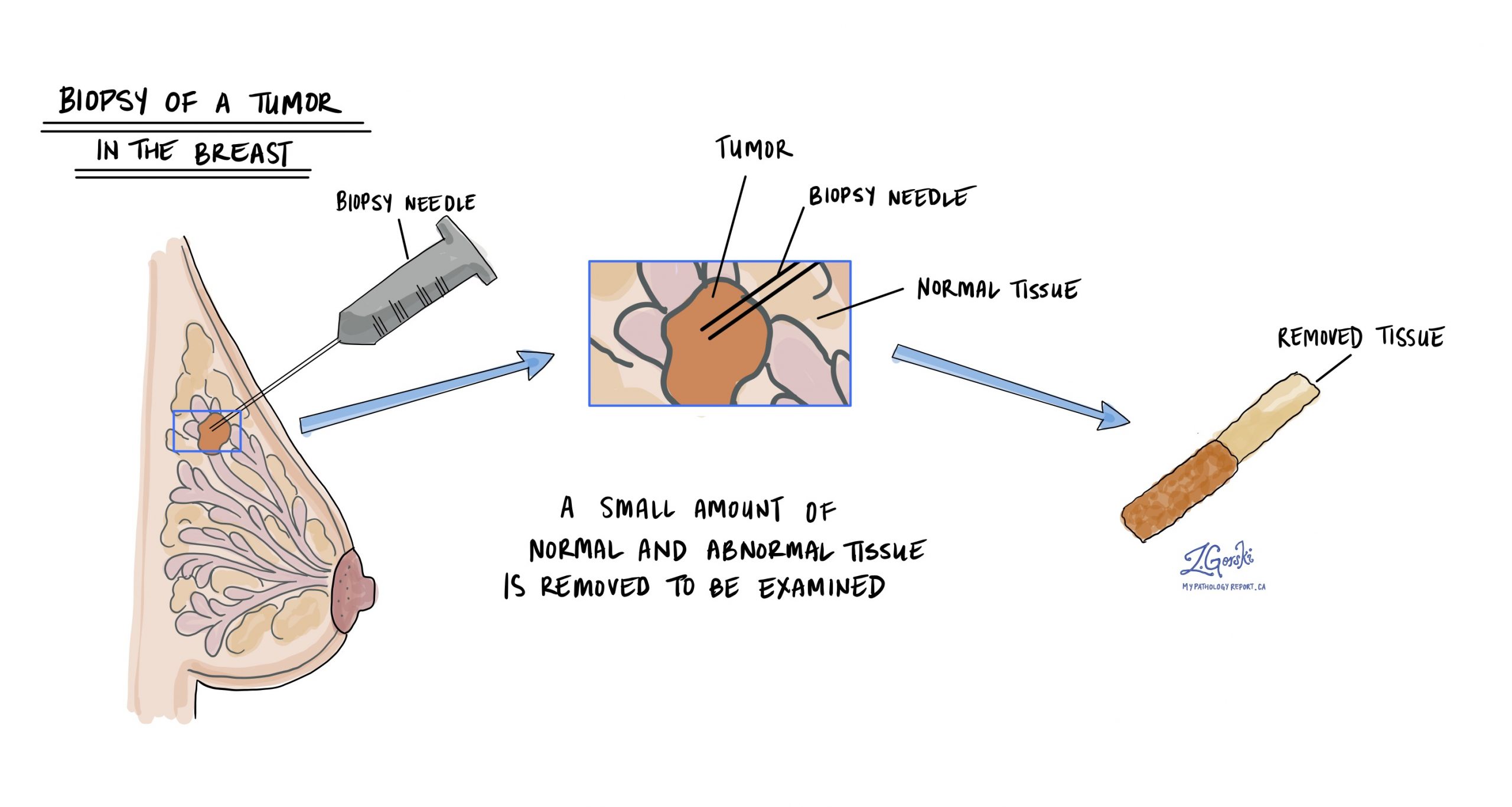
يتم تشخيص سرطان الثدي الغازي عادة بعد إزالة عينة صغيرة من الورم في إجراء يسمى خزعة. ثم يتم إرسال الأنسجة إلى أخصائي علم الأمراض لفحصها تحت المجهر. قد يُعرض عليك بعد ذلك إجراء عملية جراحية إضافية لإزالة الورم تمامًا.
الصف النسيجي نوتنغهام
تصنيف نوتنغهام النسيجي هو نظام يستخدم لتقييم مدى عدوانية سرطان الثدي الغازي من خلال فحص الخلايا السرطانية تحت المجهر. يتم تحديد التصنيف من خلال النظر إلى ثلاث سمات محددة:
- تشكيل النبيبات: يشير هذا إلى مقدار الورم الذي يتكون من هياكل مستديرة تشبه الغدة تسمى الأنابيب. الأورام التي تحتوي على عدد أكبر من الأنابيب تميل إلى أن تكون أقل عدوانية.
- تعدد الأشكال النووية: وهذا يصف مدى غير طبيعي الخلايا السرطانية نواة (جزء الخلية الذي يحتوي على الحمض النووي) يبدو بالمقارنة مع الخلايا الطبيعية ومدى التباين بين الخلايا. كلما بدا الأمر غير طبيعي، كلما ارتفعت الدرجة.
- معدل الانقسام: يقيس هذا عدد الخلايا الموجودة في الورم التي تنقسم لتكوين خلايا جديدة. عدد أكبر من الشخصيات الانقسامية يشير إلى ورم أكثر عدوانية.
يتم إعطاء كل من هذه الميزات درجة من 1 إلى 3، ويتم جمع الدرجات معًا لتحديد الدرجة النهائية:
- الصف الأول (درجة منخفضة): تنمو هذه الأورام بشكل أبطأ وأقل احتمالاً لنموها ينتشر كالسرطان (انتشار) إلى الغدد الليمفاوية.
- الصف الثاني (الصف المتوسط): تنمو هذه الأورام بشكل معتدل وأكثر عدوانية، مع زيادة خطر الإصابة بالسرطان تفشي إلى الغدد الليمفاوية.
- الصف الثالث (الدرجة العالية): تميل هذه الأورام إلى النمو بسرعة وترتبط بارتفاع خطر الإصابة بالأمراض النقيلية.
حجم الورم
حجم ورم الثدي مهم لأنه يستخدم لتحديد مرحلة الورم المرضي (pT) ولأن الأورام الأكبر حجما من المرجح أن تنتشر (تنتشر) إلى الغدد الليمفاوية وأجزاء أخرى من الجسم. لا يمكن تحديد حجم الورم إلا بعد إزالة الورم بأكمله. لهذا السبب، لن يتم تضمينه في تقرير علم الأمراض الخاص بك بعد أ خزعة.
العلامات التنبؤية لسرطان الثدي
العلامات النذير هي بروتينات أو عناصر بيولوجية أخرى يمكن قياسها للمساعدة في التنبؤ بكيفية سلوك مرض مثل السرطان بمرور الوقت وكيف سيستجيب للعلاج. العلامات النذير الأكثر شيوعًا التي يتم اختبارها في الثدي هي مستقبلات الهرمون مستقبلات هرمون الاستروجين (ER) و مستقبلات البروجسترون (PR) وعامل النمو HER2.
مستقبلات الهرمونات – ER و PR
ER (مستقبلات هرمون الاستروجين) و العلاقات العامة (مستقبلات هرمون البروجسترون) هي بروتينات موجودة في بعض خلايا سرطان الثدي. ترتبط هذه المستقبلات بهرموني الإستروجين والبروجسترون على التوالي. عندما ترتبط هذه الهرمونات بمستقبلاتها، يمكنها تحفيز الخلايا السرطانية على النمو. يمكن تصنيف سرطان الثدي الغازي حسب وجود أو غياب هذه المستقبلات، وهو أمر مهم لتحديد خيارات العلاج والتشخيص.
لماذا يعد تقييم الطوارئ والعلاقات العامة مهمًا؟
إن وجود ER و PR في خلايا سرطان الثدي يعني أن السرطان إيجابي لمستقبلات الهرمون. غالبًا ما يتم علاج هذا النوع من السرطان بالعلاج الهرموني (الغدد الصماء)، الذي يمنع قدرة الخلايا السرطانية على استخدام الهرمونات. تشمل العلاجات الهرمونية الشائعة عقار تاموكسيفين، ومثبطات الأروماتاز (مثل أناستروزول، وليتروزول، وإكسيميستان)، والأدوية التي تخفض مستويات الهرمون أو تمنع المستقبلات. غالبًا ما تستجيب السرطانات ذات المستقبلات الهرمونية الإيجابية بشكل جيد لهذه العلاجات.
سرطانات الثدي ذات مستقبلات الهرمونات الإيجابية عادة ما تكون أفضل المراجع من السرطانات سلبية مستقبلات الهرمون. إنهم يميلون إلى النمو بشكل أبطأ وأقل عدوانية. بالإضافة إلى ذلك، من المرجح أن تستجيب السرطانات ذات المستقبلات الهرمونية الإيجابية للعلاجات الهرمونية، والتي يمكن أن تقلل من خطر تكرار المرض وتحسين النتائج على المدى الطويل.
كيف يتم تقييم الطوارئ والعلاقات العامة والإبلاغ عنها؟
يتم تقييم حالة الطوارئ والعلاقات العامة من خلال الكيمياء المناعية (IHC)، يتم إجراؤها على عينة من أنسجة الورم تم الحصول عليها من أ خزعة أو الجراحة. يقيس الاختبار وجود هذه المستقبلات الهرمونية داخل الخلايا السرطانية.
وإليك كيفية الإبلاغ عن النتائج عادةً:
- نسبة الخلايا الإيجابية: قد يتضمن تقريرك النسبة المئوية للخلايا السرطانية التي تحتوي على مستقبلات ER وPR. على سبيل المثال، قد يشير أحد التقارير إلى أن 80% من الخلايا السرطانية إيجابية للاستروجين و70% إيجابية للعلاقات العامة.
- شدة تلطيخ: تعكس شدة التلوين (ضعيفة أو متوسطة أو قوية) عدد المستقبلات الموجودة في نواة من الخلايا السرطانية. يمكن أن يساعد هذا في تحديد احتمالية الاستجابة للعلاج الهرموني.
- درجة Allred أو درجة H: قد تستخدم بعض التقارير نظام تسجيل مثل درجة Allred أو درجة H، والتي تجمع بين النسبة المئوية للخلايا الإيجابية وشدة التلوين لإعطاء النتيجة الإجمالية. تشير الدرجات الأعلى إلى احتمالية أكبر لفعالية العلاج الهرموني.
HER2
HER2، أو مستقبل عامل نمو البشرة البشري 2، هو بروتين موجود على سطح بعض خلايا سرطان الثدي. له دور في نمو الخلايا وانقسامها. في بعض سرطانات الثدي، يتم تضخيم جين HER2، مما يؤدي إلى الإفراط في إنتاج بروتين HER2. يشار إلى هذه الحالة باسم سرطان الثدي الإيجابي HER2.
ما أهمية تقييم HER2؟
عادةً ما يكون لسرطانات الثدي الإيجابية HER2 تشخيص مختلف مقارنة بسرطانات الثدي الإيجابية HER2. قبل ظهور العلاجات المستهدفة، كانت السرطانات الإيجابية لـ HER2 مرتبطة بتشخيص أسوأ. ومع ذلك، مع العلاجات الفعالة التي تستهدف HER2، تحسن تشخيص هؤلاء المرضى بشكل ملحوظ. تساعد معرفة حالة HER2 أيضًا في التخطيط للإدارة الشاملة للمرض. على سبيل المثال، بالإضافة إلى العلاج الموجه، قد يتلقى المرضى المصابون بـ HER2 مزيجًا من العلاج الكيميائي والعلاجات الأخرى المصممة خصيصًا لملفهم السرطاني المحدد.
كيف يتم تقييم HER2 في سرطان الثدي الغازي؟
يتم تقييم حالة HER2 من خلال الاختبارات التي يتم إجراؤها على عينة من أنسجة الورم، والتي يمكن الحصول عليها من خلال خزعة أو أثناء الجراحة. الاختباران الرئيسيان المستخدمان هما:
- الكيمياء المناعية (IHC): يقيس هذا الاختبار كمية بروتين HER2 على سطح الخلايا السرطانية. يتم الإبلاغ عن النتائج كنتيجة من 0 إلى 3+. تعتبر النتيجة 0 أو 1+ سلبية لـ HER2، و2+ تعتبر حدًا، و3+ تعتبر إيجابية HER2.
- التهجين الفلوري في الموقع (FISH): يبحث هذا الاختبار عن عدد نسخ الجين HER2 داخل الخلايا السرطانية. غالبًا ما يتم استخدامه لتأكيد نتائج IHC الحدودية. إذا أظهر اختبار FISH نسخًا أكثر من الجين HER2 أكثر من المعتاد، يعتبر السرطان إيجابيًا لـ HER2.
تمديد الورم
يبدأ سرطان الثدي الغازي داخل الثدي، ولكن قد ينتشر الورم إلى الجلد الذي يغطيه أو عضلات جدار الصدر. يُستخدم امتداد الورم عندما يتم العثور على خلايا الورم في الجلد أو العضلات الموجودة أسفل الثدي. يُعد امتداد الورم مهمًا لأنه يرتبط بخطر أعلى يتمثل في نمو الورم مرة أخرى بعد العلاج (الانتكاس المحلي) أو انتقال الخلايا السرطانية إلى موقع بعيد في الجسم، مثل الرئة. يُستخدم أيضًا لتحديد مرحلة الورم المرضية (pT).
غزو الأوعية الدموية اللمفاوية
غزو الأوعية اللمفاوية (LVI) في سياق سرطان الثدي الغازي يشير مصطلح سرطان الثدي إلى الخلايا السرطانية الموجودة داخل الأوعية الليمفاوية أو الأوعية الدموية بالقرب من الورم. وهذا يشير إلى أن السرطان يمكن أن ينتشر خارج موقعه الأصلي من خلال أنظمة الدورة الدموية في الجسم. لا يمكن تحديد LVI إلا بعد فحص أخصائي علم الأمراض للأنسجة تحت المجهر. يبحث أخصائيو علم الأمراض عن الخلايا السرطانية داخل تجويف الأوعية الليمفاوية أو الدموية، والتي قد تظهر على شكل مجموعات أو خلايا مفردة محاطة بمساحة واضحة، مما يشير إلى جدران الأوعية.
يعد وجود LVI عاملاً مهمًا في تشخيص سرطان الثدي. ويرتبط مع ارتفاع خطر التكرار و ورم خبيثحيث يمكن للخلايا السرطانية أن تنتقل إلى أجزاء بعيدة من الجسم عن طريق الجهاز اللمفاوي أو مجرى الدم. غالبًا ما تؤدي هذه النتيجة إلى اتباع نهج علاجي أكثر عدوانية، والذي قد يشمل علاجًا كيميائيًا إضافيًا، أو علاجًا إشعاعيًا، أو علاجًا مستهدفًا، اعتمادًا على عوامل أخرى مثل المرحلة الإجمالية للسرطان، وحالة مستقبلات الهرمون، وحالة HER2.

هوامش
في علم الأمراض، الهامش هو حافة قطع الأنسجة عند إزالة الورم من الجسم. تعتبر الهوامش الموضحة في تقرير علم الأمراض مهمة جدًا لأنها تخبرك ما إذا كان الورم بأكمله قد تمت إزالته أو ما إذا كان جزء من الورم قد تم تركه. ستحدد حالة الهامش العلاج الإضافي (إن وجد) الذي قد تحتاجه.
تصف معظم تقارير علم الأمراض الهوامش فقط بعد إجراء جراحي يسمى استئصال or استئصال تم إجراؤها لإزالة الورم بأكمله. لهذا السبب، لا يتم وصف الهوامش عادة بعد أ خزعة يتم إجراؤه لإزالة جزء فقط من الورم. يعتمد عدد الهوامش الموصوفة في تقرير علم الأمراض على أنواع الأنسجة التي تمت إزالتها وموقع الورم. يعتمد حجم الهامش (كمية الأنسجة الطبيعية بين الورم والحافة المقطوعة) على نوع الورم الذي تتم إزالته وموقع الورم.
يقوم علماء الأمراض بفحص الهوامش بعناية للبحث عن الخلايا السرطانية عند الحافة المقطوعة للنسيج. إذا شوهدت الخلايا السرطانية عند الحافة المقطوعة للنسيج، فسيتم وصف الهامش بأنه إيجابي. إذا لم يتم رؤية أي خلايا سرطانية عند الحافة المقطوعة للنسيج، فسيتم وصف الهامش بأنه سلبي. حتى لو كانت جميع الهوامش سلبية، فإن بعض تقارير علم الأمراض ستقيس أيضًا أقرب الخلايا السرطانية إلى الحافة المقطوعة للنسيج.
يعد الهامش الإيجابي (أو القريب جدًا) مهمًا لأنه يعني أنه ربما تكون الخلايا السرطانية قد تُركت في جسمك عند إزالة الورم جراحيًا. لهذا السبب، قد يُعرض على المرضى ذوي الهامش الإيجابي إجراء عملية جراحية أخرى لإزالة بقية الورم أو العلاج الإشعاعي لمنطقة الجسم ذات الهامش الإيجابي.

العقد الليمفاوية
العقد الليمفاوية هي هياكل صغيرة على شكل حبة الفول وهي جزء من جهاز المناعة. وهي تعمل كمرشحات، حيث تحبس البكتيريا والفيروسات والخلايا السرطانية. تحتوي العقد الليمفاوية على خلايا مناعية يمكنها مهاجمة وتدمير المواد الضارة الموجودة في السائل الليمفاوي، الذي يدور في جميع أنحاء الجسم.
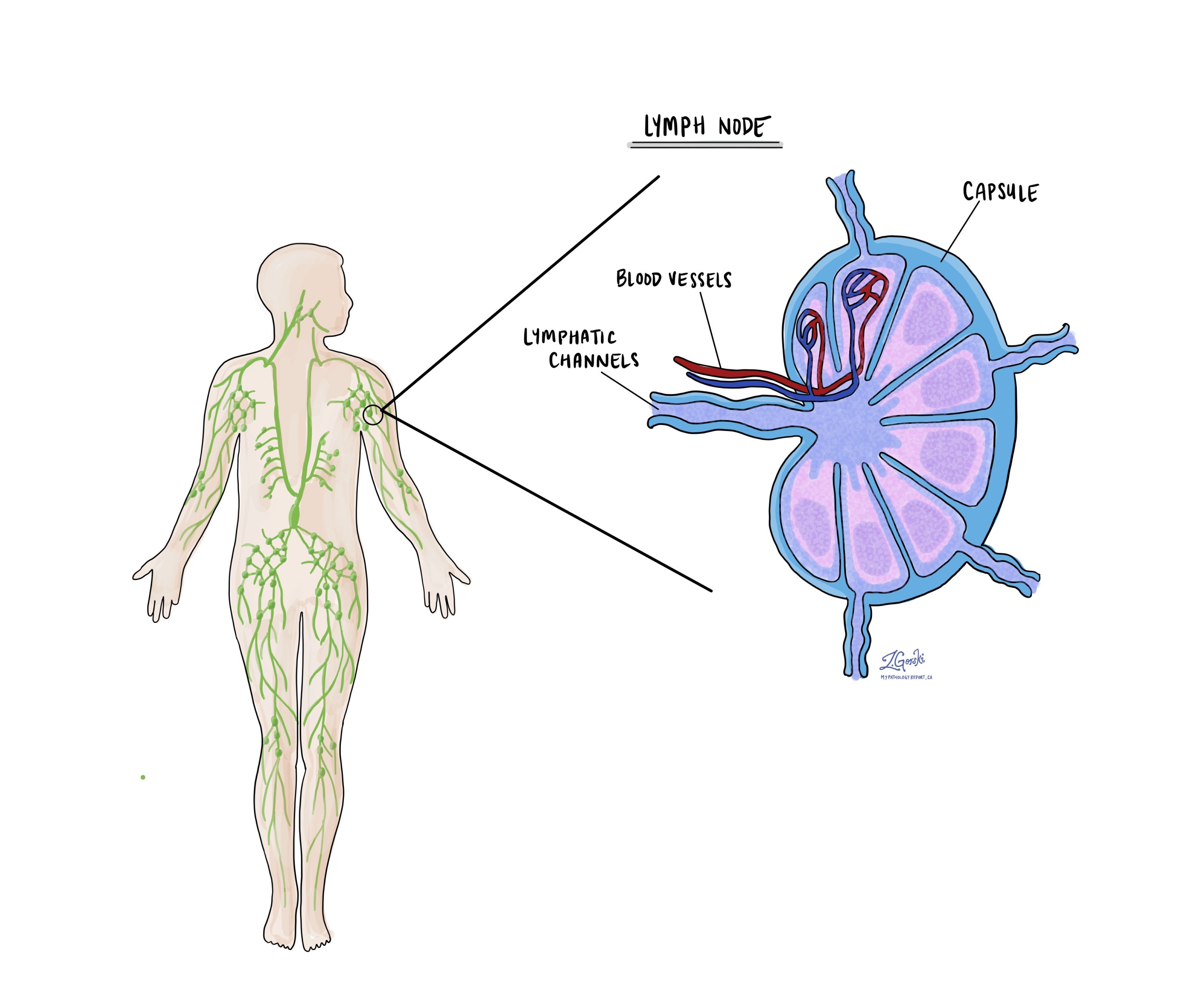
ما سبب أهمية فحص العقد الليمفاوية؟
يعد فحص الغدد الليمفاوية أمرًا مهمًا لفهم انتشار سرطان الثدي الغازي. عندما ينتشر سرطان الثدي، فإنه غالبًا ما ينتقل أولاً إلى الغدد الليمفاوية القريبة قبل الوصول إلى أجزاء أخرى من الجسم. من خلال فحص هذه الغدد الليمفاوية، يمكن لطبيبك الشرعي تحديد ما إذا كان السرطان قد انتشر خارج الثدي. تُستخدم هذه المعلومات لتحديد مرحلة السرطان والتخطيط للعلاج وتقييمه. المراجع. إذا تم العثور على السرطان في الغدد الليمفاوية، فقد يشير ذلك إلى زيادة خطر تكرار المرض والحاجة إلى علاج أكثر عدوانية.
ما هي الغدد الليمفاوية التي يتم فحصها عادة لدى المرضى المصابين بسرطان الثدي الغازي؟
بالنسبة للمرضى المصابين بسرطان الثدي الغازي، فإن الغدد الليمفاوية التي يتم فحصها عادةً تشمل:
- العقد الليمفاوية الإبطية: تقع هذه الغدد الليمفاوية تحت الذراع وهي أكثر العقد الليمفاوية شيوعًا التي يتم فحصها في سرطان الثدي. وهي مقسمة إلى مستويات بناءً على موضعها بالنسبة للعضلات الصدرية.
- العقد الليمفاوية الحارسة: هذه هي العقد الليمفاوية القليلة الأولى التي من المحتمل أن تنتشر إليها الخلايا السرطانية من الورم الرئيسي. خزعة العقدة الليمفاوية الخافرة هي إجراء يتم فيه إزالة عقدة واحدة أو بضع عقد واختبارها بحثًا عن الخلايا السرطانية.
- الغدد الليمفاوية الثديية الداخلية: وتقع هذه الغدد بالقرب من عظمة الصدر ويتم فحصها في بعض الأحيان، خاصة إذا تم العثور على السرطان في الغدد الليمفاوية الخافرة أو إذا أشارت اختبارات التصوير إلى تورطها.
كيف سيتم الإبلاغ عن نتائج فحص العقدة الليمفاوية؟
سيتم تفصيل نتائج فحص العقدة الليمفاوية في تقرير التشريح المرضي الخاص بك.
وسيتضمن التقرير معلومات عن:
- عدد العقد الليمفاوية التي تم فحصها: إجمالي عدد الغدد الليمفاوية التي تمت إزالتها وفحصها.
- عدد العقد الليمفاوية الإيجابية: عدد الغدد الليمفاوية التي تحتوي على خلايا سرطانية.
- حجم الوديعة: سيتضمن تقريرك عادةً حجم أكبر رواسب ورم موجودة في العقدة الليمفاوية.
- غيرها من الميزات: في بعض الأحيان، ميزات إضافية، مثل التمديد الخارجي (ينتشر السرطان خارج العقدة الليمفاوية).
ما هي الخلايا السرطانية المعزولة؟
يستخدم علماء الأمراض مصطلح "خلايا الورم المعزولة" لوصف مجموعة من خلايا الورم التي يبلغ قياسها 0.2 مم أو أقل وتوجد في عقدة لمفاوية. لا يتم اعتبار الغدد الليمفاوية التي تحتوي على خلايا ورم معزولة فقط (ITCs) على أنها "إيجابية" بالنسبة للمرحلة العقدية المرضية (pN).
ما هو ورم خبيث؟
"النقائل الدقيقة" هي مجموعة من خلايا الورم التي يبلغ حجمها من 0.2 مم إلى 2 مم والتي توجد في عقدة لمفاوية. إذا تم العثور على micrometastases فقط في جميع العقد الليمفاوية التي تم فحصها ، فإن المرحلة العقدية المرضية هي pN1mi.
ما هو ورم خبيث كبير؟
"النقائل الكبيرة" عبارة عن مجموعة من الخلايا السرطانية يزيد حجمها عن 2 مم وتوجد في عقدة لمفاوية. ترتبط الأورام اللحمية الكبيرة بما هو أسوأ المراجع وقد تتطلب علاجًا إضافيًا.
مؤشر عبء السرطان المتبقي
يقيس مؤشر العبء المتبقي للسرطان (RCB) كمية السرطان المتبقية في الثدي والعقد الليمفاوية القريبة بعد العلاج المساعد (العلاج المقدم قبل الجراحة). يجمع المؤشر بين العديد من السمات المرضية في درجة واحدة ويصنف استجابة السرطان للعلاج. تم تطوير هذا المؤشر من قبل الأطباء في مركز إم دي أندرسون للسرطان بجامعة تكساس (http://www.mdanderson.org/breastcancer_RCB).
هكذا يتم حساب المؤشر:
السمات المرضية المستخدمة في مؤشر RCB
- حجم فراش الورم في الثدي: يقوم أخصائيو علم الأمراض بقياس أكبر بعدين للمنطقة التي يقع فيها الورم، والتي تسمى فراش الورم. قد تحتوي هذه المنطقة على مزيج من الأنسجة الطبيعية وخلايا السرطان والنسيج الندبي الناتج عن العلاج.
- الخلية السرطانية: تقدر الخلايا السرطانية النسبة المئوية لسرير الورم الذي لا يزال يحتوي على خلايا سرطانية. ويشمل ذلك كلاً من السرطان الغازي (السرطان الذي انتشر إلى الأنسجة المحيطة) والسرطان الموضعي (الخلايا السرطانية التي لم تنتشر).
- نسبة الأمراض الموضعية: ويقوم علماء الأمراض أيضًا بتقدير نسبة السرطان الموجود في موقع الورم، أي أن الخلايا السرطانية تقتصر على قنوات الحليب أو الفصيصات ولم تنتشر إلى الأنسجة المحيطة.
- إصابة الغدد الليمفاوية: يتم حساب عدد الغدد الليمفاوية التي تحتوي على خلايا سرطانية (الغدد الليمفاوية الإيجابية)، ويتم أيضًا قياس حجم أكبر مجموعة من الخلايا السرطانية في الغدد الليمفاوية.
يتم الجمع بين هذه الميزات باستخدام صيغة موحدة لحساب مؤشر RCB.
تصنيف
بناءً على مؤشر RCB، يتم تقسيم المرضى إلى أربع فئات:
- RCB-0 (الاستجابة الكاملة المرضية): لم يتم الكشف عن أي سرطان متبقي غازي في الثدي أو الغدد الليمفاوية.
- RCB-I (الحد الأدنى من العبء): يوجد القليل جدًا من السرطان المتبقي.
- RCB-II (عبء معتدل): تبقى كمية معتدلة من السرطان.
- RCB-III (عبء واسع النطاق): تبقى كمية كبيرة من السرطان في الثدي أو الغدد الليمفاوية.
التنبؤ بالبقاء على قيد الحياة خاليا من الأمراض
يساعد تصنيف RCB في التنبؤ باحتمالية بقاء المريض خاليًا من السرطان بعد العلاج. عادةً ما يحصل المرضى الذين يحملون تصنيف RCB-0 على أفضل النتائج، مع أعلى فرص للبقاء على قيد الحياة على المدى الطويل دون تكرار الإصابة. ومع زيادة فئة RCB من RCB-I إلى RCB-III، يزداد خطر تكرار الإصابة بالسرطان، مما قد يستدعي علاجات إضافية لتقليل هذا الخطر.
المرحلة المرضية لسرطان الثدي الغازي
يساعد نظام تحديد المرحلة المرضية لسرطان الثدي الغازي الأطباء على فهم مدى انتشار السرطان والتخطيط لأفضل علاج. يستخدم النظام بشكل أساسي نظام تحديد المرحلة TNM، والذي يرمز إلى الورم والعقد والنقائل. قد تتطلب السرطانات في المرحلة المبكرة (مثل T1 أو N0) الجراحة وربما الإشعاع فقط، بينما قد تحتاج المراحل الأكثر تقدمًا (مثل T3 أو N3) إلى مزيج من الجراحة والإشعاع والعلاج الكيميائي والعلاجات المستهدفة. يضمن تحديد المرحلة المناسب حصول المرضى على العلاجات الأكثر فعالية بناءً على مدى مرضهم، مما قد يحسن معدلات البقاء على قيد الحياة ونوعية الحياة.
مرحلة الورم (pT)
تقوم هذه الميزة بفحص حجم ومدى ورم الثدي. يتم قياس الورم بالسنتيمتر، ويتم تقييم نموه خارج أنسجة الثدي.
T0: لا يوجد دليل على وجود ورم أولي. وهذا يعني أنه لا يمكن العثور على ورم في الثدي.
T1: يبلغ حجم الورم 2 سم أو أصغر في البعد الأكبر. وتنقسم هذه المرحلة أيضًا إلى:
- T1mi: حجم الورم 1 ملم أو أصغر.
- T1a: حجم الورم أكبر من 1 ملم ولكن لا يزيد عن 5 ملم.
- T1b: حجم الورم أكبر من 5 ملم ولكن لا يزيد عن 10 ملم.
- T1ج: حجم الورم أكبر من 10 ملم ولكن لا يزيد عن 20 ملم.
T2: حجم الورم أكبر من 2 سم ولكن لا يزيد عن 5 سم.
T3: حجم الورم أكبر من 5 سم.
T4: انتشر الورم إلى جدار الصدر أو الجلد، بغض النظر عن حجمه. وتنقسم هذه المرحلة أيضًا إلى:
- T4a: لقد غزا الورم جدار الصدر.
- T4b: انتشار الورم إلى الجلد، مما يسبب تقرحات أو تورم.
- T4ج: كلا T4a وT4b موجودان.
- T4د: سرطان الثدي الالتهابي، والذي يتميز باحمرار وتورم جلد الثدي.
المرحلة العقدية (pN)
تفحص هذه الميزة ما إذا كان السرطان قد انتشر إلى مكان قريب الغدد الليمفاويةوهي عبارة عن هياكل صغيرة على شكل حبة الفول توجد في جميع أنحاء الجسم.
N0: لا يوجد سرطان في الغدد الليمفاوية القريبة.
N1: انتشر السرطان إلى 1 إلى 3 عقد ليمفاوية إبطية (تحت الذراع).
N2: انتشر السرطان إلى:
- N2a: من 4 إلى 9 عقد ليمفاوية إبطية.
- رقم 2ب: الغدد الليمفاوية الثديية الداخلية دون تورط الغدد الليمفاوية الإبطية.
N3: انتشر السرطان إلى:
- N3a: 10 أو أكثر من العقد الليمفاوية الإبطية أو عقدتين ليمفاويتين تحت الترقوة (تحت الترقوة).
- رقم 3ب: الغدد الليمفاوية الثديية الداخلية والغدد الليمفاوية الإبطية.
- ن3ج: الغدد الليمفاوية فوق الترقوة (فوق الترقوة).
ما هو تشخيص الشخص الذي تم تشخيصه بسرطان الثدي الغازي؟
يعتمد تشخيص سرطان الثدي الغازي على عدة عوامل، بما في ذلك مرحلة المرض وخصائص الورم وخيارات العلاج. فيما يلي بعض أهم العوامل التي تؤثر على النتائج:
مرحلة الورم وحجمه
إن أحد أهم مؤشرات البقاء على قيد الحياة هو مرحلة السرطان، والتي تصف مدى انتشاره. إن الأورام الصغيرة والمقتصرة على الثدي في مراحلها المبكرة تتمتع بتوقعات أفضل. على سبيل المثال، فإن معدل البقاء على قيد الحياة لمدة 5 سنوات لسرطان الثدي الموضعي يتجاوز 95%. ومع ذلك، تنخفض معدلات البقاء على قيد الحياة إذا انتشر السرطان إلى العقد الليمفاوية أو الأعضاء البعيدة.
درجة الورم
تصف درجة الورم مدى عدم طبيعية الخلايا السرطانية التي تظهر تحت المجهر. تنمو الأورام عالية الدرجة وتنتشر بسرعة أكبر وقد تكون نتائجها أقل ملاءمة.
مستقبلات الهرمونات وحالة HER2
إن سرطانات مستقبلات الهرمونات الإيجابية، والتي تنمو استجابة للإستروجين أو البروجسترون، غالباً ما يكون تشخيصها أفضل لأنها يمكن علاجها بالعلاجات الهرمونية. أما سرطانات مستقبلات HER2 الإيجابية فهي أكثر عدوانية ولكنها قد تستجيب بشكل جيد للعلاجات المستهدفة مثل عقار تراستوزوماب. أما سرطانات الثدي الثلاثية السلبية (التي تفتقر إلى مستقبلات الإستروجين والبروجسترون وHER2) فهي أكثر صعوبة في العلاج وقد يكون تشخيصها أقل ملاءمة.
غزو الأوعية الدموية اللمفاوية
تزيد الخلايا السرطانية الموجودة في الأوعية الدموية أو الأوعية اللمفاوية القريبة من الورم من خطر انتشار السرطان وقد تؤثر على قرارات العلاج.
الهوامش المرضية
يؤثر اكتمال إزالة الورم أثناء الجراحة على خطر تكرار الإصابة. فالأورام التي تتم إزالتها بالكامل دون وجود خلايا سرطانية على حواف العينة الجراحية تكون أقل عرضة لتكرار الإصابة محليًا.
مؤشر وضع العلامات Ki-67
استخدم مؤشر وضع العلامات Ki-67 يقيس هذا المؤشر سرعة انقسام الخلايا السرطانية. يشير مؤشر Ki-67 الأعلى إلى وجود ورم أكثر عدوانية وقد يؤثر على القرارات المتعلقة بالعلاج الكيميائي.
الاختبارات الجينية
قد يستفيد بعض المرضى من إجراء اختبار جيني للورم للمساعدة في التنبؤ بخطر تكرار الإصابة. يمكن أن تساعد الاختبارات مثل درجة تكرار الإصابة بـ 21 جينًا أو التوقيع الجيني 70 في تحديد المرضى الذين قد يستفيدون من علاجات إضافية مثل العلاج الكيميائي.
حالة مستقبلات الأندروجين (AR)
وقد ارتبط التعبير عن مستقبلات الأندروجين بنتائج أفضل في سرطان الثدي في مرحلة مبكرة. وقد أظهرت الدراسات أن المرضى الذين تعبر أورامهم عن مستقبلات الأندروجين قد يكون لديهم تحسن في البقاء على قيد الحياة بدون مرض والبقاء على قيد الحياة بشكل عام. ومع ذلك، فإن دور مستقبلات الأندروجين في سرطان الثدي، وخاصة في الأورام الإيجابية لمستقبلات الإستروجين والسلبية لمستقبلات الإستروجين، معقد. وفي حين أن مستقبلات الأندروجين قد تكون واعدة كهدف للعلاجات الهرمونية أو القائمة على الأندروجين، إلا أن الأدلة لا تزال قيد التحقيق. ونتيجة لذلك، لا يتم إجراء اختبار مستقبلات الأندروجين بشكل روتيني ولكن يمكن النظر فيه في حالات سريرية محددة.
الاستجابة للعلاج المساعد
إن الاستجابة للعلاج المساعد قبل الجراحة، وهو العلاج الذي يتم إعطاؤه قبل الجراحة، يمكن أن توفر معلومات تشخيصية مهمة. إن تحقيق استجابة مرضية كاملة (عدم اكتشاف أي سرطان متبقي بعد العلاج) هو مؤشر قوي لنتائج أفضل، وخاصة بالنسبة لسرطانات الثدي الإيجابية لـ HER2 والثلاثية السلبية. بالنسبة للمرضى الذين يعانون من مرض متبقي بعد العلاج المساعد، يمكن استخدام مؤشر عبء السرطان المتبقي لتقدير خطر تكرار المرض. يأخذ هذا المؤشر في الاعتبار عوامل مثل حجم الورم، وإصابة العقد الليمفاوية، ومدى السرطان المتبقي ويوجه قرارات العلاج الإضافية.



