por Jason Wasserman MD PhD FRCPC
Febrero 4, 2026
Carcinoma de células de Hürthle Es un tipo raro de cáncer de tiroides que se origina en las células foliculares, que producen la hormona tiroidea. Este tumor se compone principalmente de células de Hürthle (también llamadas células oncocíticas), que son más grandes que las células tiroideas normales y se ven rosadas y granulares al microscopio debido a su gran cantidad de mitocondrias. Estas estructuras producen energía para la célula.
El carcinoma de células de Hürthle ahora se denomina con mayor precisión carcinoma oncocítico en la patología moderna. Ambos términos describen la misma enfermedad, pero carcinoma oncocítico Se prefiere porque refleja mejor la biología del tumor. Es posible que aún vea el término carcinoma de células de Hürthle en historias clínicas, informes de imágenes o informes patológicos antiguos.
Este artículo explica cómo se diagnostica, clasifica y examina el carcinoma de células de Hürthle bajo el microscopio, y cómo estos hallazgos se relacionan con el pronóstico y el seguimiento.
¿Dónde se origina el carcinoma de células de Hürthle?
La mayoría de los carcinomas de células de Hürthle se originan en la glándula tiroides. En raras ocasiones, los tumores pueden desarrollarse en tejido tiroideo ectópico, es decir, tejido tiroideo que se formó fuera de su ubicación habitual durante el desarrollo. Algunos ejemplos son la lengua (tiroides lingual) o el tórax (mediastino).
¿Cuáles son los síntomas del carcinoma de células de Hürthle?
Muchos pacientes notan un nódulo tiroideo indoloro que crece lentamente. Los tumores con invasión limitada suelen descubrirse casualmente durante una exploración física de rutina o mediante imágenes.
Los tumores más grandes o más invasivos pueden causar:
-
Una masa visible o palpable en el cuello.
-
Presión o tirantez en el cuello.
-
Dificultad para tragar o respirar.
-
Ronquera.
La mayoría de los pacientes tienen niveles normales de hormona tiroidea, por lo que los síntomas de función tiroidea hiperactiva o hipoactiva son poco comunes.
¿Cómo se hace este diagnóstico?
El diagnóstico del carcinoma de células de Hürthle requiere varios pasos porque este tumor no se puede diagnosticar definitivamente únicamente mediante imágenes o biopsia con aguja.
El proceso de diagnóstico puede incluir:
-
Estudios de imagen.
-
Extirpación quirúrgica del tumor.
-
Examen microscópico cuidadoso de la cápsula tumoral y los vasos sanguíneos.
Cada paso proporciona información importante, pero el diagnóstico final casi siempre se realiza después de la cirugía.
Proyección de imagen
La ecografía suele ser la primera prueba de diagnóstico por imagen. El carcinoma de células de Hürthle no se puede distinguir con fiabilidad de los tumores benignos. Adenoma de células de Hürthle Solo por ecografía. Muchos tumores aparecen como nódulos sólidos con un halo circundante creado por la cápsula tumoral.
Los tumores que se extienden más allá de la cápsula pueden presentar márgenes irregulares o invasión de tejidos cercanos. La mayoría de los carcinomas de células de Hürthle son hipofuncionantes (fríos) en las gammagrafías con yodo radiactivo, aunque existen tumores funcionantes poco frecuentes. Muchos son ávidos de FDG-PET, lo que significa que captan glucosa en las imágenes PET.
Aspiración con aguja fina (PAAF)
La PAAF puede identificar un tumor de células de Hürthle, pero no puede determinar si el tumor es benigno or malignoEsto se debe a que la invasión capsular y vascular no se puede evaluar en muestras de biopsia pequeñas.
Como resultado, los informes de la FNA a menudo utilizan términos como Neoplasia de células de Hürthle or Sospechoso de neoplasia de células de Hürthle, y se requiere extirpación quirúrgica para establecer el diagnóstico.
Características microscópicas
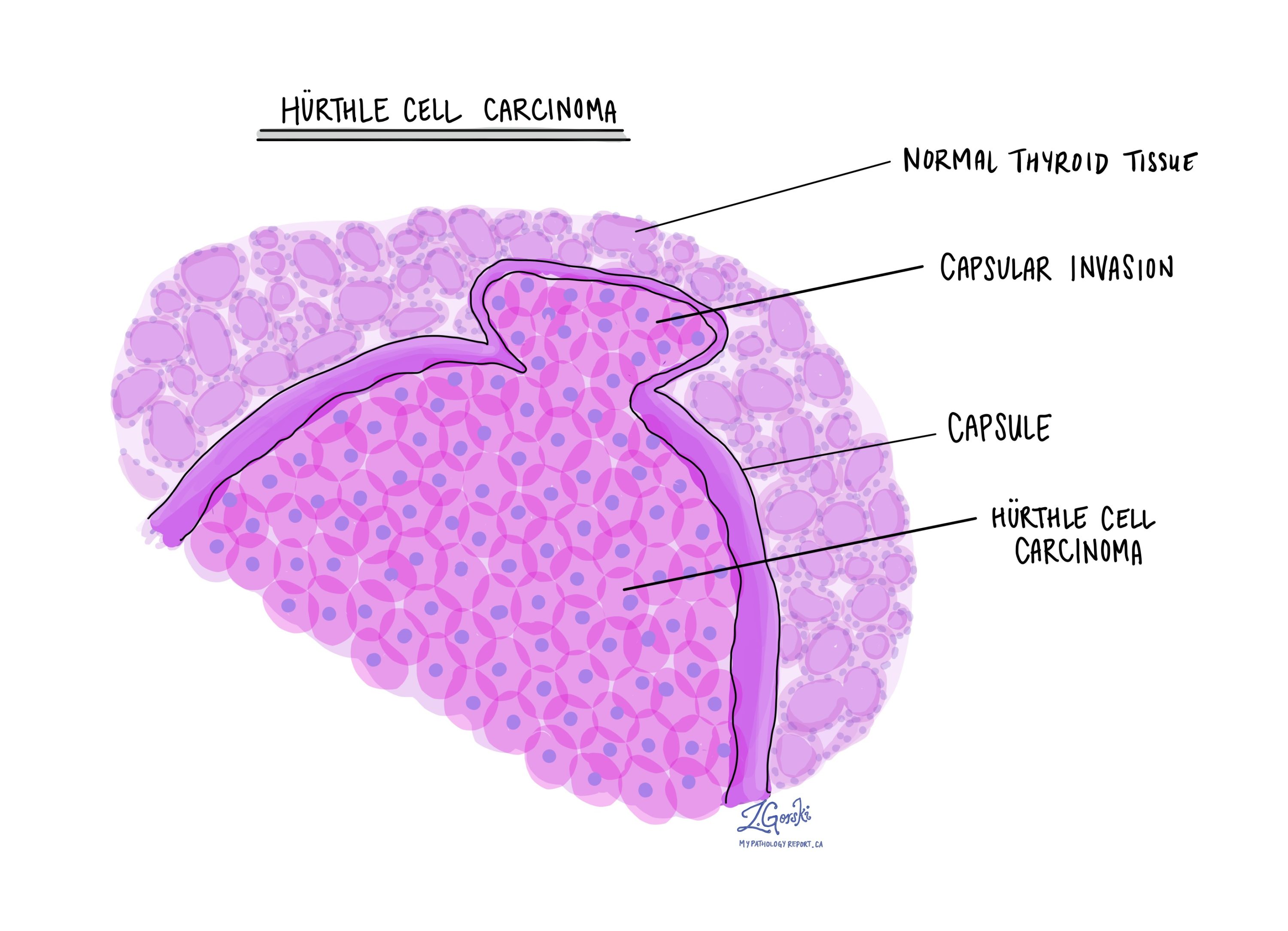
Al microscopio, el carcinoma de células de Hürthle es típicamente un tumor bien delimitado, densamente encapsulado y compuesto al menos en un 75 % de células de Hürthle (oncocíticas).
Las células tumorales presentan un citoplasma granular rosado abundante y núcleos redondos con nucléolos prominentes. Los patrones de crecimiento suelen ser sólidos o trabeculares, con menos folículos que los observados en tumores benignos. La cápsula suele ser más gruesa que la de un adenoma de células de Hürthle y puede contener calcificaciones.
Los hallazgos microscópicos más críticos son:
-
Invasión capsular, lo que significa que las células tumorales han crecido completamente a través de la cápsula.
-
Invasión vascular, lo que significa que las células tumorales se encuentran dentro de los vasos sanguíneos.
Estas características confirman que el tumor es maligno y ayudan a determinar su agresividad.
Clasificación de tumores (subtipos)
El carcinoma de células de Hürthle se subdivide según el crecimiento y la propagación del tumor. Esta clasificación es importante porque predice con precisión el comportamiento, el riesgo de recurrencia y la probabilidad de propagación a distancia.
Carcinoma de células de Hürthle mínimamente invasivo
Este subtipo presenta únicamente invasión capsular, sin invasión de vasos sanguíneos. Por lo demás, el tumor permanece bien contenido.
Los tumores mínimamente invasivos suelen ser indolentes y tienen un pronóstico excelente una vez extirpados por completo. A menudo no se requiere tratamiento adicional más allá de la cirugía.
Carcinoma de células de Hürthle angioinvasivo encapsulado
Estos tumores están completamente encapsulados, pero presentan invasión vascular. Los patólogos cuentan el número de vasos sanguíneos afectados y describen la invasión como:
-
Invasión vascular limitada (menos de 4 vasos).
-
Invasión vascular extensa (4 o más vasos).
Los tumores con invasión vascular limitada tienen un riesgo intermedio, mientras que aquellos con invasión vascular extensa se comportan de forma más agresiva y requieren un seguimiento más estrecho.
Carcinoma de células de Hürthle ampliamente invasivo
Los tumores ampliamente invasivos muestran una infiltración extensa en el tejido tiroideo o los tejidos blandos circundantes, a menudo con múltiples áreas de invasión vascular.
Este subtipo tiene el mayor riesgo de recurrencia y metástasis a distancia, más comúnmente en los pulmones, los huesos o el hígado, y requiere un tratamiento más intensivo y una vigilancia a largo plazo.
Invasión vascular
La invasión vascular implica la presencia de células tumorales dentro de los vasos sanguíneos, a menudo adheridas a la pared vascular o mezcladas con un coágulo sanguíneo. Esta es una de las características más importantes del carcinoma de células de Hürthle.
Los tumores sin invasión vascular suelen permanecer localizados. Por el contrario, los tumores con invasión vascular, especialmente cuando afectan múltiples vasos, presentan un riesgo significativamente mayor de diseminarse a órganos distantes. Por ello, la presencia y la extensión de la invasión vascular influyen considerablemente en el pronóstico y la planificación del tratamiento.
Extensión extratiroidea
La extensión extratiroidea significa que las células tumorales han crecido más allá de la glándula tiroides hacia los tejidos circundantes. Normalmente, una fina capa de tejido conectivo rodea la tiroides, y la mayoría de los carcinomas de células de Hürthle permanecen confinados en la glándula.
-
La extensión extratiroidea microscópica sólo puede verse mediante examen microscópico y no cambia el estadio del tumor.
-
La extensión extratiroidea macroscópica (bruta) es visible durante la cirugía o el diagnóstico por imágenes y afecta estructuras cercanas como los músculos del cuello, la tráquea o el esófago.
Sólo la extensión extratiroidea macroscópica aumenta el estadio del tumor porque se asocia con un mayor riesgo de recurrencia y puede afectar las decisiones de tratamiento.
Transformación de alto grado
En casos raros, el carcinoma de células de Hürthle puede sufrir una transformación de alto grado, lo que significa que se transforma en una forma más agresiva de cáncer de tiroides, como carcinoma de tiroides poco diferenciado o carcinoma tiroideo diferenciado de alto grado, tipo oncocítico.
Las características que sugieren una transformación de alto grado incluyen necrosis tumoral, aumento del número de células en división, figuras mitóticas anormales y pérdida de las características oncocíticas típicas. Los tumores con transformación de alto grado son más agresivos, a menudo resistentes al yodo radiactivo, y tienen un peor pronóstico.
Ganglios linfaticos
Ganglios linfaticos Son pequeños órganos inmunitarios que filtran el líquido linfático. Las células cancerosas pueden propagarse desde la tiroides a los ganglios linfáticos cercanos a través de los vasos linfáticos.
Diferente a los carcinoma folicular de tiroidesEl carcinoma de células de Hürthle puede afectar los ganglios linfáticos, aunque es menos común que se propague por vía sanguínea. Cualquier ganglio linfático extirpado durante la cirugía se examina al microscopio y se informa si hay células tumorales positivas o negativas.
La afectación de los ganglios linfáticos puede aumentar el estadio del cáncer e influir en las recomendaciones de tratamiento y vigilancia adicionales.
Estadio patológico (pTNM)
El estadio patológico del carcinoma de células de Hürthle se basa en el sistema de estadificación TNM, que considera el tumor primario (T), los ganglios linfáticos (N) y las metástasis a distancia (M). En general, los estadios más avanzados indican una enfermedad más avanzada y un peor pronóstico.
Estadio tumoral (pT)
-
T1: Tumor ≤ 2 cm, confinado a la tiroides.
-
T2: Tumor > 2 cm pero ≤ 4 cm, confinado a la tiroides.
-
T3: Tumor > 4 cm o extensión a músculos cercanos.
-
T4: El tumor se extiende a estructuras como la tráquea, la laringe o el esófago.
Estadio nodal (pN)
-
N0: No hay células tumorales en los ganglios linfáticos.
-
N1a: Células tumorales en los ganglios linfáticos centrales del cuello (niveles 6-7).
-
N1b: Células tumorales en los ganglios linfáticos laterales del cuello (niveles 1-5).
-
NX: No se examinaron ganglios linfáticos.
Pronóstico y predicción
El pronóstico del carcinoma de células de Hürthle depende principalmente de la extensión de la invasión, especialmente la invasión vascular.
Los tumores con invasión capsular solo tienen un pronóstico excelente. Los tumores con invasión vascular limitada presentan un riesgo intermedio, mientras que aquellos con invasión vascular extensa o amplia presentan un pronóstico significativamente peor.
Un pequeño porcentaje de tumores puede posteriormente transformarse en carcinoma anaplásico de tiroides, ya sea en la recurrencia o en el diagnóstico inicial, lo que conlleva un pronóstico muy malo.
Preguntas para hacerle a su médico
-
¿Mi tumor era mínimamente invasivo, angioinvasivo o ampliamente invasivo?
-
¿Había invasión vascular y qué tan extensa fue?
-
¿Necesito un tratamiento adicional como yodo radiactivo?
-
¿Cuál es mi riesgo de recurrencia o propagación?
-
¿Con qué frecuencia necesitaré imágenes o análisis de sangre de seguimiento?


