Di Jason Wasserman MD PhD FRCPC e Matt Cecchini MD PhD FRCPC
27 Novembre 2025
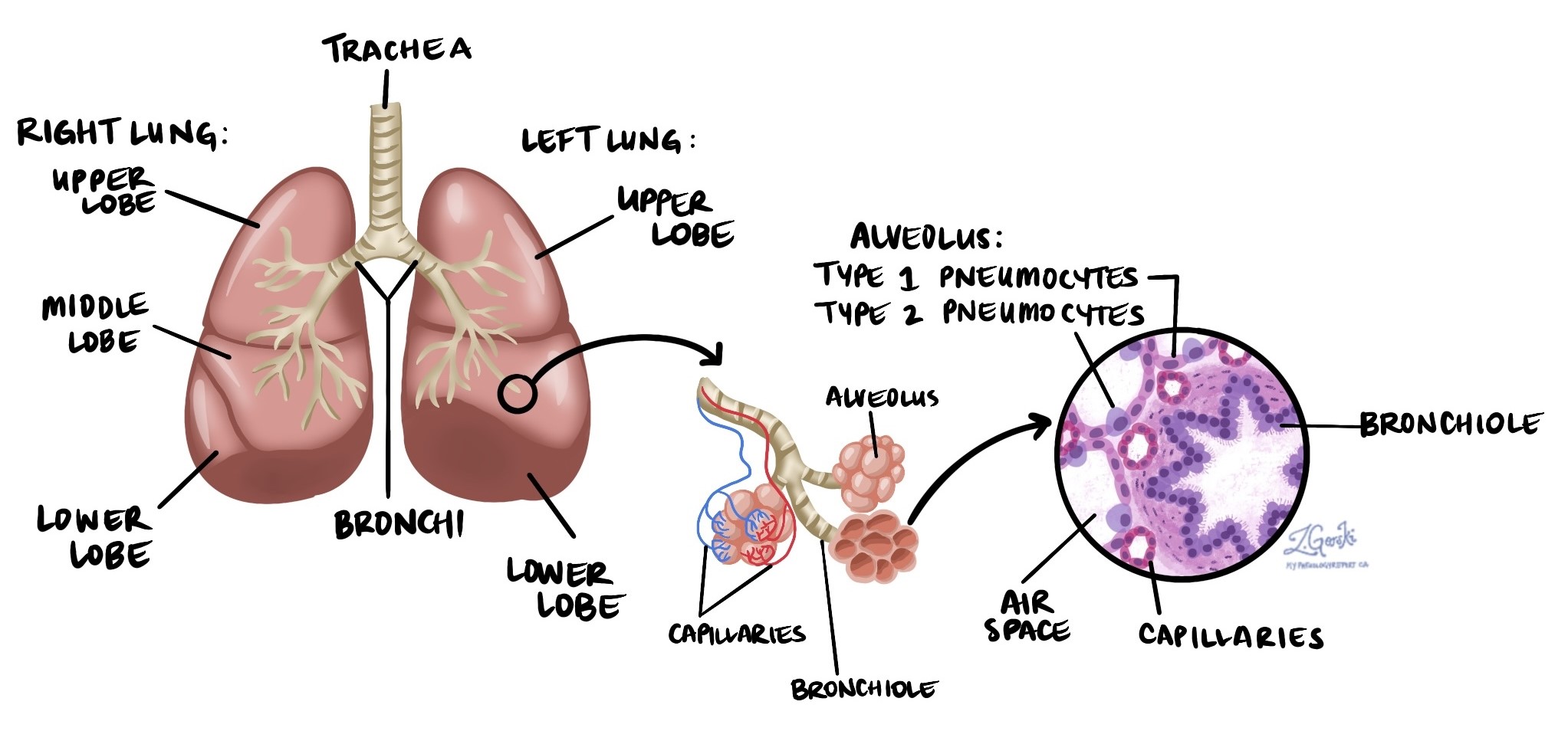
adenocarcinoma è il tipo più comune di cancro ai polmoni, rappresentando circa il 40% di tutti i casi di cancro ai polmoni in Nord America. Appartiene al gruppo di tumori noti come carcinoma polmonare non a piccole cellule (NSCLC)L'adenocarcinoma ha origine nei pneumociti, le cellule specializzate che rivestono le piccole sacche d'aria dei polmoni chiamate alveoli. Gli alveoli sono il luogo in cui l'ossigeno entra nel flusso sanguigno e l'anidride carbonica viene rimossa.
Poiché l'adenocarcinoma spesso inizia vicino ai margini esterni del polmone, può essere individuato precocemente quando gli esami di diagnostica per immagini, come radiografie o TAC, mostrano un piccolo nodulo o una massa.
Quali sono le cause dell'adenocarcinoma nel polmone?
La causa principale dell'adenocarcinoma polmonare è il fumo di tabacco. Questo include sigarette, sigari e pipa. Tuttavia, l'adenocarcinoma può svilupparsi anche in persone che non hanno mai fumato.
Altre cause e fattori di rischio includono:
-
Esposizione al radon.
-
Esposizioni professionali, come ad esempio all'amianto, alla silice o ai gas di scarico dei motori diesel.
-
Inquinamento dell'aria esterna.
Questi fattori possono danneggiare le cellule polmonari e aumentare il rischio di cancro nel tempo.
Quali sono i sintomi dell'adenocarcinoma polmonare?
I sintomi dell'adenocarcinoma polmonare variano. Alcune persone non presentano sintomi, soprattutto nelle fasi iniziali. Quando compaiono, i sintomi possono includere:
-
Tosse persistente o in peggioramento.
-
Tossendo sangue.
-
Dolore al petto
-
Mancanza di respiro
-
Stanchezza o perdita di peso involontaria.
Se il cancro si diffonde ad altre parti del corpo, i sintomi dipendono dalla sede. Ad esempio, la diffusione alle ossa può causare dolore o persino una frattura patologica, ovvero una frattura ossea causata dal cancro che indebolisce il tessuto osseo.
Quali condizioni sono associate all'adenocarcinoma del polmone?
L'adenocarcinoma del polmone può derivare da condizioni precancerose quali:
-
L'iperplasia adenomatosa atipica (AAH) è una condizione in cui le cellule che rivestono gli alveoli appaiono anomale ma non sono cancerose.
-
Adenocarcinoma in situ (AIS) è un tumore non invasivo limitato alla superficie interna degli alveoli e di dimensioni inferiori a 3 cm.
L'AIS può evolvere in adenocarcinoma invasivo quando il tumore cresce oltre i 3 cm o quando le cellule cancerose invadono il tessuto di supporto sotto il rivestimento alveolare.
Come si fa questa diagnosi?
La diagnosi di adenocarcinoma inizia quando gli esami di imaging mostrano un'area sospetta nel polmone. Per confermare la diagnosi, un biopsia Viene eseguita per rimuovere un piccolo campione di tessuto. Le biopsie possono essere ottenute tramite agobiopsia, broncoscopia, ecografia endobronchiale (EBUS) o agoaspirato (FNA). Il campione di tessuto viene quindi esaminato al microscopio da un patologo, un medico specializzato nella diagnosi di malattie attraverso lo studio dei tessuti.
Se il tumore viene confermato, potrebbe essere raccomandato un intervento chirurgico per rimuoverlo. Il tipo di intervento dipende dalle dimensioni e dalla posizione del tumore. I tumori più piccoli vicino alla superficie esterna possono essere rimossi con una resezione a cuneo, mentre i tumori più grandi o più centrali potrebbero richiedere una lobectomia o persino una pneumonectomia.
Dopo la rimozione, il patologo esamina l'intero tumore. Le caratteristiche più importanti includono:
-
Il modello di crescita (tipo istologico).
-
Se il cancro si è diffuso nel tessuto polmonare circostante.
-
Che si diffonda attraverso gli spazi aerei (STAS) è presente.
-
Se le cellule tumorali sono penetrate nei vasi sanguigni o nei canali linfatici.
-
Se il tumore si è sviluppato nella pleura.
-
Se i margini chirurgici sono puliti.
-
Se i linfonodi contengono cellule cancerose.
Immunoistochimica (IHC)
L'immunoistochimica È un test speciale che utilizza anticorpi legati a coloranti per rilevare proteine specifiche all'interno delle cellule. Queste proteine agiscono come "marcatori" che aiutano il patologo a confermare il tipo di cancro e a determinarne l'origine.
L'adenocarcinoma del polmone in genere presenta i seguenti risultati:
-
TTF-1: Positivo.
-
p40: Negativo.
-
CK5: Negativo.
-
Cromogranina: Negativo.
-
Sinaptofisina: Negativa.
Questo schema di colorazione supporta la diagnosi e aiuta a escludere altri tipi di cancro ai polmoni, come il carcinoma squamocellulare o i tumori neuroendocrini.
Tipi istologici di adenocarcinoma
L'adenocarcinoma polmonare è suddiviso in tipi istologici in base alla modalità di crescita delle cellule tumorali. Un tumore può presentare uno o più quadri clinici.
Tipo lepidico
Le cellule tumorali crescono lungo la superficie interna degli alveoli. Se completamente lepido e di dimensioni inferiori a 3 cm, il tumore è classificato come AIS.
Tipo acinoso
Le cellule tumorali formano strutture rotonde, simili a ghiandole.
Tipo solido
Le cellule tumorali crescono in strati densi con poco spazio aperto. Questo tipo è più aggressivo.
Tipo papillare
Le cellule tumorali formano delle proiezioni simili a dita chiamate papille.
Tipo micropapillare
Le cellule tumorali formano piccoli ammassi che assomigliano a ciuffi. Questo è un modello altamente aggressivo.
Grado del tumore
Per l'adenocarcinoma polmonare, il grado tumorale descrive l'aggressività del tumore al microscopio. Il grado si basa su due caratteristiche microscopiche:
-
Il modello istologico predominante.
-
Il quadro clinico peggiore (il più aggressivo) osservato in qualsiasi parte del tumore.
I tumori con crescita prevalentemente lepidica e minime caratteristiche solide o micropapillari sono ben differenziati, il che significa che crescono più lentamente e hanno una prognosi migliore. I tumori con crescita acinare o papillare e piccole quantità di pattern aggressivi sono moderatamente differenziati. I tumori che contengono grandi quantità di crescita solida o micropapillare sono scarsamente differenziati, il che significa che si comportano in modo più aggressivo, crescono più velocemente e hanno maggiori probabilità di diffondersi.
Il grado del tumore è uno dei più importanti fattori predittivi della prognosi, soprattutto nella fase iniziale della malattia.
Diffusione negli spazi aerei (STAS)
STAS significa che le cellule tumorali si trovano sospese negli spazi aerei del polmone, oltre il bordo del tumore principale. Queste cellule sono separate dalla massa primaria e possono viaggiare attraverso i piccoli canali aerei del polmone.
La presenza di STAS è associata a un rischio più elevato di recidiva, soprattutto dopo un intervento chirurgico limitato come la resezione a cuneo. Per questo motivo, STAS è incluso nel referto istologico e contribuisce a orientare le decisioni terapeutiche.
tumori multipli
È possibile trovare più di un tumore nei polmoni. In queste situazioni, ogni tumore viene esaminato separatamente. Talvolta, tumori multipli rappresentano la diffusione di un singolo tumore originale, soprattutto quando appaiono identici al microscopio. Quando piccole escrescenze secondarie compaiono nello stesso polmone del tumore primario, vengono spesso chiamate noduli, piccole lesioni rotondeggianti che possono rappresentare una diffusione metastatica all'interno del polmone.
In altri casi, i tumori potrebbero essersi formati indipendentemente, soprattutto se presentano caratteristiche o quadri istologici diversi. Ad esempio, un tumore potrebbe essere un adenocarcinoma mentre un altro un carcinoma a cellule squamose. Quando i tumori si formano separatamente, sono considerati tumori primari distinti e non metastasi. Distinguere tra queste due possibilità è importante perché influenza la stadiazione, il trattamento e la prognosi.
Invasione pleurica
La pleura è una sottile membrana composta da due strati:
-
La pleura viscerale ricopre la superficie dei polmoni.
-
La pleura parietale, che riveste l'interno della cavità toracica.
L'invasione pleurica significa che le cellule tumorali si sono sviluppate in uno o entrambi questi strati. I tumori che invadono solo la pleura viscerale sono considerati localmente più avanzati rispetto ai tumori limitati al tessuto polmonare stesso. I tumori che invadono la pleura parietale, lo strato esterno attaccato alla parete toracica, sono considerati ancora più avanzati, perché il tumore si è sviluppato oltre il polmone e ha raggiunto il rivestimento della cavità toracica. L'invasione pleurica aumenta lo stadio T ed è associata a un rischio maggiore di diffusione e recidiva.
Invasione linfovascolare
L'invasione linfovascolare (LVI) si verifica quando le cellule tumorali penetrano nei vasi sanguigni o linfatici all'interno o in prossimità del tumore. Questi vasi fungono da vie di diffusione del cancro ad altre parti del corpo, inclusi linfonodi, ossa, fegato o cervello. In presenza di invasione linfovascolare, il rischio di metastasi è maggiore e potrebbe essere raccomandato un trattamento aggiuntivo.
Margini
I margini sono i bordi del tessuto rimosso durante l'intervento chirurgico. Il patologo esamina tutti i margini per determinare se il tumore è stato rimosso completamente. Un margine negativo significa che non sono visibili cellule tumorali sul bordo di taglio. Un margine positivo significa che è presente tumore sul bordo, sollevando il timore che una parte di tumore sia ancora presente. Lo stato dei margini aiuta i medici a decidere se sia necessario un ulteriore intervento chirurgico o una radioterapia.

Linfonodi
Linfonodi Sono piccoli organi immunitari che filtrano il fluido linfatico. L'adenocarcinoma polmonare si diffonde comunemente ai linfonodi del polmone e della parte centrale del torace. Durante l'intervento chirurgico, i linfonodi provenienti da specifiche regioni anatomiche (chiamate stazioni linfonodali) possono essere rimossi ed esaminati.
Il referto istologico indicherà il numero di linfonodi esaminati, la loro localizzazione e l'eventuale presenza di tumore. Queste informazioni aiutano a determinare lo stadio linfonodale e svolgono un ruolo fondamentale nella scelta del trattamento.

Stadio patologico (pTNM)
L'adenocarcinoma polmonare viene stadiato utilizzando il sistema TNM:
-
Lo stadio T descrive le dimensioni del tumore e se ha invaso le strutture vicine.
-
Lo stadio N indica se i linfonodi contengono cancro.
-
Lo stadio M indica se il cancro si è diffuso a organi distanti, come il cervello, le ossa o il fegato.
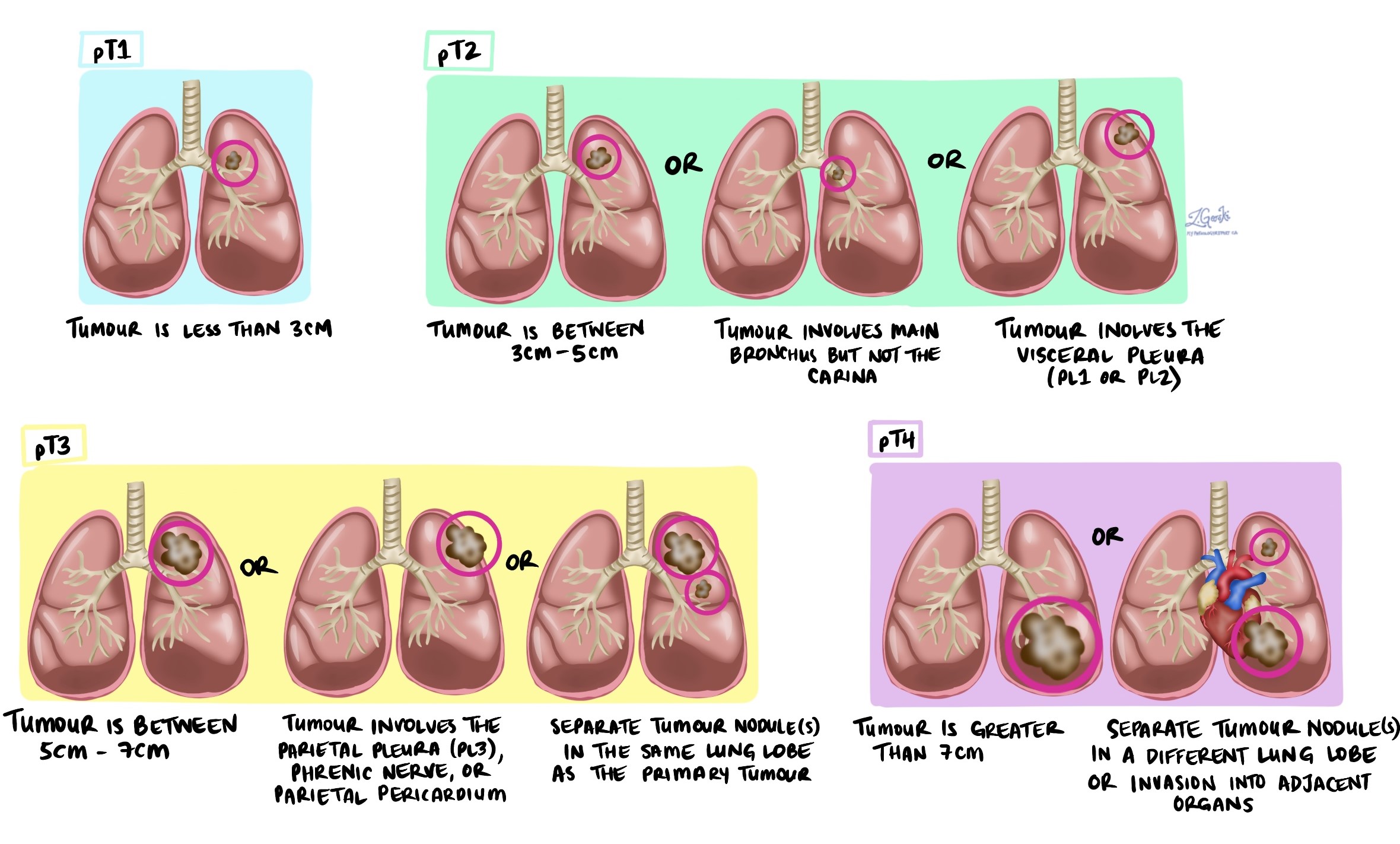
Stadio del tumore (pT)
-
T1: il tumore è di 3 cm o più piccolo.
-
T2: Il tumore è più grande di 3 cm ma non più grande di 5 cm, oppure ha invaso la pleura viscerale o le vie aeree centrali.
-
T3: il tumore è più grande di 5 cm ma non più grande di 7 cm oppure è cresciuto nei tessuti adiacenti.
-
T4: il tumore è più grande di 7 cm o ha invaso organi vicini come il cuore o l'esofago.
Stadio nodale (pN)
-
NX: I linfonodi non sono stati esaminati.
-
N0: Nessuna cellula cancerosa nei linfonodi.
-
N1: Cellule cancerose nei linfonodi all'interno del polmone o in prossimità delle vie aeree (stazioni 10–14).
-
N2: Cellule cancerose nei linfonodi nella parte centrale del torace, vicino alle vie aeree (stazioni 7–9).
-
N3: Cellule cancerose nei linfonodi sul lato opposto del torace o nella parte inferiore del collo (stazioni 1–6).
Gli stadi più avanzati presentano un rischio maggiore di diffusione e recidiva e spesso richiedono un trattamento più intensivo.
Biomarcatori per l'adenocarcinoma del polmone
I biomarcatori sono cambiamenti misurabili nelle cellule tumorali, che spesso coinvolgono geni o proteine specifici. Questi cambiamenti aiutano i medici a comprendere il comportamento del tumore e quali trattamenti potrebbero essere più efficaci. Nell'adenocarcinoma polmonare, i biomarcatori sono particolarmente importanti perché molti tumori presentano alterazioni genetiche che possono essere colpite con terapie che bloccano i segnali anomali che favoriscono la crescita del tumore. Il test dei biomarcatori è ormai parte integrante della diagnosi e guida molte decisioni terapeutiche.
Quali tipi di biomarcatori vengono testati nell'adenocarcinoma polmonare?
La maggior parte dei test sui biomarcatori per l'adenocarcinoma polmonare si concentra sulle mutazioni genetiche e sui riarrangiamenti genici presenti nel DNA del tumore. Queste alterazioni vengono rilevate utilizzando tecniche di laboratorio specializzate come la PCR (un test che amplifica piccole porzioni di DNA), il sequenziamento di nuova generazione (NGS; un test che esamina più geni contemporaneamente) e la FISH (un test che utilizza sonde fluorescenti per rilevare i riarrangiamenti genici). Questi test vengono eseguiti su tessuto bioptico o sul tumore rimosso durante l'intervento chirurgico e svolgono un ruolo essenziale nel determinare quali trattamenti possano essere più efficaci.
EGFR
L'EGFR è un gene che codifica per un recettore che controlla la crescita cellulare. Quando l'EGFR ospita mutazioni specifiche, il recettore diventa iperattivo, stimolando la crescita tumorale. Le mutazioni dell'EGFR sono prevalenti nelle persone che non hanno mai fumato, nelle donne e negli individui di origine est-asiatica. Queste mutazioni sono importanti perché i tumori con alterazioni dell'EGFR spesso rispondono molto bene alle terapie mirate all'EGFR, che bloccano il segnale di crescita anomala e possono ridurre le dimensioni del tumore o rallentarne la progressione.
I patologi testano le mutazioni dell'EGFR esaminando il DNA del tumore mediante PCR o sequenziamento di nuova generazione per rilevare specifiche alterazioni genetiche.
Il referto patologico descriverà il tumore come EGFR-positivo se viene rilevata una mutazione e come EGFR-negativo se non viene rilevata alcuna mutazione.
ALK
ALK è un gene che può fondersi con un altro gene, creando una proteina di fusione anomala che promuove la crescita tumorale. Queste fusioni di ALK sono più comuni nei pazienti più giovani e nelle persone che non hanno mai fumato. I riarrangiamenti di ALK sono importanti perché i tumori con questa alterazione spesso rispondono eccezionalmente bene alle terapie mirate ad ALK, che bloccano la proteina di fusione anomala.
Il test ALK viene eseguito utilizzando l'immunoistochimica, che evidenzia la proteina ALK nelle cellule tumorali, la FISH, che rileva i riarrangiamenti del gene ALK, o il sequenziamento di nuova generazione, che analizza direttamente il gene ALK.
I tumori vengono descritti come ALK-positivi quando è presente un riarrangiamento e ALK-negativi quando non viene rilevato alcun riarrangiamento.
ROS1
ROS1 è un gene che può subire riarrangiamenti, formando una proteina di fusione che stimola la crescita tumorale. Sebbene meno comuni delle alterazioni di EGFR o ALK, le fusioni di ROS1 sono importanti perché rispondono molto bene alle terapie mirate a ROS1, che bloccano la proteina anomala e contribuiscono a controllare il cancro.
Il test ROS1 può essere eseguito mediante immunoistochimica, FISH o sequenziamento di nuova generazione per rilevare una fusione del gene ROS1.
Il tumore verrà descritto come ROS1-positivo se viene rilevata una fusione, altrimenti come ROS1-negativo.
FRATELLO
BRAF è un gene coinvolto nella regolazione della crescita cellulare. Mutazioni specifiche, come la mutazione BRAF V600E, possono causare una crescita più rapida delle cellule tumorali. Queste mutazioni sono importanti perché i tumori con alterazioni di BRAF possono rispondere alle terapie mirate a BRAF, che bloccano la via di segnalazione anomala.
Il test viene eseguito analizzando il DNA tumorale mediante PCR o sequenziamento di nuova generazione per identificare specifiche mutazioni BRAF.
Il tumore verrà descritto come BRAF-positivo se è presente una mutazione e BRAF-negativo se non viene rilevata alcuna mutazione.
MET
MET è un gene che aiuta a controllare la normale crescita cellulare. Un'anomalia specifica, lo "skipping" dell'esone 14 di MET, fa sì che la proteina MET rimanga attiva più a lungo del normale, consentendo alle cellule tumorali di crescere in modo incontrollato. Questo biomarcatore è importante perché i tumori con "skipping" dell'esone 14 di MET spesso rispondono alle terapie mirate a MET.
Il test MET viene solitamente eseguito utilizzando il sequenziamento di nuova generazione per rilevare il salto dell'esone 14 del gene MET o altre mutazioni del gene MET.
Il tumore verrà classificato come MET-positivo se viene rilevata una mutazione MET e come MET-negativo se non viene rilevata alcuna mutazione.
RET
RET è un gene che può fondersi con un altro gene, creando una proteina anomala che stimola la crescita tumorale. Le fusioni di RET sono importanti perché i tumori con questa alterazione spesso rispondono eccezionalmente bene alle terapie mirate a RET.
Le fusioni RET vengono identificate mediante sequenziamento di nuova generazione o FISH, entrambe in grado di rilevare il riarrangiamento anomalo.
Il tumore verrà descritto come RET-positivo se è presente una fusione e RET-negativo in caso contrario.
NTRK (NTRK1, NTRK2, NTRK3)
I geni NTRK possono fondersi con altri geni, creando proteine di fusione TRK anomale che promuovono fortemente la crescita tumorale. Sebbene rare, queste fusioni sono importanti perché i tumori con alterazioni di NTRK mostrano spesso risposte significative e durature alle terapie mirate a TRK.
Il test NTRK può comportare l'immunoistochimica per individuare l'espressione anomala della proteina TRK, seguita da FISH o sequenziamento di nuova generazione per confermare la presenza di una fusione genica.
Il tumore verrà descritto come NTRK-positivo se viene rilevata una fusione e come NTRK-negativo se non viene rilevata alcuna fusione.
KRAS
KRAS è un gene coinvolto nella regolazione della crescita e della divisione cellulare. Le mutazioni di KRAS sono tra i biomarcatori più comuni nell'adenocarcinoma polmonare, soprattutto nelle persone con una storia di fumo. Queste mutazioni sono importanti perché aiutano a predire il comportamento del tumore e perché una specifica mutazione di KRAS, KRAS G12C, può essere trattata con nuovi farmaci mirati a KRAS.
Le mutazioni KRAS vengono rilevate tramite PCR o sequenziamento di nuova generazione per analizzare il DNA tumorale.
Il tumore verrà descritto come KRAS-positivo se viene identificata una mutazione e come KRAS-negativo se non viene trovata alcuna mutazione.
ERBB2 (HER2)
ERBB2, noto anche come HER2, è un gene che può acquisire mutazioni che portano a una segnalazione anomala e alla crescita tumorale. Le alterazioni di HER2 sono importanti perché terapie mirate – e studi clinici in corso – affrontano i tumori con mutazioni di HER2.
Il test HER2 viene eseguito utilizzando il sequenziamento di nuova generazione per rilevare le mutazioni ERBB2 nel DNA del tumore.
Il tumore verrà descritto come ERBB2-positivo se viene rilevata una mutazione, e come ERBB2-negativo se non viene rilevata alcuna mutazione.
ANR
NRAS è un gene simile a KRAS che partecipa ai processi di crescita cellulare. Le mutazioni di NRAS sono più comuni nelle persone che hanno fumato. Sebbene non siano ancora disponibili trattamenti specifici mirati a NRAS, l'identificazione di una mutazione di NRAS aiuta i medici a comprendere il comportamento del tumore e a valutare le opzioni di sperimentazione clinica.
Il test NRAS viene eseguito utilizzando il sequenziamento di nuova generazione per ricercare mutazioni nel DNA del tumore.
Il tumore verrà descritto come NRAS-positivo se viene rilevata una mutazione e come NRAS-negativo se non viene rilevata alcuna mutazione.
MAP2K1 (MEK1)
MAP2K1, noto anche come MEK1, è un gene coinvolto in una via di segnalazione che regola la crescita cellulare. Le mutazioni di MAP2K1 sono importanti perché sono in fase di studio terapie mirate a questa via, che potrebbero diventare opzioni terapeutiche.
Il test MAP2K1 viene eseguito utilizzando il sequenziamento di nuova generazione per rilevare le mutazioni nel DNA tumorale.
Il tumore verrà descritto come MAP2K1-positivo se viene identificata una mutazione e MAP2K1-negativo se non viene trovata alcuna mutazione.
NRG1
NRG1 è un gene che può formare riarrangiamenti o fusioni che promuovono la crescita tumorale. Sebbene rari, i riarrangiamenti di NRG1 sono importanti perché potrebbero essere sensibili alle nuove ed emergenti terapie mirate a NRG1 attualmente in fase di studio.
Il test NRG1 viene eseguito utilizzando il sequenziamento di nuova generazione per esaminare il DNA del tumore alla ricerca di prove di un riarrangiamento genico.
Il tumore verrà descritto come NRG1-positivo se viene rilevato un riarrangiamento e come NRG1-negativo se non viene rilevato alcun riarrangiamento.
PD-L1
PD-L1 è una proteina presente sulla superficie di alcune cellule tumorali. Interagisce con le cellule immunitarie in un modo che consente al tumore di eludere il sistema immunitario ed evitare la distruzione. PD-L1 è importante perché i tumori con elevata espressione di PD-L1 hanno maggiori probabilità di rispondere all'immunoterapia, un tipo di trattamento che aiuta il sistema immunitario a riconoscere e attaccare le cellule tumorali. I farmaci immunoterapici chiamati inibitori di PD-1 o PD-L1 sono ora trattamenti standard per molti pazienti con adenocarcinoma polmonare, soprattutto quando il tumore mostra elevati livelli di PD-L1.
I patologi testano la PD-L1 utilizzando l'immunoistochimica, una tecnica di laboratorio che utilizza anticorpi legati a coloranti per legarsi alla proteina PD-L1 e renderla visibile al microscopio. Il test misura quante cellule tumorali mostrano PD-L1 sulla loro superficie e quanto intensamente lo esprimono. Questo test viene solitamente eseguito su un campione bioptico prima dell'inizio del trattamento.
I risultati del test PD-L1 sono riportati in percentuale, rappresentando la proporzione di cellule tumorali che presentano colorazione PD-L1. Questo valore è chiamato Tumour Proportion Score (TPS).
-
Un TPS <1% è considerato PD-L1-negativo o molto basso.
-
Un TPS compreso tra 1 e 49% è considerato un'espressione da bassa a intermedia.
-
Un TPS pari o superiore al 50% è considerato ad alta espressione.
Alcuni report possono includere anche punteggi per le cellule immunitarie o utilizzare il punteggio positivo combinato (CPS), a seconda del metodo di test utilizzato.
Dopo la diagnosi
Dopo la conferma della diagnosi, il medico esaminerà il referto istologico, gli esami di diagnostica per immagini e le condizioni generali del paziente per elaborare un piano di trattamento personalizzato. Il trattamento può includere un intervento chirurgico, chemioterapia, immunoterapia, terapia mirata, radioterapia o una combinazione di questi approcci.
È importante eseguire test molecolari sul tumore. Molti adenocarcinomi polmonari presentano alterazioni genetiche specifiche, come mutazioni in EGFR, ALK, ROS1, KRAS o RET, che possono essere trattate con terapie altamente efficaci. I test molecolari sono ormai una parte standard ed essenziale della cura del cancro al polmone, anche nelle fasi iniziali della malattia.
Il team sanitario potrebbe anche discutere di ulteriori esami di diagnostica per immagini per verificare la diffusione del tumore, test di funzionalità polmonare per valutare la capacità polmonare e strategie per gestire sintomi come tosse o mancanza di respiro. Il follow-up dopo il trattamento è importante per monitorare eventuali recidive o lo sviluppo di nuovi noduli polmonari.
Domande da porre al medico
-
In che stadio si trova il mio tumore e cosa comporta per il mio piano terapeutico?
-
Nel mio tumore è stata riscontrata invasione pleurica, invasione linfovascolare o STAS?
-
I margini chirurgici erano puliti?
-
Il cancro si è diffuso a qualche linfonodo?
-
Ho bisogno di test molecolari per EGFR, ALK, KRAS o altri biomarcatori?
-
Quali trattamenti consigliate e quali sono i loro obiettivi?
-
Dovrei consultare un oncologo medico, un radioterapista o un chirurgo per ulteriori cure?
-
Quale programma di follow-up consigliate dopo il trattamento?