Por Jason Wasserman, MD PhD FRCPC y Zuzanna Gorski, MD FRCPC
14 de Mayo de 2026
Lesión intraepitelial escamosa de alto grado (HSIL) Es una condición precancerosa del cuello uterino causada por una infección con virus del papiloma humano (VPH)Está compuesto por células escamosas infectadas y alteradas por el virus. Estas células anormales se encuentran en el zona de transformación, la parte del cuello uterino donde las células glandulares son reemplazadas gradualmente por células escamosas. HSIL no es cáncer, pero se considera un cambio precanceroso grave porque puede progresar con el tiempo a un tipo de cáncer de cuello uterino llamado Carcinoma de células escamosas asociado al VPH Si no se trata.
Otro nombre para HSIL es neoplasia intraepitelial cervical (CIN). La CIN se divide en tres niveles según su gravedad: CIN1, CIN2 y CIN3. HSIL corresponde a CIN2 y CIN3, que se consideran cambios de alto grado. La forma de menor grado, CIN1, se llama lesión intraepitelial escamosa de bajo grado (LSIL) y se comporta de manera muy diferente. Este artículo le ayudará a comprender los hallazgos de su informe de patología: qué significa cada término y por qué es importante para su atención médica.
¿Qué causa la HSIL?
HSIL es causada por una infección persistente con tipos de VPH de alto riesgoEl VPH es un virus muy común que se transmite por contacto piel con piel, incluyendo el contacto sexual. Los tipos de alto riesgo más frecuentemente asociados con HSIL y cáncer de cuello uterino incluyen el VPH16 y el VPH18, junto con el VPH31, 33, 45, 52 y 58. Estos virus producen proteínas que interfieren con los sistemas que controlan el crecimiento celular normal y, con el tiempo, pueden provocar un crecimiento anormal de las células escamosas.
La mayoría de las infecciones por VPH no derivan en HSIL. En la mayoría de las personas, el sistema inmunitario elimina el virus en uno o dos años, y los cambios celulares se resuelven con él. Solo un pequeño porcentaje de infecciones persiste en el cuello uterino el tiempo suficiente para causar cambios precancerosos. Varios factores aumentan la probabilidad de infección persistente y progresión a HSIL:
- Infección persistente por VPH de alto riesgo — Las infecciones que duran dos años o más son el factor de riesgo más importante para la HSIL (lesión intraepitelial escamosa de alto grado).
- Un sistema inmunitario debilitado — Condiciones como la infección por VIH, el trasplante de órganos o la terapia inmunosupresora a largo plazo dificultan que el cuerpo elimine el virus.
- Fumar cigarrillos — Fumar daña las células cervicales y las hace más vulnerables a los cambios relacionados con el VPH.
- Uso prolongado de anticonceptivos orales — En algunos estudios se ha asociado con un riesgo ligeramente mayor.
- Falta de exámenes de detección de cáncer de cuello uterino regulares — Sin pruebas de detección precoz, los cambios precancerosos pueden pasar desapercibidos durante muchos años.
¿Cuáles son los síntomas?
La mayoría de las personas con HSIL no presentan síntomas. Las células anormales en el HSIL se limitan a la superficie del cuello uterino y no invaden los tejidos más profundos, por lo que generalmente no causan sangrado, dolor ni secreción. Por esta razón, el HSIL casi siempre se detecta mediante exámenes de detección rutinarios de cáncer de cuello uterino, y no debido a la presencia de síntomas.
Cuando se presentan síntomas, estos pueden incluir sangrado vaginal anormal (como sangrado después de las relaciones sexuales o entre períodos), flujo vaginal inusual que puede ser acuoso o con sangre, o molestias pélvicas, aunque el dolor pélvico es poco común. Estos síntomas no son específicos de HSIL y pueden ser consecuencia de muchas otras afecciones menos graves. Dado que HSIL en sí mismo rara vez causa síntomas perceptibles, es importante realizar un seguimiento regular. Prueba de Papanicolaou y las pruebas de VPH siguen siendo la forma más fiable de detectarlo antes de que tenga la oportunidad de progresar.
¿Cómo se hace el diagnóstico?
La HSIL se sospecha con mayor frecuencia por primera vez cuando una prueba de Papanicolaou muestra células escamosas anormales, o cuando una Prueba de VPH es positivo para los tipos de alto riesgo. Cuando se encuentra cualquiera de los resultados, el siguiente paso suele ser una colposcopia: un examen del cuello uterino utilizando un colposcopio, un instrumento de aumento que permite al médico observar de cerca su superficie. Durante la colposcopia, se toma una pequeña muestra de tejido llamada biopsia Se toma una muestra de cualquier área que parezca anormal y se envía al laboratorio para su análisis. También se puede tomar una segunda muestra, denominada legrado endocervical, del interior del canal cervical para detectar cambios que no se pueden observar completamente con el colposcopio.
Bajo el microscopio, la patólogo identifica HSIL examinando cuánto del revestimiento superficial del cuello uterino (el epitelio) ha sido reemplazado por células escamosas anormales. En HSIL, las células anormales se extienden a través de al menos dos tercios del espesor del epitelio y carecen de la maduración normal que se observa en las células escamosas sanas.
Para respaldar el diagnóstico, a menudo se realizan pruebas adicionales. Una tinción de proteínas llamada p16, interpretado por inmunohistoquímica, casi siempre muestra una tinción fuerte y continua de tipo "bloque" en HSIL porque las células infectadas con VPH de alto riesgo producen grandes cantidades de esta proteína. Este patrón de tinción apoya el diagnóstico de HSIL y ayuda a distinguirlo de LSIL y otras afecciones que pueden verse similares bajo el microscopio. Cuando el diagnóstico es incierto, una prueba llamada hibridación in situ (ISH) También se puede utilizar para detectar material genético del VPH directamente dentro de las células, confirmando si las células anormales son causadas por el VPH y, en ocasiones, identificando el tipo específico de VPH.
¿Cómo se ve el HSIL bajo el microscopio?
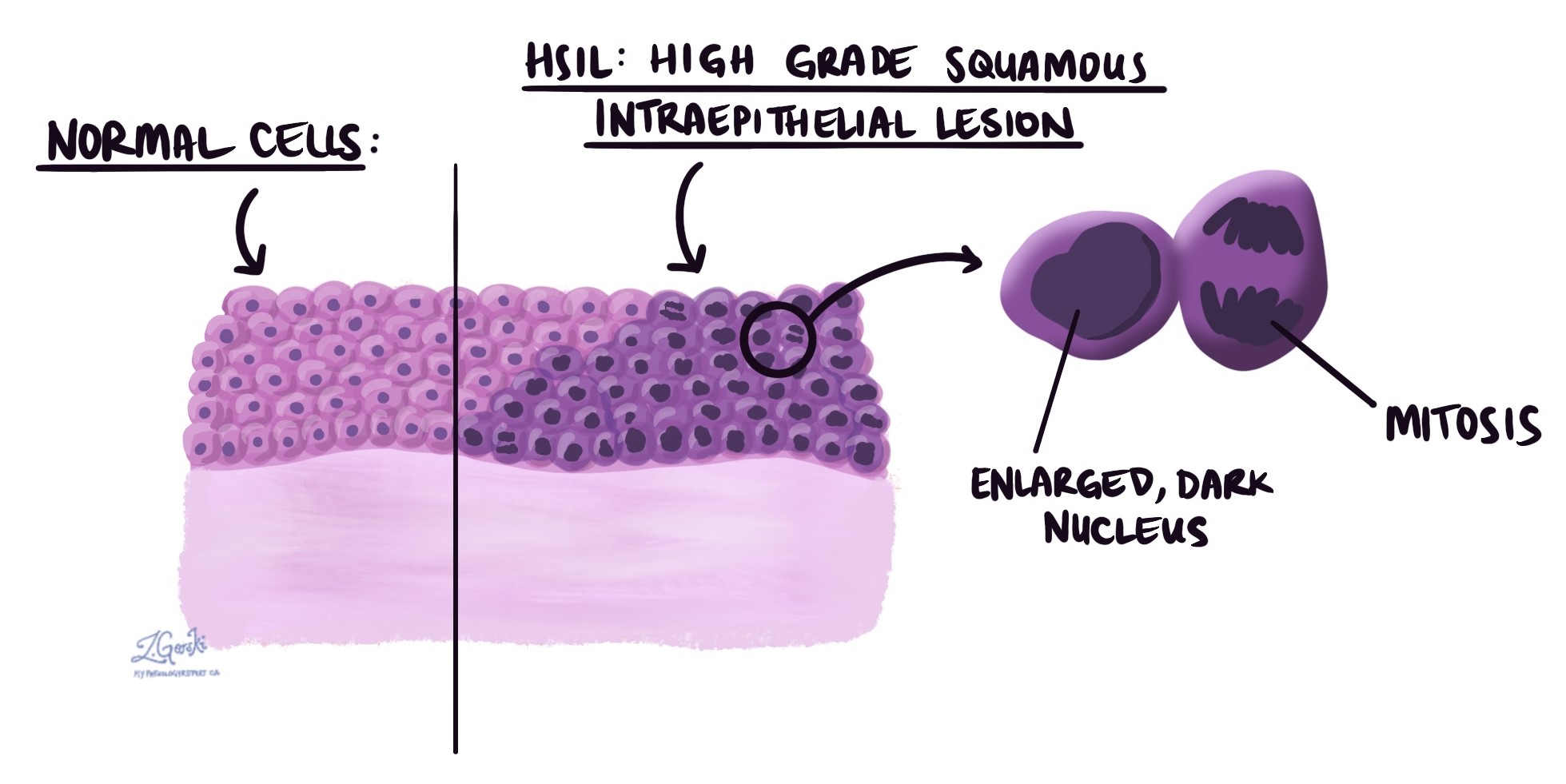
Bajo el microscopio, la HSIL se compone de células escamosas anormales, más oscuras y grandes de lo normal, que ocupan los dos tercios superiores o la totalidad del espesor del revestimiento superficial del cuello uterino. Estas células permanecen confinadas al epitelio y no han invadido los tejidos más profundos, lo que convierte a la HSIL en una lesión precancerosa en lugar de cancerosa. Varias características ayudan al patólogo a reconocer la HSIL:
- Núcleos oscuros y agrandados — Los núcleos (las partes de las células que contienen material genético) aparecen más oscuros de lo normal, una característica denominada hipercromasia.
- Pérdida de la maduración normal — Las células escamosas sanas se vuelven progresivamente más planas y maduras a medida que se desplazan hacia la superficie. En la HSIL, esta maduración ordenada se pierde y las células de aspecto inmaduro se extienden hacia el interior del epitelio.
- Alta relación núcleo-citoplasma — Las células tienen menos citoplasma (el cuerpo de la célula) en relación con el tamaño del núcleo, lo que hace que su aspecto general sea oscuro y denso.
- Muchas figuras mitóticas — Figuras mitóticas Las células en división son numerosas, incluyendo a menudo formas anormales llamadas figuras mitóticas atípicas. Muchas de estas células en división se observan por encima del tercio inferior del epitelio, que es donde normalmente deberían estar confinadas.
- Coilocitos ocasionales — Coilocitos Son células con núcleos irregulares y un espacio claro (o “halo”) alrededor del núcleo, causadas por la infección por VPH. Son más típicas de las LSIL, pero también pueden estar presentes en las HSIL.
¿En qué se diferencia HSIL de LSIL?
Tanto la lesión intraepitelial escamosa de alto grado (HSIL) como la de bajo grado (LSIL) son causadas por la infección del cuello uterino por el virus del papiloma humano (VPH), pero difieren en el aspecto que tienen las células al microscopio, en la probabilidad de que se resuelvan por sí solas y en su tratamiento.
LSIL (que corresponde a CIN1) es una lesión de bajo grado en la que las células escamosas anormales se localizan en el tercio inferior del epitelio. El riesgo de que LSIL progrese a cáncer es bajo, y la mayoría de los casos se resuelven espontáneamente a medida que el sistema inmunitario elimina la infección subyacente por VPH. Por este motivo, LSIL suele controlarse mediante un seguimiento exhaustivo en lugar de un tratamiento inmediato.
La HSIL (que corresponde a CIN2 y CIN3) es una lesión de alto grado en la que las células anormales se extienden por al menos dos tercios del epitelio. La HSIL tiene muchas menos probabilidades de resolverse espontáneamente y conlleva un riesgo significativo de progresar a cáncer de cuello uterino con el tiempo si no se trata. Debido a este riesgo, el enfoque estándar cuando se confirma la HSIL mediante biopsia es extirpar la zona afectada.
Márgenes quirúrgicos
A margen Es el borde de corte del tejido extirpado durante un procedimiento de escisión. Tras la cirugía, el patólogo examina los márgenes al microscopio para determinar si hay células HSIL presentes en el borde de corte. Los márgenes se informan únicamente en muestras de escisión, como en un procedimiento de escisión electroquirúrgica con asa (LEEP) o una biopsia cónica. No se informan en las pruebas de Papanicolaou ni en las biopsias pequeñas, cuyo objetivo no es extirpar la lesión por completo.
- Margen negativo — No se observan células HSIL en el borde de corte del tejido. Este resultado sugiere que la zona anómala se extirpó por completo, lo cual es el desenlace más alentador.
- Margen positivo — Las células HSIL están presentes en el borde de la incisión. Esto significa que algunas células anormales pueden permanecer en el cuello uterino, lo que aumenta el riesgo de recurrencia de HSIL y lleva al equipo ginecológico a considerar la posibilidad de una nueva escisión o un seguimiento más exhaustivo.
En las muestras de escisión cervical se evalúan tres ubicaciones de los márgenes:
- Margen endocervical — El borde interno de la muestra, el más cercano al útero. La afectación de este margen es particularmente significativa porque las células anormales pueden permanecer en la parte superior del canal endocervical, donde son difíciles de detectar en las pruebas de seguimiento.
- Margen ectocervical — El borde exterior del espécimen, el más cercano a la vagina.
- Margen estromal — El borde profundo, que corresponde a la pared del cuello uterino debajo del tejido extirpado.
¿Cuál es el pronóstico?
Con tratamiento, el pronóstico para HSIL es excelente en la mayoría de los casos. La mayoría de las pacientes se curan después de una sola escisión, y el riesgo de progresión a cáncer de cuello uterino disminuye sustancialmente una vez que se ha extirpado el tejido anormal. Varias características en el informe de patología influyen en la probabilidad de recurrencia o progresión:
- Estado de los márgenes después de la escisión — Los márgenes negativos se asocian con una baja tasa de recurrencia, generalmente entre el 5 y el 10 % a lo largo de los años posteriores al tratamiento. Los márgenes positivos, especialmente en el borde endocervical, se asocian con un riesgo sustancialmente mayor de enfermedad residual o recurrente.
- Eliminación del VPH después del tratamiento — Un resultado negativo en la prueba del VPH entre seis y doce meses después del tratamiento es uno de los indicadores más fiables de que la infección subyacente se ha eliminado y el riesgo de recurrencia es bajo. La persistencia de la infección por VPH tras el tratamiento es el factor predictivo más importante de recurrencia.
- Grado de la lesión — El riesgo de progresión a cáncer sin tratamiento es significativamente mayor en el caso de CIN3 que en el de CIN2. Sin embargo, con tratamiento, ambos se manejan de manera similar y el pronóstico es parecido.
- Estado inmunológico — Las personas con sistemas inmunitarios debilitados (infección por VIH, trasplante de órganos, inmunosupresión a largo plazo) tienen un mayor riesgo de recurrencia y pueden requerir una vigilancia más estrecha.
- Riesgo de progresión sin tratamiento — Cuando no se trata la HSIL, los estudios indican que una proporción significativa de las lesiones CIN3 progresa a cáncer de cuello uterino invasivo en un período de años a décadas. La CIN2 presenta una tasa de progresión menor, pero aún significativa, y un porcentaje notable de lesiones CIN2 también se resuelve espontáneamente, especialmente en pacientes jóvenes.
¿Qué sucede después de este diagnóstico?
Una vez confirmada la presencia de HSIL mediante biopsia, el equipo ginecológico analizará las opciones para el tratamiento de la zona afectada. Dado que la HSIL conlleva un riesgo significativo de progresar a cáncer de cuello uterino con el tiempo, el enfoque estándar consiste en extirpar el tejido anormal. La elección del procedimiento depende del tamaño y la ubicación de la lesión, su edad, su deseo de preservar la fertilidad y su historial médico general.
Entre las opciones que el equipo podría considerar se incluyen:
- Procedimiento de escisión electroquirúrgica con asa (LEEP) — Un fino lazo de alambre calentado por una corriente eléctrica elimina una capa de tejido cervical, incluida la zona de transformación. La LEEP es el procedimiento más común para la HSIL porque elimina la zona anormal y, al mismo tiempo, proporciona tejido que el patólogo puede examinar exhaustivamente para determinar el estado de los márgenes y detectar cualquier hallazgo inesperado.
- Biopsia cónica con bisturí frío (conización) — En el quirófano se extirpa quirúrgicamente una porción cónica del cuello uterino. Esta opción se suele considerar cuando se necesita una muestra más grande o profunda, cuando la zona anómala se extiende hacia la parte superior del canal endocervical o cuando existe la sospecha de que pueda haber un cáncer en etapa temprana.
- Procedimientos ablativos (crioterapia, ablación láser) — Estos métodos destruyen el tejido anormal en lugar de extirparlo. Se utilizan con menos frecuencia para las lesiones intraepiteliales escamosas de alto grado (HSIL) porque no proporcionan tejido para el examen patológico, lo que significa que no se puede evaluar el estado de los márgenes y podría pasar desapercibido un pequeño cáncer subyacente.
- Vigilancia estrecha sin tratamiento inmediato — En casos seleccionados, sobre todo en pacientes jóvenes con CIN2 que desean preservar su fertilidad, se puede considerar la vigilancia con pruebas repetidas de Papanicolaou y VPH en lugar de la escisión inmediata. Esta opción se contempla a veces porque una proporción significativa de las lesiones CIN2 se resuelven espontáneamente, especialmente en personas menores de 25 años.
Tras el tratamiento, es fundamental realizar un seguimiento continuo para detectar cualquier recurrencia a tiempo. El programa de seguimiento estándar incluye la prueba de Papanicolaou y la prueba del VPH seis meses después del tratamiento, con pruebas adicionales a los 12 y 24 meses. Tras dos resultados negativos consecutivos, la mayoría de las pacientes pueden retomar los intervalos de detección habituales. Su médico o ginecólogo adaptará este programa según sus resultados histopatológicos específicos, el estado de los márgenes, los resultados de la prueba del VPH y su historial médico general.
Preguntas para hacerle a su médico
- ¿Mi biopsia confirmó la presencia de HSIL y se describió como CIN2 o CIN3?
- ¿Se analizó mi muestra para detectar la proteína p16 y cuál fue el resultado?
- ¿Mi muestra dio positivo para VPH de alto riesgo? Y, de ser así, ¿de qué tipo?
- ¿Qué opciones de tratamiento me recomendaría y cuáles son las ventajas y desventajas de cada una?
- Quiero preservar mi fertilidad; ¿cómo influye eso en la elección del procedimiento?
- Si la vigilancia estrecha es una opción para mí, ¿cómo sería el programa de vigilancia?
- Si me someto a un procedimiento, ¿los márgenes quirúrgicos estuvieron libres de tumor y qué significan los resultados de los márgenes para los próximos pasos?
- ¿Qué probabilidades tengo de que la HSIL reaparezca después del tratamiento?
- ¿Con qué frecuencia necesitaré pruebas de Papanicolaou y pruebas de VPH de seguimiento, y durante cuánto tiempo?
- ¿Cuándo puedo volver a someterme a las pruebas de detección rutinarias de cáncer de cuello uterino?
- ¿Debería considerar la vacunación contra el VPH si aún no me he vacunado?
- ¿Qué síntomas deberían motivarme a ponerme en contacto con usted entre citas?
Artículos relacionados en MyPathologyReport.com
- Neoplasia intraepitelial cervical (CIN)
- Lesión intraepitelial escamosa de bajo grado (LSIL) del cuello uterino
- Adenocarcinoma in situ (AIS) del cuello uterino
- Carcinoma de células escamosas del cuello uterino asociado al VPH
- Carcinoma de células escamosas del cuello uterino independiente del VPH
- ASC-H del cuello uterino
- ASC-US del cuello uterino
- Negativo para lesión intraepitelial o malignidad (NILM)
- La prueba de Papanicolaou
- Virus del papiloma humano (VPH)
- VPH de alto riesgo
- p16